
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Тепловые эффекты различных процессов
|
|
1. Теплота растворения – это количество энергии, которое выделяется или поглощается при растворении 1 моля вещества в количестве растворителя, достаточном для полной сольватации (на 1 моль вещества 300 – 400 молей растворителя).
Теплота растворения равна сумме двух слагаемых:
DНрастворения = DН1 + DН2
где DН1 – теплота перехода твердого или газообразного вещества в то состояние, в котором оно существует в растворе.
DН2 – теплота взаимодействия растворяемого вещества с растворителем (теплота сольватации или теплота гидратации, если растворителем является вода).
DН2 всегда отрицательна, а DН1 может быть и положительна и отрицательна.
П
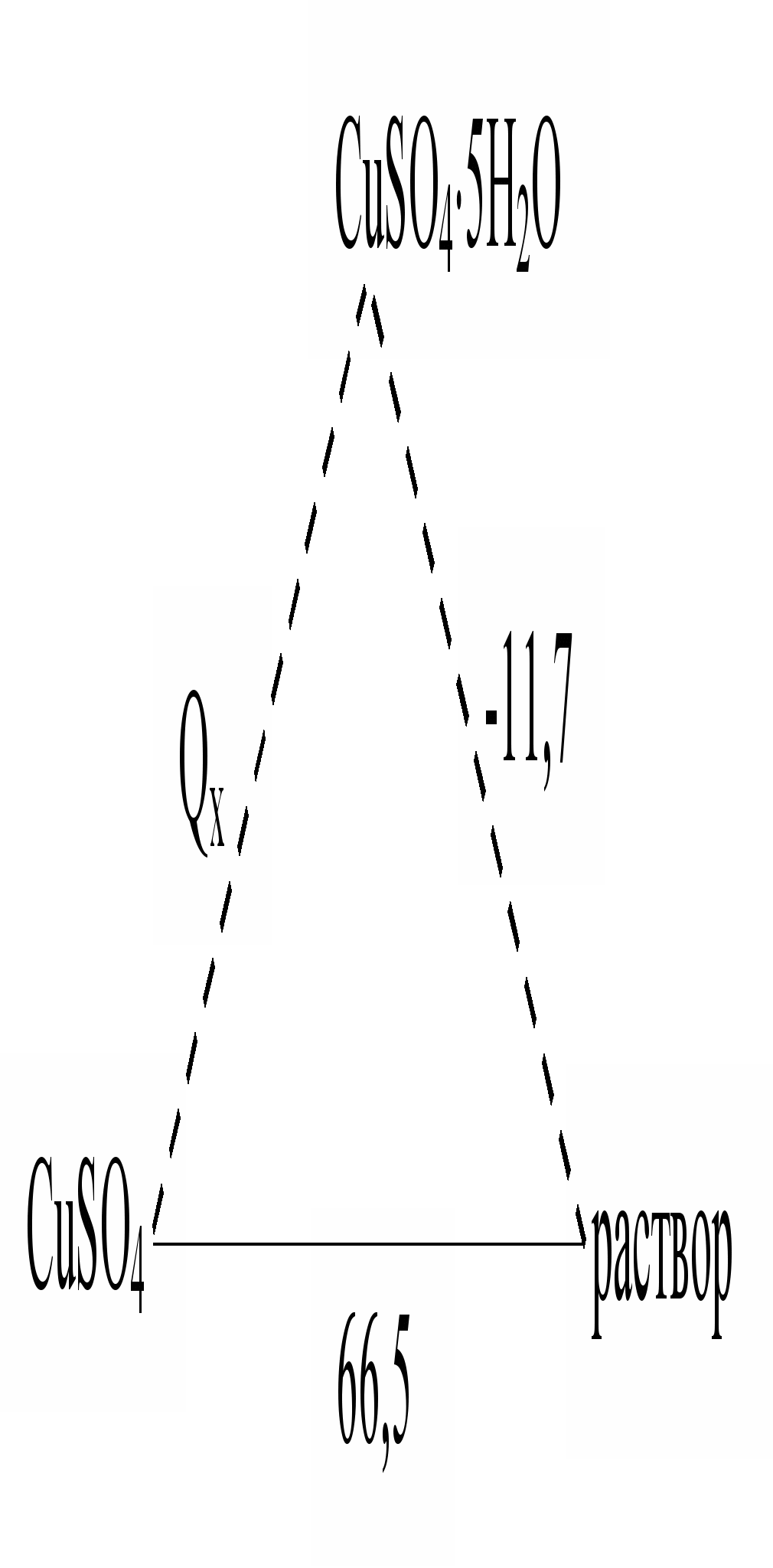
ример. Вычислить тепловой эффект перехода CuSO4 ®CuSO4×5H2O (теплоту гидратации), если теплота растворения CuSO4 и CuSO4×5H2O равны 66,5 и –11,7 кДж соответственно. Исходя из закона Гесса:
66,5 = Qx –11,7.
Отсюда: Qх = + 78,2 кДж; DН = –78,2кДж
2. ^ Теплота нейтрализации – это количество энергии, которое выделяется при образовании одного моля воды из Н+ (Н3О+) и ОН– при стандартных условиях:
NaOH + HCl = NaCl + H2O или
H+(aq) + OH–(aq) = H2O(ж) + 56,98 кДж
При взаимодействии сильной кислоты и сильного основания, независимо от их природы, теплота нейтрализации будет постоянной и равна 56,98 кДж.
Если в реакцию вступает слабая кислота или слабое основание, то теплота нейтрализации будет меньше, так как ионизация кислоты (основания) потребует затраты энергии.
HCN + NaOH = NaCN + H2O + Q
HCN + OH– = CN– + H2O + Q; Q < 56,98 кДж
3. ^ Теплота фазовых превращений – это количество энергии, которое выделяется или поглощается в процессе перехода компонентов системы из одной фазы в другую.
Пример. Вычислить тепловой эффект перехода Si (аморфный) ® Si (кристаллический), если теплоты сгорания этих модификаций составляют 867,3 и 850,6 кДж соответственно. Аморфный кремний можно сразу окислить до SiO2:
Si(ам) + О2 =SiO2 + 867,3 кДж, а можно сначала превратить его в кристаллическую модификацию, которую затем подвергнуть окислению.
1. Si (ам) = Si (крист.) + Qx
2. Si (крист.) + О2 = SiO2 + 850,6 кДж
867,3 – 850,6 = 16,7 кДж
DН = – 16,7 кДж
Date: 2015-05-22; view: 1256; Нарушение авторских прав