
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Загальні відомості. Класифікація
|
|
Теплоємкість – одна з найважливіших термодинамічних характеристик, що використовується при розрахунках теплоти процесів, теплових ефектів хімічних реакцій, теплових балансів металургійних процесів тощо.
Теплоємкістю називається величина, що показує, яку кількість теплоти треба надати одиниці маси речовини, щоб підвищити її температуру на один кельвін. Теплоємкість позначається буквою С.
Теплоємкість класифікують за трьома напрямками. В залежності від маси речовини (мольна або питома), в залежності від процесу (ізобарна або ізохорна) і в залежності від температури (істинна або середня).
Мольна (молярна) теплоємкість (С) показує кількість теплоти, що потрібна для нагрівання одного моль речовини на один кельвін. Вона вимірюється в Дж/(моль×К).
Питома теплоємкість (Спит.) показує кількість теплоти, що потрібна для нагрівання одного кілограма речовини на один кельвін. Питома теплоємкість вимірюється в Дж/(кг×К).
Співвідношення між мольною і питомою теплоємкостями визначається рівнянням
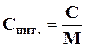 , (2.1)
, (2.1)
де М – мольна маса речовини, кг/моль.
Теплоємкість не є функцією стану системи, а визначається характером процесу. У прямому зв'язку з характером виробничих металургійних процесів, найбільшу цікавість представляє ізобарна теплоємкість (Ср) – теплоємкість при сталому тиску.
Для теоретичних розрахунків користуються також ізохорною теплоємкістю (СV) – теплоємкістю при сталому об'ємі.
Зрозуміло, що для всіх речовин Ср > СV, оскільки при Р = const частина теплоти витрачається на роботу проти сил зовнішнього тиску. Однак, для твердих і рідких речовин робота розширення мала і нею у практичних розрахунках нехтують. Виходячи з цього, а також враховуючи зміст понять мольної теплоємкості і об'ємної роботи, можна одержати наступні співвідношення між ізобарною і ізохорною теплоємкостями:
для газів 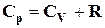 (формула Майера); (2.2)
(формула Майера); (2.2)
для твердих і рідких речовин Ср» СV. (2.3)
Суттєвий вплив на теплоємкість чинить температура. В залежності від температури, до якої відноситься теплоємкість, розрізняють істинну і середню теплоємкості.
Істинна теплоємкість (С) – це теплоємкість при певній температурі. Вона дорівнює відношенню нескінченно малої кількості теплоти (dQ), наданої одиниці маси речовини, до нескінченно малої зміни температури системи (dT), що відбувається при цьому
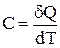 . (2.4)
. (2.4)
Зваживши, що при сталому тиску Qp = DН, а при сталому об'ємі QV = DU, можна записати:
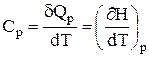 ;
;
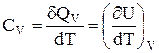 . (2.5)
. (2.5)
Отже, істинна ізобарна теплоємкість – це часткова похідна ентальпії за температурою при сталому тиску; істинна ізохорна теплоємкість – це часткова похідна внутрішньої енергії за температурою при сталому об'ємі.
Оскільки внутрішня енергія залежить лише від температури, часткові похідні в рівняннях (2.5) слід замінити на повні:
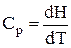 і
і 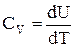 .
.
На практиці користуються середніми теплоємкостями (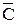 ).Середня теплоємкість дорівнює відношенню кількості теплоти, наданої одиниці маси речовини (Q), до відповідної зміни температури, що при цьому відбувається. Отже:
).Середня теплоємкість дорівнює відношенню кількості теплоти, наданої одиниці маси речовини (Q), до відповідної зміни температури, що при цьому відбувається. Отже:
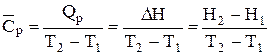 ;
;
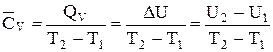 . (2.6)
. (2.6)
Середня теплоємкість постійна в інтервалі температур Т1¸Т2. Співвідношення між істинною і середньою теплоємкостями випливає при аналізі рівнянь (2.5 і 2.6):
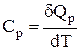 ;
; 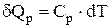 ;
;
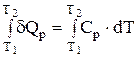 ;
;
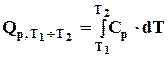 ; (2.7)
; (2.7)
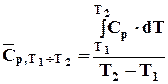 . (2.8)
. (2.8)
Date: 2015-05-08; view: 592; Нарушение авторских прав