
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Уравнение Клапейрона—Клаузиуса
|
|
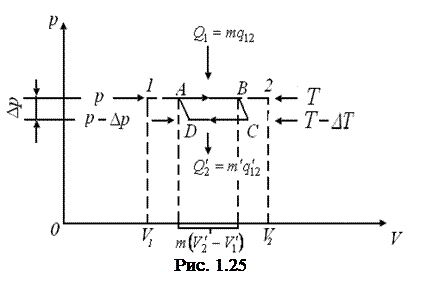 В предыдущих па-раграфах мы выяснили, что две любые фазы вещества могут находиться в равновесии лишь при определенном давлении, величина которого зависит от температуры. Общий вид этой зависимости можно получить, воспользовавшись понятием энтропии. Для этого рассмотрим цикл Карно для системы, состоящей из находящегося в равновесии двух фаз данного вещества.
В предыдущих па-раграфах мы выяснили, что две любые фазы вещества могут находиться в равновесии лишь при определенном давлении, величина которого зависит от температуры. Общий вид этой зависимости можно получить, воспользовавшись понятием энтропии. Для этого рассмотрим цикл Карно для системы, состоящей из находящегося в равновесии двух фаз данного вещества.
На диаграмме (р,V) цикл Карно для двухфазной системы имеет вид, показанный на рис. 1.25 (температуры нагревателя и холодильника предполагаются отличающимися на очень малую величину Δ T). Цифрами 1 и 2 помечены крайние точки горизонтального участка изотермы с температурой Т. Состояния 1 и 2 являются однофазными состояниями. Все промежуточные точки отрезка 1 и 2 изображают двухфазные состояния, отличающиеся друг от друга распределением массы вещества между первой и второй фазами.
Изотермический процесс А→В сопровождается фазовым превращением некоторой массы вещества m. При этом объем вещества получает приращение, равное 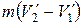 , где
, где 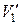 и
и 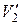 — удельные объемы первой и второй фаз. Для того чтобы такое превращение могло произойти, веществу нужно сообщить количество тепла Q1, равное
— удельные объемы первой и второй фаз. Для того чтобы такое превращение могло произойти, веществу нужно сообщить количество тепла Q1, равное 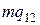 , где
, где 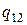 - удельная теплота, поглощаемая при переходе из состояния 1 в состояние 2 при температуре Т. Тепло Q1 представляет собой то тепло, которое получает система в ходе цикла от нагревателя. Холодильнику тепло отдается в ходе изотермического процесса С→D. Количество отданного тепла равно
- удельная теплота, поглощаемая при переходе из состояния 1 в состояние 2 при температуре Т. Тепло Q1 представляет собой то тепло, которое получает система в ходе цикла от нагревателя. Холодильнику тепло отдается в ходе изотермического процесса С→D. Количество отданного тепла равно 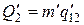 , где
, где 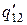 - теплота перехода 1-2 при температуре Т-DТ, а
- теплота перехода 1-2 при температуре Т-DТ, а 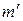 - масса вещества, претерпевающая фазовое превращение в ходе процесса С→D. Эта величина несколько отличается от m, так как некоторая масса вещества претерпевает фазовые превращения в ходе адиабатических процессов.
- масса вещества, претерпевающая фазовое превращение в ходе процесса С→D. Эта величина несколько отличается от m, так как некоторая масса вещества претерпевает фазовые превращения в ходе адиабатических процессов.
На изотермическом участке А-В энтропия системы получает приращение Δ S1, равное 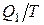 . На изотермическом участке С–D приращение энтропии равно
. На изотермическом участке С–D приращение энтропии равно 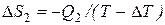 . В ходе адиабатических процессов В–С и D–А энтропия не изменяется. Полное приращение энтропии за цикл равно нулю. Следовательно,
. В ходе адиабатических процессов В–С и D–А энтропия не изменяется. Полное приращение энтропии за цикл равно нулю. Следовательно,
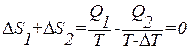 .
.
Отсюда
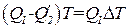 . (1.112)
. (1.112)
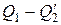 равно работе, совершаемой за цикл. Эту работу можно найти, вычислив площадь цикла. Приближенно площадь цикла можно считать равной
равно работе, совершаемой за цикл. Эту работу можно найти, вычислив площадь цикла. Приближенно площадь цикла можно считать равной 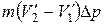 (рис. 1.25). Таким образом мы приходим к соотношению
(рис. 1.25). Таким образом мы приходим к соотношению
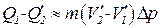 . (1.113)
. (1.113)
В пределе при Δ р, стремящемся к нулю (для чего необходимо, чтобы D Т также стремилось к нулю), соотношение (1.113) превращается в строгое равенство.
Подставим в (1.112) вместо 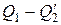 выражение (1.113). Кроме того, заменим Q 1 на
выражение (1.113). Кроме того, заменим Q 1 на 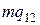 . В результате получим, что
. В результате получим, что
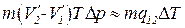 .
.
Отсюда
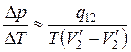 .
.
Наконец, совершив определенный переход Δ Т→0, придем к строгому равенству
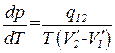 . (1.114)
. (1.114)
Полученное соотношение называется уравнением Клапейрона-Клаузиуса. Оно связывает производную от равновесного давления по температуре с теплотой перехода, температурой и разностью удельных объемов фаз, находящихся в равновесии.
Согласно (1.114) знак производной 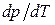 зависит от того, каким изменением объема - возрастанием или уменьшением - сопровождается фазовый переход, происходящий при поглощении тепла. При испарении жидкости или твердого тела объем всегда возрастает, поэтому производная
зависит от того, каким изменением объема - возрастанием или уменьшением - сопровождается фазовый переход, происходящий при поглощении тепла. При испарении жидкости или твердого тела объем всегда возрастает, поэтому производная 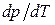 для кривой испарения, а также для кривой сублимации может быть только положительной: повышение температуры приводит к увеличению равновесного давления.
для кривой испарения, а также для кривой сублимации может быть только положительной: повышение температуры приводит к увеличению равновесного давления.
При плавлении объем, как правило, возрастает, так что 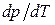 >0: увеличение давления приводит к повышению температуры плавления. Однако у некоторых веществ, к числу которых принадлежит и вода, объем жидкой фазы меньше объема твердой фазы
>0: увеличение давления приводит к повышению температуры плавления. Однако у некоторых веществ, к числу которых принадлежит и вода, объем жидкой фазы меньше объема твердой фазы 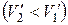 [11]. В этом случае
[11]. В этом случае 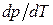 <0 - увеличение давления сопровождается понижением температуры плавления. Подвергнув лед сильному сжатию, можно, не повышая температуры выше 0°С, вызвать его плавление.
<0 - увеличение давления сопровождается понижением температуры плавления. Подвергнув лед сильному сжатию, можно, не повышая температуры выше 0°С, вызвать его плавление.
Температура перехода из одной кристаллической модификации в другую будет повышаться или понижаться с ростом давления в зависимости от того, какая из твердых фаз обладает большим удельным объемом.
Date: 2015-05-05; view: 895; Нарушение авторских прав