
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Твердых растворов
|
|
В условиях реальных скоростей охлаждения кристаллизующегося сплава (в земляной, либо металлической форме, или в кристаллизаторе – при получении слитков) от 10 -2 К/с до 10 2 К/с, всегда будут развиваться диффузионные процессы обмена на межфазной поверхности в течение всего периода кристаллизации (разделительная диффузия). При этом выравнивающая диффузия в жидкой фазе в основном проходит полностью, и практически, полностью подавляется гомогенизирующая диффузия внутри растущего твердого кристалла. В результате нарушаются равновесные условия кристаллизации, формируется химическая неоднородность по сечению кристаллов. В конечной структуре литого сплава наблюдается дендритная ликвация.
Рассмотрим кристаллизацию сплава Со системы с неограниченной растворимостью компонентов в твердом и жидком состояниях в неравновесных условиях (рисунок 3.2.1). Начальные этапы кристаллизации после переохлаждения ниже температуры ликвидуса практически не отличаются от таких же этапов кристаллизации в равновесных условиях за исключением того, что для образования первого зародыша твердой фазы требуется несколько более высокая степень переохлаждения.

|
Рисунок 3.2.1- Схема процессов неравновесной кристаллизации сплавов в системе с неограниченной растворимостью компонентов в твердом и жидком состояниях: а - диаграмма фазового равновесия с нанесенной схемой изменения состава фаз при неравновесной кристаллизации; б - схема кристалла с дендритной ликвацией
Неравновесная кристаллизация будет проходить с образованием большего количества одновременно зарождающихся кристаллов, при более высоких скоростях их роста, но в условиях меньшей диффузионной подвижности атомов (вследствие более низких температур превращения).
Рассмотрим кристаллизацию единичного кристалла a-твердого раствора в этих условиях (рисунок 3.2.1а). При переохлаждении жидкого раствора ниже температуры, соответствующей точке 1, в расплаве появляется тонкий разветвленный зародыш твердого раствора. Химический состав этого кристалла определяется точкой а на линии солидус, что соответствует концентрации компонентаВ в a-твердом растворе Са ( рисунок 3.2.1 б).
Понижение температуры до точки 2, как и в случае равновесной кристаллизации, вызовет осаждение на ранее образовавшемся дендритном зародыше нового слоя твердого раствора. Концентрация компонента В в новом слое твердой фазы будет соответствовать равновесной концентрации Сb (точка b на линии равновесного солидуса). Возникнув при переохлаждении, такой слой далее не растет в диффузионном режиме, поскольку диффузионные процессы в твердой фазе при неравновесной кристаллизации подавлены. В условиях непрерывного охлаждения по достижении температуры точки 2 можно определить мгновенное значение средней концентрации твердого раствора Се, как
 ,
,
где Ма - масса закристаллизовавшегося первого зародыша a-твердого раствора с концентрацией, равной Са; Мb – масса второго слоя с концентрацией компонента В - Сb.
Точка е, соответствующая такой средней концентрации a-твердого раствора, оказывается левее линии равновесного солидуса. Это означает, что закристаллизовавшийся твердый раствор оказывается не насыщенным по компоненту В.
Дальнейшее понижение температуры при кристаллизации до точки 3 приводит к появлению нового слоя a-твердого раствора. Концентрация компонента В в таком слое соответствует точке равновесного солидуса с - (слой Сс на схеме кристалла - рисунок 3.2.1, б). Роста слоя в диффузионном режиме, как и предыдущего, не наблюдается в связи с подавлением гомогенизации твердого раствора. Поэтому к температуре точки 3 растущий кристалл оказывается вновь неоднородным. Средний состав a-твердого раствора в первом приближении можно определить по выражению, аналогичному выше приведенному:
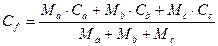 ,
,
где М и С с соответствующими индексами a, b, c - масса и концентрация компонента В в a-твердом растворе для первого зародыша и двух последовательно нараставших на его поверхность слоев.
Точка f, отвечающая средней мгновенной концентрации твердой фазы при температуре точки 3 в условиях непрерывного охлаждения, лежит также левее равновесного солидуса (слой Сf, на схеме кристалла, рисунок 3.2.1,б).
Далее при охлаждении до температуры точки 4 закристаллизуется новый тонкий слой a–твердого раствора с концентрацией компонента В, соответствующей точке d (слой Сd на схеме кристалла, рисунок 3.2.1,б). будет Точка g, определяющая средний состав твердой фазы, при температуре 4 оказывается левее точки d.
Это означает, что в условиях неравновесного ускоренного охлаждения кристаллизация сплава Со не заканчивается при температуре равновесного солидуса (точка 4). В сплаве кроме закристаллизовавшегося неоднородного по химическому составу кристалла твердой фазы содержится некоторое количество жидкости. Эта жидкость является неравновесной, поскольку содержит повышенное количество легкоплавкого компонента В, не перераспределившегося в центральные слои кристалла в связи с рассмотренными выше неравновесными условиями кристаллизации. Кристаллизация неравновесной жидкости должна завершиться в тот момент, когда средняя концентрация твердой фазы при неравновесной кристаллизации станет равной составу сплава, т.е. когда линия изменения среднего состава твердой фазы aefg (рисунок 3.2.1,а) пересечется с фигуративной линией сплава. Это соответствует точке h на линии среднего состава твердой фазы и температуре точки 5. Эта точка 5 является температурой неравновесного солидуса сплава Со для рассмотренных условий неравновесной кристаллизации. В этот момент образуется последний внешний слой кристалла, состав которого также определяется точкой m на равновесном солидусе (слой Сm на схеме кристалла, рисунок 3.2.1, б).
Таким образом, по сечению кристалла твердого раствора, формирующегося в условиях неравновесной кристаллизации, возникает химическая неоднородность, которая носит название: внутрикристаллитной или дендритной ликвации (рисунок 3.2.2).

| Рисунок 3.2.2. Сплав Cu – 30% Zn, a - латунь в литом состоянии. Структурная составляющая: кристаллы неоднородного a – твердого раствора Zn в Cu, ´100 |
Date: 2015-10-18; view: 1042; Нарушение авторских прав