
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Термодинамические условия кристаллизации
|
|
Гомогенное и гетерогенное зарождение кристаллов.
Кристаллизация может происходить как при переходе из жидкого состояния в твердое, так и в твердом состоянии при переходе из одной аллотропической формы в другую. Во втором случае такое превращение носит название «фазовая перекристаллизация».
Известно, что при постоянных температуре T и давлении p самопроизвольные процессы в системе идут в сторону уменьшения энергии Гиббса. Равновесное состояние характеризуется минимальным значением энергии Гиббса G = H – TS, где H – энтальпия, S - энтропия.
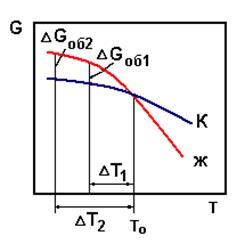
Рассмотрим кристаллизацию чистого металла. Изменение энергии Гиббса твердого (К) и жидкого (Ж) состояний металла от температуры показано на рисунке 1.2.1.
| ||
| Рис. 1.2.1. Зависимость объемной энергии Гиббса G чистого металла от температуры для жидкой и кристаллической фаз. | ||
Ниже температуры Т0 термодинамически устойчива кристаллическая фаза, обладающая меньшей энергией Гиббса, а выше Т0 – жидкая фаза.
Т0 - это температура, при которой жидкость находится в термодинамическом равновесии с твердой фазой. Чтобы началась кристаллизация, необходимо переохладить расплав ниже Т0, например, до Т1.
Разность DGоб1 (рис. 1.2.1) является термодинамическим стимулом (движущей силой) кристаллизации.
DТ1= Т0 - Т1 – величина или степень переохлаждения.
Степень переохлаждения – разность между Т0 и температурой Т, при которой может протекать процесс кристаллизации. Из рисунка видно, что чем больше степень переохлаждения, тем больше DGоб.
Установлено, что всякое фазовое превращение протекает путем возникновения в материнской (исходной) фазе небольших объемов новой фазы, называемых зародышевыми центрами, и последующего их роста.
Кинетика фазового превращения может быть оценена при помощи двух кристаллизационных параметров:
1) скорость зарождения центров (скорость образования зародышей) n, т.е. число центров, возникающих в единицу времени в единице объема [с-1×мм-3];
2) линейная скорость роста каждого кристалла [мм /c].
Чем больше количество возникающих зародышевых центров и больше скорость их роста, тем быстрее протекает фазовое превращение (кристаллизация).
Зародышевые центры новой фазы (в данном случае кристаллической, твердой) могут возникать в любых случайных объемах, а также на посторонних частицах, случайно присутствующих в расплаве.
Первый путь образования зародышевых центров называют гомогенным (самопроизвольным), а второй путь – гетерогенным (несамопроизвольным).
Дальнейший рост участков новой фазы подчиняется одним и тем же законам, независимо от способа образования зародышевых центров.
Рассмотрим самопроизвольное (гомогенное) образование центров кристаллизации.
При понижении температуры жидкого металла ниже Т0 в нем образуются зародыши кристаллов, которые растут за счет жидкой фазы. Такие зародыши образуются из групп атомов (кластеров). Группа атомов становится зародышем только в том случае, если при возникновении она имеет размеры, при которых может сопротивляться разрушающему воздействию движущихся атомов жидкости. В противном случае она распадается и не становится зародышем, способным развиваться в кристалл, т.е. размер зародыша должен быть не менее некоторой величины.
Предположим, что в расплаве образуется кристалл объемом V. Это приводит к снижению энергии Гиббса на величину
 , (1.2.1)
, (1.2.1)
где 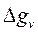 - изменение энергии Гиббса на единицу объема твердой фазы;
- изменение энергии Гиббса на единицу объема твердой фазы;

При зарождении кристалла возникает граница раздела между твердой и жидкой фазами, обладающая энергией
 , (1.2.2)
, (1.2.2)
где П – суммарная поверхность зародыша, s - удельная поверхностная энергия.
При этом энергия Гиббса возрастает на величину
 . (1.2.3)
. (1.2.3)
Общее изменение энергии Гиббса при возникновении кристалла объемом V равно:
DG=DGоб +DGпов, (1.2.4)
или
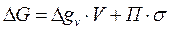 . (1.2.5)
. (1.2.5)
Примем, что зародыш имеет форму куба с размером ребра r. Тогда уравнение (1.2.5) можно записать в виде:
 . (1.2.6)
. (1.2.6)
Первое слагаемое пропорционально r3, а второе – r2. Поэтому при малом r величина DG растет, так как преобладает увеличение поверхностной энергии, а при большом r величина DG уменьшается вследствие абсолютного роста первого слагаемого.
Анализ уравнения (1.2.6) показывает, что функция DG=f(r) имеет максимум (рис. 1.2.2).

|
| Рис. 1.2.2. Зависимость изменения энергии Гиббса DG от размера кристалла r при температурах T1 и T2 (Т1>T2). |
Зародыш будет расти, если его размер r ≥ rкр (где rкр - критический размер), так как увеличение размера зародыша приведет к уменьшению DG. Критическое значение DGкр соответствует зародышу размером rкр. Если r < rкр, то зародыш расти не сможет, так как его рост привел бы к увеличению DG.
Следовательно, центрами кристаллизации являются кристаллики размером не менее критической величины.
Определим величину rкр. Для этого первую производную функции DG=f(r) приравняем к нулю:
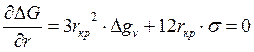 . (1.2.7)
. (1.2.7)
Отсюда
 . (1.2.8)
. (1.2.8)
Подставим rкр (выражение (1.2.8)) в уравнение (1.2.6). После соответствующих преобразований имеем
 . (1.2.9)
. (1.2.9)
Аналогичные выражения можно получить, если принять форму зародыша в виде шара радиусом r:
 ; (1.2.10)
; (1.2.10)
 ; (1.2.11)
; (1.2.11)
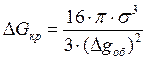 . (1.2.12)
. (1.2.12)
Видно, что выражения (1.2.8) и (1.2.12) различаются величиной коэффициента.
Так как при увеличении степени переохлаждения DТ межфазная энергия s практически не изменяется, а Dgоб непрерывно растет, то из формул (1.2.8) – (1.2.12) следует, что критический размер зародыша и работа его образования уменьшаются с ростом степени переохлаждения.
Откуда же берется энергия, необходимая для образования критического зародыша? В расплаве из-за хаотичного теплового движения всегда существуют группы атомов, кинетическая энергия которых как больше, так и меньше средней величины, характерной для данной температуры. Отклонение энергии от среднестатистического значения называют флуктуацией энергии.
Date: 2015-10-18; view: 4736; Нарушение авторских прав