
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Глава VII. Галогены
|
|
Реагируют почти со всеми простыми веществами, кроме некоторых неметаллов. Все галогены— энергичные окислители, поэтому встречаются в природе только в виде соединений. С увеличением порядкового номера химическая активность галогенов уменьшается, химическая активность галогенид-ионов F−, Cl−, Br−, I−, At− уменьшается.
К галогенам относятся фторF, хлорCl, бромBr, йодI, астатAt, а также (формально) искусственный элемент унунсептийUus.
| Фтор F | Хлор Cl | Бром Br | Йод I |

| 
| 
|
Все галогены— неметаллы. На внешнем энергетическом уровне 7электронов, являются сильными окислителями. При взаимодействии с металлами возникает ионная связь, и образуются соли. Галогены, (кроме F) при взаимодействии с более электроотрицательнымиэлементами, могут проявлять и восстановительные свойства вплоть до высшей степени окисления +7. Как уже было сказано выше, галогены имеют высокую реакционную способность, поэтому встречаются в природе обычно в виде соединений. Их распространённость в земной коре уменьшается при увеличении атомного радиуса от фтора к йоду. Количество астата в земной коре измеряется граммами, а унунсептий в природе отсутствует. Фтор, хлор, бром и йод производятся в промышленных масштабах, причем хлор производится в гораздо больших количествах. В природе эти элементы встречаются в основном в виде галогенидов(за исключением йода, который также встречается в виде йодата натрия или калия в месторождениях нитратов щелочных металлов).
Н2 + Br2 = 2HBr(г) + 73 кДж.
Поскольку многие хлориды, бромидыи иодидырастворимыв воде, то эти анионыприсутствуют в океане и природных рассолах. Основным источником фтора является фторид кальция, который очень малорастворими находится в осадочных породах (какфлюоритCaF2).
Основным способом получения простых веществявляется окислениегалогенидов. Впервые фтор был получен в1886г.французским химиком Анри Муассаномпри электролизераствора гидрофторида калия KHF2 в безводной плавиковой кислоте.
В лабораторных условиях хлор получают из соляной кислоты при взаимодействии ее с оксидом марганца (IV) при нагревании:
4HCl + MnO2 = Cl2 + MnCl2 + 2H2O
Вместо окислителя MnO2 можно применить перманганат калия. Реакция протекает при обычной температуре:
16HCl + 2KMnO4 = 5Cl2 + 2MnCl2 + 2KCl + 8H2O
В промышленности хлор в основном получают электролизом водного раствора хлорида натрияв специальных электролизёрах. При этом протекают следующие реакции:
полуреакция на аноде: 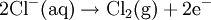
полуреакция на катоде: 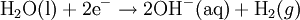
Бромполучают химическим окислением бромид-иона, находящегося в морской воде. Подобный процесс используется и для получения йодаиз природных рассолов, богатых I−. В качестве окислителя в обоих случаях используют хлор, обладающий более сильными окислительными свойствами, а образующиеся Br2 и I2 удаляются из раствора потоком воздуха.
Date: 2015-09-24; view: 889; Нарушение авторских прав