
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Задание 36 № 50. 3 page
|
|
2) 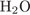 и
и 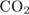
3)  и
и 
4) 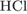 и
и 
9. Задание 9 № 3818. Разбавленная серная кислота реагирует с каждым из двух веществ:
1) железо и оксид серы(IV)
2) азотная кислота и оксид цинка
3) оксид углерода(IV) и оксид меди(II)
4) хлорид бария и цинк
10. Задание 10 № 4529. Раствор нитрата кальция взаимодействует с
1) 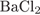
2) 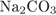
3) 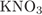
4) 
11. Задание 11 № 2163. Дана схема превращений:
SO2  Na2SO3
Na2SO3  Na2SO4
Na2SO4
Определите вещества X и Y.
1) Х − NaCl, Y − K2SO4
2) X − NaHSO3, Y − H2SO4
3) X − NaOH, Y − H2SO4
4) X − Na2O, Y − BaSO4
12. Задание 12 № 157. Бутен-1 является структурным изомером
1) бутана
2) циклобутана
3) бутина
4) бутадиена
13. Задание 13 № 3696. С хлороводородом может реагировать
1) пентан
2) толуол
3) циклогексан
4) циклопропан
14. Задание 14 № 3823. В отличие от метанола, этанол вступает в реакцию
1) гидрирования
2) внутримолекулярной дегидратации
3) этерификации
4) дегидрирования
15. Задание 15 № 2081. Верны ли следующие суждения о свойствах муравьиной кислоты?
А. Вступает в реакцию «серебряного зеркала».
Б. При комнатной температуре является твердым веществом.
1) верно только А
2) верно только Б
3) верны оба утверждения
4) оба утверждения неверны
16. Задание 16 № 591. Глицерин можно получить в результате гидролиза
1) белка
2) жира
3) крахмала
4) целлюлозы
17. Задание 17 № 1997. Определите органическое вещество Y в схеме превращений:
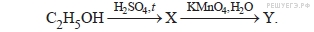
1) СН3СООК
2) СН3СООН
3) СН3СНО
4) НОСН2СН2ОН
18. Задание 18 № 2430. К необратимым реакциям относят
1) взаимодействие азота с водородом
2) гидролиз карбоната натрия
3) гидролиз карбида кальция
4) взаимодействие этилового спирта с уксусной кислотой
19. Задание 19 № 895. С наибольшей скоростью при комнатной температуре протекает реакция
1) 
2) 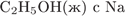
3) 
4) 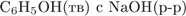
20. Задание 20 № 2000. При увеличении давления увеличивается выход продукта(ов) в обратимой реакции
1) СН4(г) + Н2O(г)  СO(г) + ЗН2(г)
СO(г) + ЗН2(г)
2) С(тв) + 2Н2(г)  СН4(г)
СН4(г)
3) С(тв) + Н2O(г)  СO(г) + Н2(г)
СO(г) + Н2(г)
4) С(тв) + СO2(г)  2СO(г)
2СO(г)
21. Задание 21 № 1885. Реакция между карбонатом натрия и хлоридом бария протекает, потому что в результате
1) выделяется газ и образуется вода
2) выделяется газ
3) образуется раствор слабого электролита
4) образуется осадок
22. Задание 22 № 3643. Из ионов металлов в организме человека больше всего
1) 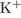
2) 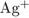
3) 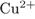
4) 
23. Задание 23 № 515. Верны ли следующие суждения о производстве аммиака?
А. В промышленности аммиак получают синтезом из простых веществ.
Б. Реакция синтеза аммиака экзотермическая.
1) верно только А
2) верно только Б
3) верны оба суждения
4) оба суждения неверны
24. Задание 24 № 1170. Объём (н.у.) формальдегида, который потребуется для получения 1 л формалина (р = 1,11 г/мл) с массовой долей формальдегида 40%, равен (с точностью до десятых)
1) 0,4 л
2) 33,6 л
3) 134,4 л
4) 331,5 л
25. Задание 25 № 3604. При окислении аммиака хлором образовались хлорид аммония и 20 л азота. Чему равен объём израсходованного хлора? Объёмы газов измерены при одинаковых условиях.
1) 20 л
2) 40 л
3) 60 л
4) 80 л
26. Задание 26 № 225. Какой объём (н.у.) оксида серы (IV) вступил в реакцию с избытком раствора гидроксида натрия, если при этом образовался сульфит натрия количеством вещества 0,2 моль? (Запишите число с точностью до сотых.)
1) 4,21
2) 4,48
3) 3,44
4) 2,21
27. Задание 27 № 904. Установите соответствие между названием соединения и его функциональной группой,
НАЗВАНИЕ СОЕДИНЕНИЯ
A) диметиламин
Б) бутановая кислота
B) метаналь
Г) глицерин
ФУНКЦИОНАЛЬНАЯ ГРУППА
1) карбоксильная группа
2) нитрогруппа
3) аминогруппа
4) альдегидная группа
5) гидроксильная группа
28. Задание 28 № 4454. Установите соответствие между схемой окислительно-восстановительной реакции и изменением степени окисления окислителя.
| СХЕМА ОВР | ИЗМЕНЕНИЕ СТЕПЕНИ ОКИСЛЕНИЯ ОКИСЛИТЕЛЯ | |
А) 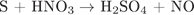 Б)
Б) 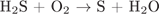 В)
В) 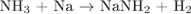 Г)
Г) 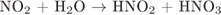
| 1)  2)
2) 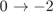 3)
3) 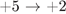 4)
4) 
|
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
| А | Б | В | Г |
29. Задание 29 № 1807. Установите соответствие между формулой вещества и продуктом, который выделяется на инертном аноде при электролизе водного раствора вещества.
ФОРМУЛА ВЕЩЕСТВА
A) HCl
Б) K2S
B) NaOH
Г) AgNO3
ПРОДУКТ НА АНОДЕ
1) водород
2) кислород
3) галоген
4) металл
5) азот
6) сера
| A | Б | В | Г |
30. Задание 30 № 864. Установите соответствие между химической формулой соли и реакцией среды её водного раствора.
| ФОРМУЛА СОЛИ | РЕАКЦИЯ СРЕДЫ | |
A) 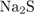 Б)
Б)  B)
B)  Г)
Г) 
| 1) кислая 2) нейтральная 3) щелочная |
31. Задание 31 № 306. Установите соответствие между схемами превращений и формулами веществ, необходимых для их последовательного осуществления.
СХЕМЫ ПРЕВРАЩЕНИЙ
A) 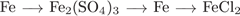
Б) 
В) 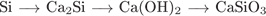
Г) 
ФОРМУЛЫ ВЕЩЕСТВ
1) 
2) 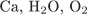
3) 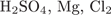
4) 
5) 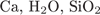
32. Задание 32 № 3978. Установите соответствие между веществами и реактивом, с помощью которого их можно отличить.
| Вещества | Реактивы | |
| А) карбонат натрия и сульфат натрия Б) хлорид алюминия и хлорид калия В) сульфат аммония и сульфат лития Г) карбонат натрия и силикат натрия | 1) гидроксид меди (II) 2) натрий 3) соляная кислота 4) бромная вода 5) гидроксид калия |
33. Задание 33 № 3612. При присоединении бромоводорода к пропену
1) разрывается  -связь
-связь
2) образуется дибромалкан
3) преимущественно образуется 2-бромпропан
4) образуются 1-бромпропан и 2-бромпропан в равных соотношениях
5) происходит промежуточное образование катиона 
6) происходит промежуточное образование радикала 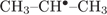
34. Задание 34 № 308. Для предельных одноатомных спиртов характерна(-о):
1) sр3-гибридизация атомов углерода
2) наличие водородных связей между молекулами
3) взаимодействие с гидроксидом меди (II)
4) реакция гидрирования
5) реакция полимеризации
6) реакция этерификации
35. Задание 35 № 1169. Диметиламин
1) твердое вещество
2) плохо растворим в воде
3) взаимодействует с серной кислотой
4) проявляет кислотные свойства
5) взаимодействует с раствором хлороводорода
6) горит на воздухе
36. Задание 36 № 398. Используя метод электронного баланса, составьте уравнение реакции
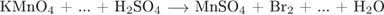
Определите окислитель и восстановитель.
37. Задание 37 № 4423. При сливании водных растворов сульфита калия и перманганата калия выпал осадок. Осадок при нагревании обработали концентрированной соляной кислотой, при этом наблюдалось образование газа. Полученный газ прореагировал с алюминием. Продукт данной реакции растворили в избытке раствора гидроксида натрия. Напишите уравнения четырёх описанных реакций.
38. Задание 38 № 1217. Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
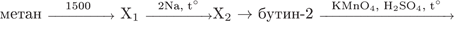

39. Задание 39 № 1218. В 15%-ном растворе серной кислоты массой 300 г растворили карбид алюминия. Выделившийся при этом метан занял объём 2,24 л (н.у.). Рассчитайте массовую долю серной кислоты в полученном растворе.
40. Задание 40 № 4517. Некоторое органическое соединение массой 5,8 г, взаимодействуя с гидроксидом меди(II), при нагревании образовало 14,4 г осадка оксида меди(I). Указанное органическое соединение вступает в реакции присоединения гидросульфита натрия и этанола. На основании этих данных:
1) установите простейшую молекулярную формулу соединения,
2) составьте его структурную формулу,
3) приведите уравнение реакции его взаимодействия с гидроксидом меди(II).
Вар 6
1. Задание 1 № 3683. Электронную конфигурацию, отличную от инертного газа, имеет ион
1) 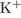
2) 
3) 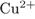
4) 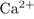
2. Задание 2 № 1007. Верны ли следующие суждения о соединениях хрома?
А Высшая степень окисления хрома равна +4.
Б. Высший оксид хрома относится к основным оксидам.
1) верно только А
2) верно только Б
3) верны оба суждения
4) оба суждения неверны
3. Задание 3 № 3343. В каком веществе реализуются ковалентные полярные связи?
1) 
2) 
3) 
4) 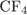
4. Задание 4 № 536. Степень окисления азота в карбонате аммония равна
1) -3
2) -2
3) +2
4) +3
5. Задание 5 № 4604. Молекулярную кристаллическую решётку имеет
1) 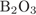
2) 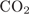
3) 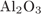
4) 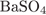
6. Задание 6 № 753. Химические соединения: 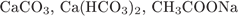 относятся к
относятся к
1) кислотам
2) основаниям
3) солям
4) оксидам
7. Задание 7 № 1987. С щелочами не взаимодействует
1) алюминий
2) бром
3) сера
4) магний
8. Задание 8 № 3775. Какие соединения не могут реагировать между собой?
1) 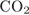 и
и 
2) 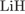 и
и 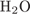
3)  и
и 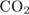
4)  и
и 
9. Задание 9 № 3066. С гидроксидом натрия и соляной кислотой взаимодействует каждый из двух гидроксидов:
1) 
2) 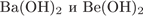
3) 
4) 
10. Задание 10 № 585. Хлорид железа (II) можно получить в результате реакции между веществами
1) 
2) 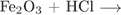
3) 
4) 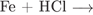
11. Задание 11 № 801. В схеме превращений
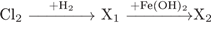
веществом «Х2» является
1) оксид железа (II)
2) соляная кислота
3) хлорид железа (III)
4) хлорид железа (II)
12. Задание 12 № 4358. Гомологом метилпропанола-1 является
1) бутанол-1
2) пропанон
3) пропандиол-1,2
4) 2-метилбутанол-1
13. Задание 13 № 3696. С хлороводородом может реагировать
1) пентан
2) толуол
3) циклогексан
4) циклопропан
14. Задание 14 № 1748. Два изомерных между собой продукта образуются при дегидратации
1) этанола
2) бутанола-2
3) пропанола-2
4) фенола
15. Задание 15 № 2427. Верны ли следующие суждения о свойствах указанных кислородсодержащих органических соединений?
А. Этилацетат подвергается гидролизу.
Б. Муравьиная кислота реагирует с аммиачным раствором оксида серебра(I).
1) верно только А
2) верно только Б
3) верны оба суждения
4) оба суждения неверны
16. Задание 16 № 634. Этиленгликоль можно получить гидролизом
1) 1,2-дихлорэтана
2) ацетилена
3) жира
4) этилата калия
17. Задание 17 № 3357. В схеме превращений
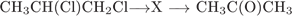
веществом Х является
1) 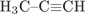
2) 
3) 
4) 
18. Задание 18 № 1195. Взаимодействие кислорода с литием относится к реакциям
1) соединения, эндотермическим
2) соединения, экзотермическим
3) замещения, эндотермическим
4) обмена, экзотермическим
19. Задание 19 № 336. Для увеличения скорости химической реакции

необходимо
1) увеличить концентрацию ионов железа
2) размельчить железо
3) уменьшить температуру
4) уменьшить концентрацию кислоты
20. Задание 20 № 1455. В системе

смещение химического равновесия вправо произойдет при
1) повышении давления
2) повышении температуры
3) увеличении концентрации оксида серы (VI)
4) добавлении катализатора
21. Задание 21 № 1798. В воде растворили 0,5 моль газа и в полученном растворе обнаружили 1 моль ионов. Формула газа
1) NH3
2) SO2
3) НСl
4) CH2O
22. Задание 22 № 428. Реактивом на многоатомные спирты является
1) 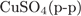
2) 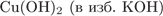
3) 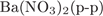
4) 
23. Задание 23 № 2782. Только электролизом расплава соли в промышленности можно получить
1) натрий
2) серебро
3) цинк
4) хром
24. Задание 24 № 826. При растворении в 270 г воды сульфата калия был получен раствор с массовой долей 10%. Масса растворённого 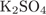 равна
равна
1) 17,4 г
2) 27 г
3) 30 г
4) 174 г
25. Задание 25 № 3475. Какой объём кислорода теоретически необходим для полного окисления 200 л сернистого газа до оксида серы(VI)? Объёмы газов измерены при одинаковых условиях.
1) 100 л
2) 200 л
3) 300 л
4) 400 л
26. Задание 26 № 4729. При взаимодействии 32 г карбида кальция с избытком воды образуется ацетилен, объём (н.у.) которого равен
1) 112 л
2) 11,2 л
3) 224 л
4) 22,4 л
27. Задание 27 № 2569. Установите соответствие между названием вещества и его принадлежностью к определённому (-ой) классу (группе) органических соединений.
| НАЗВАНИЕ ВЕЩЕСТВА | КЛАСС (ГРУППА) ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ |
| A) фенилаланин | 1) амины |
| Б) этиленгликоль | 2) углеводороды |
| B) бутин | 3) спирты |
| Г) циклобутан | 4) альдегиды |
| 5) аминокислоты | |
28. Задание 28 № 948. Установите соответствие между схемой реакции и формулой недостающего в ней вещества.
СХЕМА РЕАКЦИИ
А) 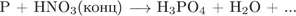
Б) 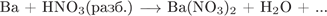
В) 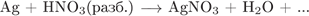
Г) 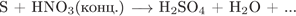
ФОРМУЛА ВЕЩЕСТВА
1) 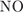
2) 
3) 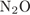
4) 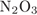
5) 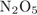
29. Задание 29 № 1164. Установите соответствие между формулой соли и продуктом(-ами), образующимся(-ися) на катоде при электролизе её водного раствора.
ФОРМУЛА СОЛИ
A) 
Б) 
B) 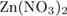
Г) 
ПРОДУКТ НА КАТОДЕ
1) 
2) 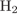
3) 
4) 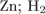
5) 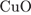
6) 
30. Задание 30 № 2572. Установите соответствие между формулой соли и средой её водного раствора.
| ФОРМУЛА СОЛИ | СРЕДА РАСТВОРА |
A) 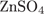
| 1) кислая |
Б) 
| 2) нейтральная |
B) 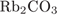
| 3) щелочная |
Г) 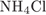
| |
31. Задание 31 № 4255. Установите соответствие между простым веществом и реагентами, с каждым из которых оно может взаимодействовать.
| ПРОСТОЕ ВЕЩЕСТВО | РЕАГЕНТЫ | |
А)  Б)
Б) 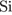 В)
В) 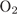 Г)
Г) 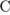
| 1) 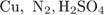 2)
2)  3)
3)  4)
4)  5)
5) 
|
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
| А | Б | В | Г |
32. Задание 32 № 3927. Установите соответствие между парой неорганических веществ и реактивом, с помощью которого можно различить эти вещества.
| ВЕЩЕСТВА | РЕАГЕНТ | |
А) 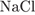 и и  Б)
Б) 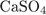 и и 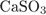 В)
В) 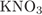 и и 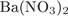 Г)
Г)  и и 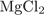
| 1) 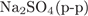 2)
2)  3)
3) 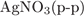 4)
4) 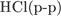 5)
5) 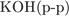
|
Date: 2015-09-22; view: 654; Нарушение авторских прав