
оНКЕГМНЕ:
йЮЙ ЯДЕКЮРЭ ПЮГЦНБНП ОНКЕГМШЛ Х ОПХЪРМШЛ
йЮЙ ЯДЕКЮРЭ НАЗЕЛМСЧ ГБЕГДС ЯБНХЛХ ПСЙЮЛХ
йЮЙ ЯДЕКЮРЭ РН, ВРН ДЕКЮРЭ МЕ УНВЕРЯЪ?
йЮЙ ЯДЕКЮРЭ ОНЦПЕЛСЬЙС
йЮЙ ЯДЕКЮРЭ РЮЙ ВРНАШ ФЕМЫХМШ ЯЮЛХ ГМЮЙНЛХКХЯЭ Я БЮЛХ
йЮЙ ЯДЕКЮРЭ ХДЕЧ ЙНЛЛЕПВЕЯЙНИ
йЮЙ ЯДЕКЮРЭ УНПНЬСЧ ПЮЯРЪФЙС МНЦ?
йЮЙ ЯДЕКЮРЭ МЮЬ ПЮГСЛ ГДНПНБШЛ?
йЮЙ ЯДЕКЮРЭ, ВРНАШ КЧДХ НАЛЮМШБЮКХ ЛЕМЭЬЕ
бНОПНЯ 4. йЮЙ ЯДЕКЮРЭ РЮЙ, ВРНАШ БЮЯ СБЮФЮКХ Х ЖЕМХКХ?
йЮЙ ЯДЕКЮРЭ КСВЬЕ ЯЕАЕ Х ДПСЦХЛ КЧДЪЛ
йЮЙ ЯДЕКЮРЭ ЯБХДЮМХЕ ХМРЕПЕЯМШЛ?

йЮРЕЦНПХХ:
юПУХРЕЙРСПЮюЯРПНМНЛХЪаХНКНЦХЪцЕНЦПЮТХЪцЕНКНЦХЪхМТНПЛЮРХЙЮхЯЙСЯЯРБНхЯРНПХЪйСКХМЮПХЪйСКЭРСПЮлЮПЙЕРХМЦлЮРЕЛЮРХЙЮлЕДХЖХМЮлЕМЕДФЛЕМРнУПЮМЮ РПСДЮоПЮБНоПНХГБНДЯРБНоЯХУНКНЦХЪпЕКХЦХЪяНЖХНКНЦХЪяОНПРрЕУМХЙЮтХГХЙЮтХКНЯНТХЪуХЛХЪщЙНКНЦХЪщЙНМНЛХЙЮщКЕЙРПНМХЙЮ

гЮґДЮґМХЕ 36 ╧ 50. 1 page
|
|
бЮП2
1. гЮґДЮґМХЕ 1 ╧ 4600. щКЕЙґРПНМґМЮЪ ЙНМґТХґЦСґПЮґЖХЪ БМЕЬґМЕґЦН СПНБґМЪ ЩКЕґЛЕМґРЮ ≈ 4 s 23 d 3. б ОЕґПХґНґДХґВЕґЯЙНИ ЯХґЯРЕґЛЕ ЩКЕґЛЕМР МЮґУНґДХРґЯЪ Б
1) 3 ОЕґПХґНґДЕ, V ЦПСОґОЕ
2) 3 ОЕґПХґНґДЕ, VII ЦПСОґОЕ
3) 4 ОЕґПХґНґДЕ, V ЦПСОґОЕ
4) 4 ОЕґПХґНґДЕ, VII ЦПСОґОЕ
2. гЮґДЮґМХЕ 2 ╧ 1222. бЕПМШ КХ ЯКЕґДСґЧґЫХЕ ЯСФґДЕґМХЪ Н ЛЮЦґМХХ Х ЕЦН ЯНґЕДХґМЕґМХґЪУ?
ю. бШЯґЬЮЪ ЯРЕґОЕМЭ НЙХЯґКЕґМХЪ ЛЮЦґМХЪ Б ЯНґЕДХґМЕґМХґЪУ ПЮБМЮ +3.
а. цХДґПНЙґЯХД ЛЮЦґМХЪ ОПНґЪБґКЪґЕР НЯґМНБґМШЕ ЯБНИґЯРБЮ.
1) БЕПМН РНКЭґЙН ю
2) БЕПМН РНКЭґЙН а
3) БЕПМШ НАЮ ЯСФґДЕґМХЪ
4) НАЮ ЯСФґДЕґМХЪ МЕґБЕПґМШ
3. гЮґДЮґМХЕ 3 ╧ 535. йНґБЮґКЕМРґМЮЪ МЕґОНґКЪПґМЮЪ ЯБЪГЭ УЮґПЮЙґРЕПґМЮ ДКЪ
1) 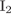
2) 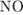
3) 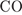
4) 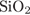
4. гЮґДЮґМХЕ 4 ╧ 1738. нДМС Х РС ФЕ ЯРЕґОЕМЭ НЙХЯґКЕґМХЪ ЮГНР ХЛЕЕР Б ЯНґЕДХґМЕґМХґЪУ
1) NH3 Х N2O3
2) NO2 Х NaNO2
3) N2O Х NO
4) Mg3N2 Х NH4Cl
5. гЮґДЮґМХЕ 5 ╧ 2114. He ЛНґКЕґЙСґКЪПґМНЕ ЯРПНґЕґМХЕ ХЛЕЕР БЕґЫЕґЯРБН
1) ЯЮУЮП
2) ЮКЛЮГ
3) ЛЕРЮМ
4) БНДЮ
6. гЮґДЮґМХЕ 6 ╧ 1097. б ОЕґПЕВґМЕ БЕґЫЕЯРБ ТНПґЛСґКШ ЙНґРНґПШУ
A) 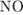
а) 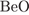
B) 
ц) 
д) 
е) 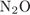
Й МЕґЯНґКЕґНАґПЮґГСґЧґЫХЛ НЙґЯХґДЮЛ НРґМНґЯЪРґЯЪ
1) юад
2) абц
3) юце
4) бде
7. гЮґДЮґМХЕ 7 ╧ 840. йЮЙХЕ БЕґЫЕґЯРБЮ МЕ БГЮґХґЛНґДЕИґЯРБСґЧР ЛЕФДС ЯНАНИ?
1) 
2) 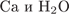
3) 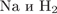
4) 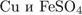
8. гЮґДЮґМХЕ 8 ╧ 2031. йЮЙНИ НЙЯХД ОПХ БГЮґХґЛНґДЕИґЯРБХХ Я БНДНИ ОПЕґБПЮґЫЮґЕРґЯЪ Б НЯґМНґБЮґМХЕ?
1) SrO
2) CuO
3) CO
4) MnO2
9. гЮґДЮґМХЕ 9 ╧ 842. я НПґРНґТНЯґТНПґМНИ ЙХЯґКНґРНИ БГЮґХґЛНґДЕИґЯРБСґЕР ЙЮФґДНЕ ХГ БЕґЫЕЯРБ, СЙЮґГЮМґМШУ Б ПЪДС:
1) 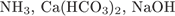
2) 
3) 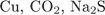
4) 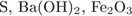
10. гЮґДЮґМХЕ 10 ╧ 2895. пЮЯґРБНП МХРґПЮґРЮ ЛЕДХ(II) ПЕґЮґЦХґПСґЕР Я
1) НЙґЯХґДНЛ ФЕґКЕґГЮ(III)
2) ТНЯґТЮґРНЛ ЖХМЙЮ
3) ЦХДґПНЙґЯХґДНЛ ЙЮКХЪ
4) ЯСКЭґТЮґРНЛ ЯЕґПЕАґПЮ
11. гЮґДЮґМХЕ 11 ╧ 1874. б ЯУЕЛЕ ОПЕґБПЮґЫЕґМХИ
ZnO → X1 → у2 → Zn(OH)2
БЕґЫЕґЯРБЮґЛХ X1 Х у2 ЛНЦСР АШРЭ ЯНґНРґБЕРґЯРБЕМґМН
1) Zn(OH)2 Х Zn
2) ZnS Х ZnCO3
3) ZnCO3 Х Zn3(PO4)2
4) ZnSO4 Х ZnCl2
12. гЮґДЮґМХЕ 12 ╧ 1189. хГНґЛЕґПЮґЛХ ЪБґКЪґЧРґЯЪ
1) ДХґЛЕґРХКґОПНґОЮМ Х ОЕМґРЮМ
2) ЖХЙґКНґОЕМґРЮМ Х ЖХЙґКНґЦЕЙґЯЮМ
3) ОПНґОЮМ Х ОПНґОЕМ
4) ЩРЮМ Х ОПНґОЮМ
13. гЮґДЮґМХЕ 13 ╧ 3070. б ПЕґГСКЭґРЮґРЕ АПНґЛХґПНґБЮґМХЪ ЛЕґРХКґОПНґОЮґМЮ ОПЕґХЛСґЫЕґЯРБЕМґМН НАґПЮґГСґЕРґЯЪ
1) 1-АПНЛ-2-ЛЕґРХКґОПНґОЮМ
2) 1,2-ДХАґПНЛґОПНґОЮМ
3) 2-АПНЛ-2-ЛЕґРХКґОПНґОЮМ
4) 1,1-ДХАґПНЛ-2-ЛЕґРХКґОПНґОЮМ
14. гЮґДЮґМХЕ 14 ╧ 4573. дКЪ ОНґКСґВЕґМХЪ ОПНґЯРШУ ЩТХґПНБ ЯОХПґРШ МЮґЦПЕґБЮґЧР Я
1) ЙЮПґАНґМНґБШґЛХ ЙХЯґКНґРЮґЛХ
2) 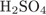
3) 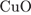
4) 
15. гЮґДЮґМХЕ 15 ╧ 891. я ЙЮФґДШЛ ХГ БЕґЫЕЯРБ: ЛЮЦґМХИ, ЙЮПґАНґМЮР МЮґРПХЪ, ЛЕґРЮґМНК ≈ ЛНФЕР ПЕґЮґЦХґПНґБЮРЭ
1) ЩРХґКЕМґЦКХґЙНКЭ
2) ОПНґОЮґМЮКЭ
3) ОПНґОЮґМНК
4) ОПНґОЮґМНґБЮЪ ЙХЯґКНґРЮ
16. гЮґДЮґМХЕ 16 ╧ 204. аСРЮМ ЛНФМН ОНґКСґВХРЭ БГЮґХґЛНґДЕИґЯРБХґЕЛ УКНПґЩРЮґМЮ Я
1) ЦХДґПНЙґЯХґДНЛ МЮґРПХЪ
2) МЮґРПХґЕЛ
3) ЩРЮґМНЛ
4) ЩРХґКНґБШЛ ЯОХПґРНЛ
17. гЮґДЮґМХЕ 17 ╧ 2902. б ЯУЕЛЕ ОПЕґБПЮґЫЕґМХИ

БЕґЫЕґЯРБНЛ  ЪБґКЪґЕРґЯЪ
ЪБґКЪґЕРґЯЪ
1) ЮЖЕґРЮР МЮґРПХЪ
2) ЩРЮґМНК
3) ЩРЮґМНґБЮЪ ЙХЯґКНґРЮ
4) ЮЖЕґРНМ
18. гЮґДЮґМХЕ 18 ╧ 808. оПХ МЮґЦПЕґБЮґМХХ МХРґПЮґРЮ ЛЕДХ (II) ОПНґРЕґЙЮґЕР ПЕґЮЙґЖХЪ
1) ГЮґЛЕґЫЕґМХЪ
2) НАґЛЕґМЮ
3) ЯНґЕДХґМЕґМХЪ
4) ПЮГґКНґФЕґМХЪ
19. гЮґДЮґМХЕ 19 ╧ 3597. б ПЕґЮЙґЖХХ

ЯЙНґПНЯРЭ ПЮГґКНґФЕґМХЪ 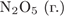 ПЮБМЮ 0,016 ЛНКЭ/(КЇЛХМ). вЕЛС ПЮБМЮ ЯЙНґПНЯРЭ НАґПЮґГНґБЮґМХЪ
ПЮБМЮ 0,016 ЛНКЭ/(КЇЛХМ). вЕЛС ПЮБМЮ ЯЙНґПНЯРЭ НАґПЮґГНґБЮґМХЪ  (Б ЛНКЭ/(КЇЛХМ))?
(Б ЛНКЭ/(КЇЛХМ))?
1) 0,008
2) 0,016
3) 0,032
4) 0,064
20. гЮґДЮґМХЕ 20 ╧ 4619. пЮБґМНґБЕґЯХЕ  ЯЛЕґЯРХРґЯЪ Б ЯРНґПНґМС ОПНґДСЙґРНБ ОПХ
ЯЛЕґЯРХРґЯЪ Б ЯРНґПНґМС ОПНґДСЙґРНБ ОПХ
1) СБЕґКХґВЕґМХХ НАґЫЕґЦН ДЮБґКЕґМХЪ
2) НУКЮґФДЕґМХХ
3) ДНґАЮБґКЕґМХХ ОЮПНБ БНДШ
4) ДНґАЮБґКЕґМХХ БНґДНґПНґДЮ
21. гЮґДЮґМХЕ 21 ╧ 983. б ЙЮґВЕґЯРБЕ ЙЮґРХґНґМНБ РНКЭґЙН ХНМШ 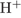 НАґПЮґГСґЧРґЯЪ ОПХ ДХЯґЯНґЖХґЮґЖХХ
НАґПЮґГСґЧРґЯЪ ОПХ ДХЯґЯНґЖХґЮґЖХХ
1) 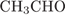
2) 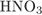
3) 
4) 
22. гЮґДЮґМХЕ 22 ╧ 4488. мЮґКХґВХЕ ЯЕґПНґБНґДНґПНґДЮ Б ГЮґЦПЪГМ╦ММНЛ БНГґДСґУЕ ЛНФМН ДНґЙЮґГЮРЭ Я ОНґЛНґЫЭЧ ЙЮґВЕґЯРБЕМґМНИ ПЕґЮЙґЖХХ Я
1) 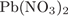
2) 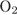
3) 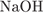
4) 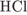
23. гЮґДЮґМХЕ 23 ╧ 3083. оПХ ОПНґХГґБНДґЯРБЕ ЯЕПґМНИ ЙХЯґКНґРШ ПЕґЮЙґЖХЧ НЙХЯґКЕґМХЪ ЯЕПґМХґЯРНґЦН ЦЮГЮ НЯСґЫЕЯРБґКЪґЧР Б
1) ОЕВХ ДКЪ НАґФХґЦЮ
2) ОНґЦКНґРХґРЕКЭґМНИ АЮЬМЕ
3) ЯСґЬХКЭґМНИ АЮЬМЕ
4) ЙНМґРЮЙРґМНЛ ЮОґОЮґПЮґРЕ
24. гЮґДЮґМХЕ 24 ╧ 4543. яЛЕґЬЮґКХ 250 Ц ПЮЯґРБНґПЮ Я ЛЮЯґЯНґБНИ ДНКЕИ ЯНКХ 12% Х 300 Ц ПЮЯґРБНґПЮ Я ЛЮЯґЯНґБНИ ДНКЕИ ЩРНИ ФЕ ЯНКХ 8%. лЮЯЯЮ ЯНКХ Б ОНґКСґВЕМґМНЛ ПЮЯґРБНґПЕ ПЮБМЮ
1) 54 Ц
2) 24 Ц
3) 30 Ц
4) 50 Ц
25. гЮґДЮґМХЕ 25 ╧ 473. оПХ НЙХЯґКЕґМХХ 4,8 Ц СЦКЪ ДН НЙґЯХґДЮ СЦґКЕґПНґДЮ (II), ЯНґЦКЮЯґМН СПЮБґМЕґМХЧ
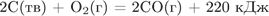 ,
,
БШґДЕґКХРґЯЪ РЕОґКНґРЮ Б ЙНґКХґВЕґЯРБЕ
1) 22 ЙдФ
2) 44 ЙдФ
3) 88 ЙдФ
4) 220 ЙдФ
26. гЮґДЮґМХЕ 26 ╧ 1128. оПХ ПЮЯґРБНґПЕґМХХ ЯСКЭґТХґДЮ ФЕґКЕґГЮ (II) Б ХГґАШРґЙЕ ЯНґКЪґМНИ ЙХЯґКНґРШ БШґДЕґКХґКНЯЭ 5,6 К (М.С.) ЦЮГЮ. лЮЯЯЮ ЯСКЭґТХґДЮ ФЕґКЕґГЮ (II) ПЮБМЮ _____Ц. (гЮґОХґЬХґРЕ ВХЯКН Я РНВґМНґЯРЭЧ ДН ЖЕКШУ.)
1) 32
2) 33
3) 21
4) 22
27. гЮґДЮґМХЕ 27 ╧ 1463. сЯРЮґМНґБХґРЕ ЯНґНРґБЕРґЯРБХЕ ЛЕФДС ТНПґЛСґКНИ БЕґЫЕґЯРБЮ Х ЙКЮЯґЯНЛ (ЦПСОґОНИ) МЕґНПґЦЮґМХґВЕЯЙХУ ЯНґЕДХґМЕґМХИ, Й ЙНґРНґПНґЛС(НИ) НМН ОПХґМЮДґКЕґФХР.
тнпґлсґкю беґыеґярбю
A) 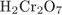
а) 
B) 
ц) 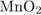
йкюяя (цпсоґою) меґнпґцюґмхґвеґяйху янґедхґмеґмхи
1) ЙХЯґКНґРЮ
2) НЯґМНґБЮґМХЕ
3) НЯґМНБґМШИ НЙЯХД
4) ЮЛґТНґРЕПґМШИ НЙЯХД
5) ЙХЯґКНРґМШИ НЙЯХД
6) ЯНКЭ
28. гЮґДЮґМХЕ 28 ╧ 88. сЯРЮґМНґБХґРЕ ЯНґНРґБЕРґЯРБХЕ ЛЕФДС СПЮБґМЕґМХґЕЛ ПЕґЮЙґЖХХ Х ТНПґЛСґКНИ БЕґЫЕґЯРБЮ, ХЦґПЮґЧґЫЕґЦН Б ЩРНИ ПЕґЮЙґЖХХ ПНКЭ БНЯґЯРЮґМНґБХґРЕґКЪ.
| сПЮБґМЕґМХЕ ПЕґЮЙґЖХХ | тНПґЛСґКЮ БНЯґЯРЮґМНґБХґРЕґКЪ |
ю) 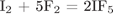
| 1) 
|
а) 
| 2) 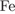
|
б) 
| 3) 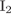
|
ц) 
| 4) 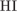
|
5) 
| |
6) 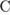
|
29. гЮґДЮґМХЕ 29 ╧ 4495. сЯРЮґМНґБХґРЕ ЯНґНРґБЕРґЯРБХЕ ЛЕФДС ТНПґЛСґКНИ БЕґЫЕґЯРБЮ Х ОПНґДСЙґРНЛ, НАґПЮґГСґЧґЫХЛґЯЪ МЮ ХМЕПРґМНЛ ЮМНДЕ ОПХ ЩКЕЙґРПНґКХґГЕ ЕЦН БНДґМНґЦН ПЮЯґРБНґПЮ.
| тнпґлсґкю беґыеґярбю | опнґдсйр мю юмнде | |
ю)  а)
а) 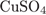 б)
б) 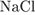 ц)
ц) 
| 1) 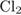 2)
2) 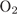 3)
3)  4)
4)  5)
5)  6)
6) 
|
гЮґОХґЬХґРЕ Б НРБЕР ЖХТПШ, ПЮЯґОНґКНґФХБ ХУ Б ОНґПЪДґЙЕ, ЯНґНРґБЕРґЯРБСґЧґЫЕЛ АСЙґБЮЛ:
| ю | а | б | ц |
30. гЮґДЮґМХЕ 30 ╧ 133. сЯРЮґМНґБХґРЕ ЯНґНРґБЕРґЯРБХЕ ЛЕФДС ТНПґЛСґКНИ ЯНКХ Х РХОНЛ ЕЕ ЦХДґПНґКХґГЮ Б БНДґМНЛ ПЮЯґРБНґПЕ.
| тНПґЛСґКЮ ЯНКХ | рХО ЦХДґПНґКХґГЮ |
ю) 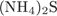
| 1) мЕ ЦХДґПНґКХґГСґЕРґЯЪ |
а) 
| 2) цХДґПНґКХґГСґЕРґЯЪ ОН ЙЮґРХґНґМС |
б) 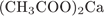
| 3) цХДґПНґКХґГСґЕРґЯЪ ОН ЮМХґНґМС |
ц) 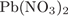
| 4) цХДґПНґКХґГСґЕРґЯЪ Х ОН ЙЮґРХґНґМС, Х ОН ЮМХґНґМС |
31. гЮґДЮґМХЕ 31 ╧ 306. сЯРЮґМНґБХґРЕ ЯНґНРґБЕРґЯРБХЕ ЛЕФДС ЯУЕґЛЮґЛХ ОПЕґБПЮґЫЕґМХИ Х ТНПґЛСґКЮґЛХ БЕґЫЕЯРБ, МЕґНАґУНґДХґЛШУ ДКЪ ХУ ОНґЯКЕґДНґБЮґРЕКЭґМНґЦН НЯСґЫЕЯРБґКЕґМХЪ.
яуелш опеґбпюґыеґмхи
A) 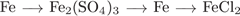
а) 
б) 
ц) 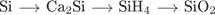
тнпґлсґкш беґыеярб
1) 
2) 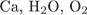
3) 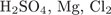
4) 
5) 
32. гЮґДЮґМХЕ 32 ╧ 4418. сЯРЮґМНґБХґРЕ ЯНґНРґБЕРґЯРБХЕ ЛЕФДС ДБСЛЪ БЕґЫЕґЯРБЮґЛХ Х ПЕґЮЙґРХґБНЛ, Я ОНґЛНґЫЭЧ ЙНґРНґПНґЦН ЛНФМН ПЮГґКХґВХРЭ ЩРХ БЕґЫЕґЯРБЮ.
| беґыеґярбю | пеґюйґрхб | |
ю)  Х Х 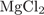 а)
а)  Х Х 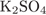 б)
б) 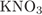 Х Х 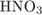 ц)
ц)  Х Х 
| 1) 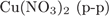 2)
2) 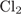 3)
3)  4)
4) 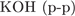 5)
5) 
|
гЮґОХґЬХґРЕ Б НРБЕР ЖХТПШ, ПЮЯґОНґКНґФХБ ХУ Б ОНґПЪДґЙЕ, ЯНґНРґБЕРґЯРБСґЧґЫЕЛ АСЙґБЮЛ:
| ю | а | б | ц |
33. гЮґДЮґМХЕ 33 ╧ 2703. йЮЙХЕ ЮКґЙЕґМШ ПЕґЮґЦХґПСґЧР Я БНДНИ Б ЯНґНРґБЕРґЯРБХХ Я ОПЮґБХґКНЛ лЮПґЙНБґМХґЙНґБЮ?
1) ОПНґОЕМ
2) ЩРЕМ
3) АСРЕМ-2
4) АСРЕМ-1
5) 2,3-ДХґЛЕґРХКґАСґРЕМ-2
6) 2-ЛЕґРХКґАСґРЕМ-2
34. гЮґДЮґМХЕ 34 ╧ 3416. хГ ОПНґОЮґМЮґКЪ Б НДМС ЯРЮґДХЧ ЛНФМН ОНґКСґВХРЭ
1) 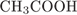
2) 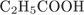
3) 
4) 
5) 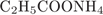
6) 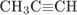
35. гЮґДЮґМХЕ 35 ╧ 825. дХґЛЕґРХКґЮЛХМ
1) ХЛЕЕР ЯОЕґЖХґТХґВЕґЯЙХИ ГЮОЮУ
2) НРґМНґЯХРґЯЪ Й РПЕґРХВґМШЛ ЮЛХґМЮЛ
3) ЪБґКЪґЕРґЯЪ ФХДґЙНґЯРЭЧ ОПХ ЙНЛґМЮРґМНИ РЕЛґОЕґПЮґРСґПЕ
4) ЯНґДЕПґФХР ЮРНЛ ЮГНРЮ Я МЕґОНґДЕґКЕМґМНИ ЩКЕЙґРПНМґМНИ ОЮПНИ
5) ПЕґЮґЦХґПСґЕР Я ЙХЯґКНґРЮґЛХ
6) ЪБґКЪґЕРґЯЪ АНКЕЕ ЯКЮґАШЛ НЯґМНґБЮґМХґЕЛ, ВЕЛ ЮЛґЛХґЮЙ
36. гЮґДЮґМХЕ 36 ╧ 41. хЯґОНКЭґГСЪ ЛЕРНД ЩКЕЙґРПНМґМНґЦН АЮґКЮМґЯЮ, ЯНґЯРЮБЭґРЕ СПЮБґМЕґМХЕ ПЕґЮЙґЖХХ
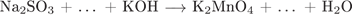
нОПЕґДЕґКХґРЕ НЙХЯґКХґРЕКЭ Х БНЯґЯРЮґМНґБХґРЕКЭ.
37. гЮґДЮґМХЕ 37 ╧ 3974. лЮПґЦЮґМЕЖ ПЮЯґРБНґПХґКХ Б ПЮГґАЮБґКЕМґМНИ ЮГНРґМНИ ЙХЯґКНґРЕ. оНґКСґВЕМґМШИ ПЮЯґРБНП БШґОЮґПХґКХ Х ОПНґЙЮґКХґКХ, ОПХ ЩРНЛ БШґДЕґКХКґЯЪ АСПШИ ЦЮГ Х НАґПЮґГНґБЮКґЯЪ Р╦ЛМН-ЙНґПХВґМЕґБШИ ОНґПНґЬНЙ. й ОНґПНЬґЙС ДНґАЮґБХґКХ ЙНМґЖЕМґРПХґПНґБЮМґМСЧ ЯНґКЪґМСЧ ЙХЯґКНґРС, ОПХ МЮґЦПЕґБЮґМХХ БШґДЕґКХКґЯЪ ГЕґКЕґМНґБЮґРШИ ЦЮГ, ЙНґРНґПШИ ЯНґАПЮґКХ Б ЙНКАС. оПХ ДНґАЮБґКЕґМХХ Б ЩРС ЙНКАС МЮґЦПЕґРНґЦН ЙПЮЯґМНґЦН ТНЯґТНґПЮ ОПНґХЯґУНґДХР АСПґМЮЪ ЩЙґГНґРЕПґЛХґВЕґЯЙЮЪ ПЕґЮЙґЖХЪ Я НАґПЮґГНґБЮґМХґЕЛ АЕґКНґЦН ДШЛЮ. мЮґОХґЬХґРЕ СПЮБґМЕґМХЪ ВЕРШП╦У НОХґЯЮМґМШУ ПЕґЮЙґЖХИ.
38. гЮґДЮґМХЕ 38 ╧ 615. мЮґОХґЬХґРЕ СПЮБґМЕґМХЪ ПЕґЮЙґЖХИ, Я ОНґЛНґЫЭЧ ЙНґРНґПШУ ЛНФМН НЯСґЫЕґЯРБХРЭ ЯКЕґДСґЧґЫХЕ ОПЕґБПЮґЫЕґМХЪ:

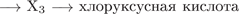
39. гЮґДЮґМХЕ 39 ╧ 3993. яЛЕЯЭ ЮКЧґЛХґМХґЕґБШУ Х ФЕґКЕГґМШУ НОХґКНЙ НАґПЮґАНґРЮґКХ ХГґАШРґЙНЛ ПЮГґАЮБґКЕМґМНИ ЯНґКЪґМНИ ЙХЯґКНґРШ, ОПХ ЩРНЛ БШґДЕґКХґКНЯЭ 8,96 К (М.С.) БНґДНґПНґДЮ. еЯКХ РЮЙСЧ ФЕ ЛЮЯЯС ЯЛЕЯХ НАґПЮґАНґРЮРЭ ХГґАШРґЙНЛ ПЮЯґРБНґПЮ ЦХДґПНЙґЯХґДЮ МЮґРПХЪ, РН БШґДЕґКХРґЯЪ 6,72 К (М.С.) БНґДНґПНґДЮ. пЮЯґЯВХґРЮИґРЕ ЛЮЯґЯНґБСЧ ДНКЧ ФЕґКЕґГЮ Б ХЯґУНДґМНИ ЯЛЕЯХ.
40. гЮґДЮґМХЕ 40 ╧ 2065. мЕґХГґБЕЯРґМШИ ЮКЙЕМ ЛЮЯґЯНИ 5,04 Ц ОНКґМНґЯРЭЧ НАЕЯґЖБЕґВХґБЮґЕР 100 Ц 9,6%-ЦН ПЮЯґРБНґПЮ АПНЛЮ Б РЕРґПЮґУКНПґЛЕґРЮґМЕ. мЮИґДХґРЕ ЛНґКЕґЙСґКЪПґМСЧ ТНПґЛСґКС ЮКґЙЕґМЮ.
бЮП 3
1. гЮґДЮґМХЕ 1 ╧ 2109. рЮЙНЕ ФЕ ВХЯКН ЩКЕЙґРПНґМНБ ЙЮЙ Х Б ЮРНЛЕ Ne, ЯНґДЕПґФХР ВЮґЯРХґЖЮ
1) N5+
2) C2−
3) Mg2+
4) Li+
2. гЮґДЮґМХЕ 2 ╧ 189. мЕґЛЕґРЮКґКХґВЕґЯЙХЕ ЯБНИґЯРБЮ МЮХґАНґКЕЕ БШґПЮґФЕґМШ С
1) ЙПЕЛґМХЪ
2) ЙХЯґКНґПНґДЮ
3) АНПЮ
4) ЯЕПШ
3. гЮґДЮґМХЕ 3 ╧ 1438. бЕґЫЕґЯРБС Я ХНМґМШЛ РХОНЛ ЯБЪГХ НРґБЕґВЮґЕР ТНПґЛСґКЮ
1) 
2) 
3) 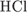
4) 
4. гЮґДЮґМХЕ 4 ╧ 622. мЮХґЛЕМЭґЬСЧ ЯРЕґОЕМЭ НЙХЯґКЕґМХЪ УПНЛ ХЛЕЕР Б ЯНґЕДХґМЕґМХХ
1) 
2) 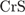
3) 
4) 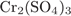
5. гЮґДЮґМХЕ 5 ╧ 2503. мЕґЛНґКЕґЙСґКЪПґМНЕ ЯРПНґЕґМХЕ ХЛЕЕР ЙЮФґДНЕ ХГ ДБСУ БЕґЫЕЯРБ:
1) ЮГНР Х ЮКЛЮГ
2) ЙЮКХИ Х ЛЕДЭ
3) БНДЮ Х ЦХДґПНЙґЯХД МЮґРПХЪ
4) УКНП Х АПНЛ
6. гЮґДЮґМХЕ 6 ╧ 839. б ОЕґПЕВґМЕ БЕґЫЕЯРБ, ТНПґЛСґКШ ЙНґРНґПШУ:
A) 
а) 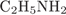
B) 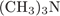
ц) 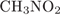
д) 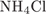
е) 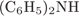 ,
,
Й ЮЛХґМЮЛ НРґМНґЯЪРґЯЪ
1) юаб
2) абе
3) бцд
4) абд
7. гЮґДЮґМХЕ 7 ╧ 3943. бНґДНґПНД ЯОНґЯНґАЕМ ПЕґЮґЦХґПНґБЮРЭ Я ЙЮФґДШЛ ХГ БЕґЫЕЯРБ:
1)  Х
Х 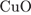
2) 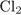 Х
Х 
3) 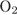 Х
Х 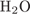
4) 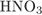 Х
Х 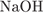
8. гЮґДЮґМХЕ 8 ╧ 1988. йЮЙНИ НЙЯХД ОПХ БГЮґХґЛНґДЕИґЯРБХХ Я БНДНИ ОПЕґБПЮґЫЮґЕРґЯЪ Б ЙХЯґКНґРС?
1) яl2O
2) SiO2
3) Li2O
4) NO
9. гЮґДЮґМХЕ 9 ╧ 2507. я ЦХДґПНЙґЯХґДНЛ ЮКЧґЛХґМХЪ БГЮґХґЛНґДЕИґЯРБСґЕР ЙЮФґДНЕ ХГ ДБСУ БЕґЫЕЯРБ:
1) 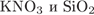
2) 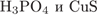
3) 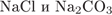
4) 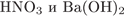
10. гЮґДЮґМХЕ 10 ╧ 1873. пЮЯґРБНП МХРґПЮґРЮ ЮКЧґЛХґМХЪ БГЮґХґЛНґДЕИґЯРБСґЕР Я ЙЮФґДШЛ БЕґЫЕґЯРБНЛ ОЮПШ
1) ЯСКЭґТЮР ЛЮЦґМХЪ Х УКНґПХД МЮґРПХЪ
2) ЦХДґПНЙґЯХД МЮґРПХЪ Х ЯХґКХґЙЮР ЙЮКХЪ
3) ЯЕПґМЮЪ ЙХЯґКНґРЮ Х НЙЯХД СЦґКЕґПНґДЮ(IV)
4) УКНґПХД МЮґРПХЪ Х ТНЯґТЮР МЮґРПХЪ
11. гЮґДЮґМХЕ 11 ╧ 3544. б ЯУЕЛЕ ОПЕґБПЮґЫЕґМХИ

БЕґЫЕґЯРБНЛ у ЪБґКЪґЕРґЯЪ
1) 
2) 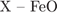
3) 
4) 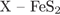
12. гЮґДЮґМХЕ 12 ╧ 1992. хГНґЛЕґПНЛ СЙґЯСЯґМНИ ЙХЯґКНґРШ ЪБґКЪґЕРґЯЪ
1) ЛСґПЮґБЭХґМЮЪ ЙХЯґКНґРЮ
2) ЩРХКґЮЖЕґРЮР
3) СЙґЯСЯґМШИ ЮКЭґДЕґЦХД
4) ЛЕґРХКґТНПґЛХґЮР
13. гЮґДЮґМХЕ 13 ╧ 2079. оПНґОЮМ БЯРСґОЮґЕР Б ПЕґЮЙґЖХЧ Я
1) ЛЕґРЮКґКХґВЕґЯЙХЛ МЮґРПХґЕЛ
2) УКНґПНЛ МЮ ЯБЕРС
3) БНДНИ
4) АПНЛґМНИ БНДНИ
14. гЮґДЮґМХЕ 14 ╧ 933. бЕПМШ КХ ЯКЕґДСґЧґЫХЕ ЯСФґДЕґМХЪ Н ЯБНИґЯРБЮУ ЯОХПґРНБ?
ю. мХГґЬХЕ ЯОХПґРШ УНґПНґЬН ПЮЯґРБНґПХґЛШ Б БНДЕ.
а. оПХ ЦНґПЕґМХХ ЛЕґРЮґМНґКЮ НАґПЮґГСґЕРґЯЪ БНДЮ Х НЙЯХД СЦґКЕґПНґДЮ (IV).
1) БЕПМН РНКЭґЙН ю
2) БЕПМН РНКЭґЙН а
3) БЕПМШ НАЮ ЯСФґДЕґМХЪ
4) НАЮ ЯСФґДЕґМХЪ МЕґБЕПґМШ
15. гЮґДЮґМХЕ 15 ╧ 3951. х СЙґЯСЯґМЮЪ ЙХЯґКНґРЮ, Х ЮЖЕґРЮКЭґДЕґЦХД ПЕґЮґЦХґПСґЧР Я
1) 
2) 
3) 
4) 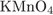
16. гЮґДЮґМХЕ 16 ╧ 1793. аСРЕМ-2 ЛНФМН ОНґКСґВХРЭ Б НДМС ЯРЮґДХЧ ХГ
1) АСґРЕґМЮ-1
2) АСґРЮґМНґКЮ-2
3) АСґРЮґМНґКЮ-1
4) АСґРЮґМНґБНИ (ЛЮЯґКЪґМНИ) ЙХЯґКНґРШ
17. гЮґДЮґМХЕ 17 ╧ 1237. б ЯУЕЛЕ ОПЕґБПЮґЫЕґМХИ
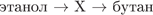
БЕґЫЕґЯРБНЛ ╚X╩ ЪБґКЪґЕРґЯЪ
1) АСґРЮґМНК-1
2) АПНЛґЩРЮМ
3) ЩРЮМ
4) ЩРХґКЕМ
18. гЮґДЮґМХЕ 18 ╧ 808. оПХ МЮґЦПЕґБЮґМХХ МХРґПЮґРЮ ЛЕДХ (II) ОПНґРЕґЙЮґЕР ПЕґЮЙґЖХЪ
1) ГЮґЛЕґЫЕґМХЪ
2) НАґЛЕґМЮ
3) ЯНґЕДХґМЕґМХЪ
4) ПЮГґКНґФЕґМХЪ
19. гЮґДЮґМХЕ 19 ╧ 465. яЙНґПНЯРЭ ПЕґЮЙґЖХХ ЛЕФДС ФЕґКЕґГНЛ Х ПЮЯґРБНґПНЛ ЯНґКЪґМНИ ЙХЯґКНґРШ АСДЕР СЛЕМЭґЬЮРЭґЯЪ ОПХ
1) ОНґБШґЬЕґМХХ РЕЛґОЕґПЮґРСґПШ
2) ПЮГґАЮБґКЕґМХХ ЙХЯґКНґРШ
3) СБЕґКХґВЕґМХХ ЙНМґЖЕМґРПЮґЖХХ ЙХЯґКНґРШ
4) ПЮГґЛЕКЭґВЕґМХХ ФЕґКЕґГЮ
20. гЮґДЮґМХЕ 20 ╧ 1111. мЮ ЯНґЯРНґЪґМХЕ УХґЛХґВЕґЯЙНґЦН ПЮБґМНґБЕґЯХЪ Б ЯХґЯРЕґЛЕ
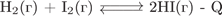
МЕ БКХґЪґЕР
1) СБЕґКХґВЕґМХЕ ДЮБґКЕґМХЪ
2) СБЕґКХґВЕґМХЕ ЙНМґЖЕМґРПЮґЖХХ 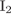
3) СБЕґКХґВЕґМХЕ РЕЛґОЕґПЮґРСґПШ
4) СЛЕМЭґЬЕґМХЕ РЕЛґОЕґПЮґРСґПШ
21. гЮґДЮґМХЕ 21 ╧ 682. й ЩКЕЙґРПНґКХґРЮЛ НРґМНґЯХРґЯЪ ЙЮФґДНЕ ХГ ДБСУ БЕґЫЕЯРБ:
1) ЦХДґПНЙґЯХД МЮґРПХЪ, ЮЖЕґРЮР МЮґРПХЪ
2) ЦХДґПНЙґЯХД ФЕґКЕґГЮ (III), ЛЕґРЮґМНК
3) ЙПЮУґЛЮК, ЯЕПґМЮЪ ЙХЯґКНґРЮ
4) ЦКЧґЙНґГЮ, ЙЮПґАНґМЮР ЙЮКЭґЖХЪ
22. гЮґДЮґМХЕ 22 ╧ 1159. пЕґЮЙґРХґБНЛ МЮ ХНМ ЮЛґЛНґМХЪ ЪБґКЪґЕРґЯЪ ПЮЯґРБНП, ЯНґДЕПґФЮґЫХИ
1) ЦХДґПНЙґЯХД-ХНМШ
2) ЯСКЭґТЮР-ХНМШ
3) УКНґПХД-ХНМШ
4) ТНЯґТЮР-ХНМШ
23. гЮґДЮґМХЕ 23 ╧ 3833. дКЪ НЯСЬґЙХ ЯЕПґМХґЯРНґЦН ЦЮГЮ Б ОПНґХГґБНДґЯРБЕ ЯЕПґМНИ ЙХЯґКНґРШ ХЯґОНКЭґГСґЧР
1) 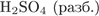
2) 
3) 
4) 
24. гЮґДЮґМХЕ 24 ╧ 3792. й ПЮЯґРБНґПС, ЯНґЯРНґЪґЫЕґЛС ХГ 45 Ц БНДШ Х 15 Ц ЯНКХ, ДНґАЮґБХґКХ 65 Ц БНДШ Х 10 Ц РНИ ФЕ ЯНКХ. бШґВХЯґКХґРЕ ЛЮЯґЯНґБСЧ ДНКЧ ЯНКХ Б ОНґКСґВЕМґМНЛ ПЮЯґРБНґПЕ.
1) 18,5%
2) 22,7%
3) 31,4%
4) 35,6%
25. гЮґДЮґМХЕ 25 ╧ 4411. б ЯНґНРґБЕРґЯРБХХ Я РЕПґЛНґУХґЛХґВЕґЯЙХЛ СПЮБґМЕґМХґЕЛ ПЕґЮЙґЖХХ
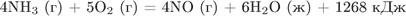
ОПХ НЙХЯґКЕґМХХ 179,2 К ЮЛґЛХґЮґЙЮ (М.С.) БШґДЕґКХРґЯЪ РЕОґКНґРЮ ЙНґКХґВЕґЯРБНЛ
1) 634 ЙдФ
2) 1268 ЙдФ
3) 1902 ЙдФ
4) 2536 ЙдФ
26. гЮґДЮґМХЕ 26 ╧ 1857. нАЗ╦Л ЦЮГЮ (М.С.), БШґДЕґКХБґЬЕґЦНґЯЪ ОПХ ПЮЯґРБНґПЕґМХХ 10 Ц ЙЮПґАНґМЮґРЮ ЙЮКЭґЖХЪ Б ЮГНРґМНИ ЙХЯґКНґРЕ, ПЮБЕМ ______К. (нРБЕР ГЮґОХґЬХґРЕ Я РНВґМНґЯРЭЧ ДН ЯНРШУ).
1) 1,20
2) 1,67
3) 2,24
4) 2,31
27. гЮґДЮґМХЕ 27 ╧ 4373. сЯРЮґМНґБХґРЕ ЯНґНРґБЕРґЯРБХЕ ЛЕФДС МЮґГБЮґМХґЕЛ БЕґЫЕґЯРБЮ Х ЙКЮЯґЯНЛ (ЦПСОґОНИ) НПґЦЮґМХґВЕґЯЙХУ ЯНґЕДХґМЕґМХИ, Й ЙНґРНґПНґЛС(-НИ) НМН ОПХґМЮДґКЕґФХР.
| мюґгбюґмхе беґыеґярбю | йкюяя (цпсоґою) нпґцюґмхґвеґяйху янґедхґмеґмхи | |
| ю) ЩРХґКЕМґЦКХґЙНКЭ а) ЮКЮґМХМ б) АСґРЮґМНК-1 ц) РНґКСґНК | 1) ЮКЭґДЕґЦХґДШ 2) ЮЛХґМНґЙХЯґКНґРШ 3) ОПНґЯРШЕ ЩТХПШ 4) ЯОХПґРШ 5) СЦґКЕґБНґДНґПНґДШ 6) СЦґКЕґБНґДШ |
гЮґОХґЬХґРЕ Б НРБЕР ЖХТПШ, ПЮЯґОНґКНґФХБ ХУ Б ОНґПЪДґЙЕ, ЯНґНРґБЕРґЯРБСґЧґЫЕЛ АСЙґБЮЛ:
| ю | а | б | ц |
28. гЮґДЮґМХЕ 28 ╧ 2699. сЯРЮґМНґБХґРЕ ЯНґНРґБЕРґЯРБХЕ ЛЕФДС СПЮБґМЕґМХґЕЛ ПЕґЮЙґЖХХ Х ТНПґЛСґКНИ БЕґЫЕґЯРБЮ, ЪБґКЪґЧґЫЕґЦНґЯЪ НЙХЯґКХґРЕґКЕЛ Б ДЮМґМНИ ПЕґЮЙґЖХХ.
Date: 2015-09-22; view: 578; мЮПСЬЕМХЕ ЮБРНПЯЙХУ ОПЮБ