
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Работа №1: Кислотные свойства салициловой кислоты. Основные свойства анилина
|
|
1.Кислотные свойства салициловой кислоты.
В пробирку поместите 20 мг салициловой кислоты, 2 мл воды и встряхните. К образовавшейся суспензии по каплям добавьте 10%-ный раствор NaOH до образования прозрачного раствора. Полученный раствор разделите поровну на 2 пробирки. К первой пробирке добавьте несколько капель 10%-ной соляной кислоты, а ко второй несколько капель раствора уксусной кислоты. Отметьте появление или отсутствие помутнения.
2. Основные свойства анилина.
В пробирку поместите 2 капли воды и 1 каплю анилина и встряхните. К образовавшейся эмульсии по каплям добавьте 10%-ный раствор соляной кислоты до образования прозрачного раствора. К этому раствору добавьте несколько капель 10%-ной NaOH. Наблюдается помутнение.
По окончании работы составьте отчет и сдайте на проверку преподавателю.
Содержание отчета:
I. Название работы.
II. Ход работы.
III. Ответы на следующие вопросы:
1. Почему при добавлении раствора NaOH к суспензии салициловой кислоты исчезает помутнение? Напишите схему реакции салициловой кислоты с NaOH. Сколько молей NaOH могут реагировать с 1 молем салициловой кислоты?
2. Какая из кислот более сильная: уксусная или салициловая?
3. Почему при добавлении соляной кислоты к эмульсии анилина исчезает помутнение? Напишите схему реакции анилина с соляной кислотой.
ЛИТЕРАТУРА:
Руководство к лабораторным занятиям по органической химии под ред. Н.А.Тюкавкиной – ДРОФА, М., 2003, с. 217-218.
Работа №2: Отношение алканов к окислению
В каждую из двух пробирок поместите по 2 капли любого алкана (гептан, октан, петролейный эфир, вазелиновое масло) и добавьте по 8 капель воды и 2 капли 2%-го раствора перманганата калия. Затем во вторую пробирку внесите 2 капли концентрированной серной кислоты. Обе пробирки энергично несколько раз встряхните и отметьте, какую окраску имеет эмульсия в каждой пробирке. Затем содержимое каждой пробирки нагрейте на спиртовке в течение 1-2 мин. и снова отметьте окраску.
По окончании работы составьте отчет и сдайте на проверку преподавателю.
Содержание отчета:
I. Название работы.
II. Ход работы.
III. Ответы на следующие вопросы:
1. Происходит ли изменение окраски перманганата в пробирке?
2. Сравните окисляющее действие перманганата в нейтральной и кислой средах, а также при комнатной температуре и при нагревании.
3. На основании полученных наблюдений сделайте вывод об отношении алканов к окислению.
ЛИТЕРАТУРА:
Руководство к лабораторным занятиям по органической химии под ред. Н.А.Тюкавкиной – ДРОФА, М., 2003, с. 222.
Работа №3: Получение и химические свойства этилена
1. Получение этилена
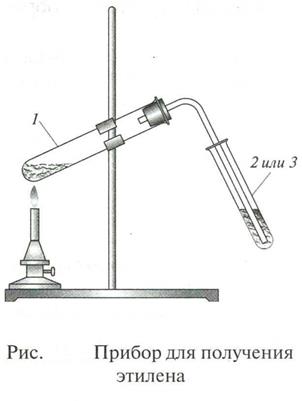
В пробирку 1 (см. рисунок) помещают 10 капель концентрированной серной кислоты, 6-8 капель этанола и несколько крупинок окиси алюминия. Пробирку закрывают пробкой с газоотводной трубкой и закрепляют в лапке штатива, как показано на рисунке. Пробирку медленно нагревают на спиртовке, из газоотводной трубки начинает выделяться этилен.
2.Бромирование этилена
В пробирку 2 помещают 6 капель бромной воды, и опускают в нее газоотводную трубку так, чтобы конец трубки был опущен в жидкость (см. рисунок). Выделяющийся в пробирке 1 этилен пропускается через бромную воду, и она обесцвечивается.
3.Окисление этилена
В пробирку 3 помещают 1 каплю 2%-ного раствора перманганата калия, 5 капель воды и 1 каплю (не более!) серной кислоты. В пробирку опускают газоотводную трубку, и пропускают через полученный раствор этилен. Обратите внимание на изменение окраски раствора в пробирке 3.
По окончании работы составьте отчет и сдайте на проверку преподавателю.
Содержание отчета:
I. Название работы.
II. Ход работы.
III. Ответы на следующие вопросы:
1. О чем свидетельствует наблюдаемое обесцвечение бромной воды и раствора перманганата?
2. Напишите схемы реакций получения этилена, бромирования и мягкого окисления (гидроксилирования) этилена
ЛИТЕРАТУРА:
Руководство к лабораторным занятиям по органической химии под ред. Н.А.Тюкавкиной – ДРОФА, М., 2003, с. 217-218.
Работа №4: Нитрование бензола
В коническую термостойкую колбу на 50 мл помещают ротор магнитной мешалки 6 лопаточек нитрата натрия и 4 мл концентрированной серной кислоты и 1 мл бензола.
Перед началом опыта включают нагрев магнитной мешалки. Реакционная колба ставится на магнитную мешалку, устанавливается минимальное перемешивание, и реакционная масса выдерживается в течение 10 мин. при температуре 70-75о (без кипения). В процессе реакции бензол растворяется.
По окончании выдержки магнитная мешалка выключается и реакционная масса осторожно (конц. серная кислота!) выливается в другую коническую колбу на 100 мл, в которую предварительно наливают 30 мл воды. Колбу охлаждают водой и перемешивают содержимое стеклянной палочкой: выпадает кристаллический осадок. Его отфильтровывают под вакуумом, промывают водой на фильтре и сушат в сушильном шкафу при 60о.
Определяют температуру плавления продукта, по которой его идентифицируют.
Справочные данные:
орто -динитробензол – т.пл. 1170;
мета -динитробензол – т.пл. 900;
пара -динитробензол – т.пл. 1740.
По окончании работы составьте отчет и сдайте на проверку преподавателю.
Содержание отчета:
I. Название работы.
II. Ход работы.
III. Ответы на следующие вопросы:
1. Напишите схему получения нитробензола из бензола, приведите механизм реакции.
2. Какой продукт образовался в проведенной вами реакции? Приведите её схему и объясните, почему получился именно этот изомер.
ЛИТЕРАТУРА:
Руководство к лабораторным занятиям по органической химии под ред. Н.А.Тюкавкиной – ДРОФА, М., 2003, с. 235-236.
Date: 2015-09-22; view: 1656; Нарушение авторских прав