
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Строение и состав гидросферы
|
|
Большая часть поверхности нашей планеты, около 71%, покрыта мировым океаном, составляющим 97% всех поверхностных вод Земли и около половины всех вод литосферы. Мировой океан – это непрерывная водная оболочка Земли, окружающая все материки и острова и обладающая общностью солевого состава. Следует дифференцировать понятия «Мировой океан» и «океан». Последний представляет часть Мирового океана, расположенную среди материков, обладающую самостоятельной системой циркуляции вод и специфическими особенностями гидрологического режима. В свою очередь, море – это часть океана, впадающая в сушу или отделённая от других его частей островами, в которой вследствие её обособленности формируются специфические черты гидрологического режима.
В химическом составе морской воды можно выделить пять компонентов: 1) главные ионы – эти одиннадцать компонентов составляют 99,98% по весу от всех растворённых в океанской воде солей; 2) биогенные элементы (С, Н, N, P, Si, Fe, Mn), из которых состоят организмы; 3) растворимые в морской воде газы: О2, N2, СО2, углеводороды и инертные газы; 4) микроэлементы; 5) органические вещества.
Подавляющую часть морской соли составляют хлориды, а не карбонаты. В этом состоит главное отличие морской воды от речной, в которой преобладают углекислые соли. Постоянство солевого состава морской воды – главнейшая закономерность в химии океана. Концентрация растворённых солей определяет величину солёности океана. За величину солёности (S) принят вес сухого остатка, содержащегося в 1 кг морской воды, когда карбонаты переведены в оксиды, бромиды и йодиды замещены эквивалентным количеством хлора и органические вещества сожжены при 480°С. Единица измерения – г/кг, или промилле (о/оо). Однако большей частью солёность вычисляется по хлорности, электропроводности или показателю преломления. Между солёностью и хлорностью имеется соотношение 5%=1,81 Сl.
Важной химической характеристикой океанических вод является водородный показатель (рН). Выделение СО2 в результате дыхания и разложения вызывает понижение рН в природных водах, потому что при соединении СО2 с водой образуется слабая (слабодиссоциирующая) кислота Н2СО3:
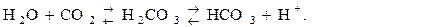 С другой стороны, поглощение СО2 в процессе фотосинтеза приводит к уменьшению количества Н2СО3 и Н+, т.е. к росту рН. Отсюда можно утверждать, что рН в океанах регулируется равновесием СО2 и карбоната кальция:
С другой стороны, поглощение СО2 в процессе фотосинтеза приводит к уменьшению количества Н2СО3 и Н+, т.е. к росту рН. Отсюда можно утверждать, что рН в океанах регулируется равновесием СО2 и карбоната кальция:
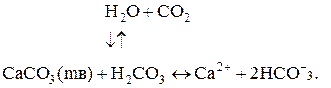
Видно, что повышение количества СО2 увеличивает содержание Н2СО3, уменьшая содержание карбоната кальция, а уменьшение содержания СО2 приводит к осаждению карбоната кальция. Вода, содержащая Н2СО3 и НСО-3 обладает буферными свойствами, поэтому достаточно большие изменения концентрации Н+ могут не приводить к сильному изменению рН.
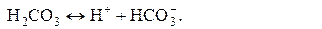 |
Рассмотрим реакцию
 |
Константа равновесия этой реакции будет
откуда
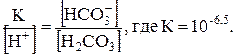
Если количества НСО-3 и Н2СО3 равны (например 10-2 моль/л), то Н+=10-6,5 моль/л и рН=6,5. Суммарное количество НСО-3 и Н2СО3 составляет 2×10-2моль/л. При добавлении в раствор кислоты равновесие сдвигается влево с образованием Н2СО3. Чтобы изменить отношение НСО-3 / Н2СО3, например до 1/3, потребуется добавить кислоты около 5×10-3 моль на литр раствора. Прибавленное количество Н+ почти в 104 раз превышает первоначальное содержание водородных ионов. Новое значение рН можно вычислить:
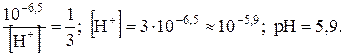 |
Таким образом, рН изменилось незначительно, несмотря на добавление такого количества ионов водорода, которое сильно превосходит первоначальное содержание в растворе. Большая часть добавленных ионов связана в форме Н2СО3, и очень маленькое количество существует как Н+. Конечно, химические свойства морской воды гораздо сложнее рассмотренных выше соотношений. Однако результирующие соотношения между растворимыми молекулами и ионами, атмосферным СО2 и твёрдым карбонатом кальция приводят к формированию буферного раствора с рН=8,0-8,4. При этом не исключено, конечно, что активность органического вещества или другие локальные причины могут образовать на некоторое время более низкие (до 6) и более высокие (до 10) значения рН. Существенной характеристикой, особенно важной для нормального протекания фотосинтеза, является «прозрачность» воды океана. За условную прозрачность морской (и океанической) воды принята глубина моря (океана), на которой белый диск диаметром 30 см становится невидимым.
Мировой океан в последние десятилетия стал объектом глубоких всесторонних исследований. И это не случайно, поскольку ресурсы океана грандиозны, как и он сам. Затрагивая вопрос о ресурсах океана, разделим их на две группы: одна из них биохимического характера, прежде всего необходимо указать на то, что океан является важным источником пищевых ресурсов. В настоящее время промыслы в океане дают 1/16 всех белков и 3-4% жиров животного происхождения. Мировой улов рыбы в последние годы составляет 63 млн. т в год. Наиболее богатые уловы оказываются приуроченными к выходам на поверхность подводных течений, выносящих из-под фотослоя, т.е. с глубины более 200 м, воды, богатые фосфатами, нитратами и другими солями. Замечено, что в местах выхода таких течений, равно как и вдоль кромки тающего полярного льда, бурно развивается планктон – главный корм рыб. Здесь вылов рыбы достигает 180 кг с 1га акватории. В общем улове в настоящее время рыба составляет 90%, моллюски – 5%, ракообразные – 3%, морские растения – 1,5%. В океане обитает свыше 300 000 видов живых организмов, от микроскопических водорослей до самых крупных на планете животных – 160-тонных синих китов. А между тем в океане пока эксплуатируется лишь 0,0001% продуцента. Важно указать, что океан является грандиозным источником минеральных ресурсов. В мировом океане сосредоточено около 5×1016 т минерального сырья. Больше всего в океане хлора, натрия, магния, кальция, калия. В океане относительно много урана, серебра, золота. Приводимая ниже табл. 4 подтверждает сказанное.
Таблица 4
Некоторые из элементов,
определяющих химические ресурсы Мирового океана
| Элемент | Содержание, т | Элемент | Содержание, т |
| Cl Na Mg Ca K | 2,6×1016 1,4×1016 1,8×1015 5,6×1014 5,3×1014 | U Cu Ag Au | 2,0 × 1111 1,5 × 1011 5,0 × 1010 1,1 × 108 |
Полезные ископаемые океана можно классифицировать следующим образом: 1) сырьё в недрах под океаном (нефть, газ, уголь, сера, железная руда); 2) прибрежные рассыпные месторождения (ильменит, монацит, циркон, магнетит, вольфрамий, золото, алмазы, платина); 3) полезные ископаемые морского дна (железомарганцевые конкреции и фосфиты).
Очень большой интерес представляет добыча нефти и газа на океанском шельфе (материковая отмель). По прогнозам, в 2002 г. половина всей нефти будет добываться со дна океана.
Колоссальное значение океана состоит и в том, что он, будучи «лёгкими» планеты, продуцирует своим фитопланктоном почти половину всего кислорода атмосферы. В обменном процессе между атмосферой и океаном, т.е. в «дыхании» океана, участвует 100 млрд. т СО2. При этом жизнь, населяющая океан, ассимилирует в год в среднем 126 млрд. т СО2 против 20 млрд. т, ассимилируемых жизнью суши. Океан, как насос, поглощает своими холодными водами СО2 в полярных широтах и отдаёт её в нагретых экваториальных и тропических зонах. Именно поэтому давление СО2 в области тропиков всегда несколько выше, чем в высоких широтах. Мировой океан как среда жизни представляет интерес прежде всего потому, что именно здесь, по мнению многих учёных, зародилась жизнь, которая в длительном процессе эволюции дала колоссальное многообразие форм. Разнообразие форм жизни на Земле поразительно, хотя оно основано на одном типе химического процесса – фотосинтезе, в результате которого в растениях из неорганических веществ создаётся органическое. Большая часть растительного мира океана – это микроскопические фитопланктоновые организмы (прикреплённые ко дну водные растения занимают очень небольшую часть), которые в основном и являются первичной продукцией моря. Объём ежегодной продукции фитопланктона в мировом океане оценивается величиной 500 млрд. т. На основе первичной продукции развиваются все другие морские организмы - бактерии, зоопланктон, рыбы, морские звери. Для развития фитопланктона кроме энергии солнечного света необходимы неорганические компоненты. В состав организмов входит до 60 химических элементов, однако 90-95% массы организмов состоит из шести элементов, называемых биофильными (жизнелюбивыми), или биогенными. Это- углерод, кислород, водород, азот, фосфор и кремний.
Хотя в общем балансе гидросферы Мировой океан занимает ведущее место, существенное значение для биосферы в целом играет пресная вода. Пресной называют воду, в 1 кг которой содержится не более 1 г солей. Из общего количества воды на Земле на долю пресной приходится не более 3%. Все остальные – это солёные воды Мирового океана, минерализованные подземные и воды соляных озёр. Распределение пресной воды по водным объектам приведено в табл. 5. Из таблицы следует, что подавляющая часть пресной воды на Земле находится в состоянии, труднодоступном для человека, а в пределах всех рек содержится лишь 0,006% всех пресных вод, или немногим больше 1/1000000 части общих запасов воды. В СНГ общий запас пресных поверхностных вод составляет почти 40,5 тыс. км3. Больше всего их в озёрах (более 26 тыс. км3) и в ледниках (11 тыс. км3); в болотах находится около 3 тыс. км3, а в руслах рек – всего 235 км3.
Таблица 5
Распределение пресной воды по объектам
| Водный объект | Содержание, тыс. км3 |
| Ледники, подземные льды (в пересчёте на воду) Подземные воды Влага в почве Пресные озёра Болота Вода в руслах рек Вода в атмосфере Биологические воды (в живых организмах) |
Речные воды представляют собой самый удобный для использования вид природных вод. Реки, словно гигантский водопровод, проходят по всем материкам. Именно водами рек с глубокой древности удовлетворяет человек свои основные хозяйственные нужды (бытовое и промышленное водоснабжение, орошение земель, энергетика, транспорт и т.д.). Это, между прочим, одна из важных причин, обусловливающих особо внимательное отношение к рекам. В СНГ около 3 млн. рек, если включить в это число и водотоки длиной менее 10 км. Суммарная длина всех рек, включая и самые малые (до 10 км), составляет приблизительно 9,6 млн. км, причём на долю рек длиной до 10 км приходится 5,6 млн. км, а на долю больших рек – 229 тыс. км.
Озёра распределены на поверхности Земли крайне неравномерно. Наибольшее скопление крупных озёр отмечается в областях древнего оледенения, в районах тектонических разломов земной коры и в засушливых районах, не имеющих речного стока в океан. Площадь всех озёр (пресных и солёных) составляет 2 млн. км2, а объём воды в них равен 176400 км2, только половина которого приходится на долю крупных пресных озёр (Мичиган, Онтарио, Верхнее). Верхнее озеро является самым крупным пресноводным водоёмом мира с площадью зеркала в 82680 км2. Однако по объёму воды (11600 км3) и максимальной глубине (406 м) оно значительно уступает Байкалу и Танганьике (Африка). В Байкале заключено 23000 км3 пресной воды, почти в 80 раз больше, чем в Азовском море. Байкал – планетарный резерв пресной воды высокого качества. Это удивительное озеро: хотя и занимает по площади зеркала (31,5 тыс. км2) лишь восьмое место в мире, содержит больше воды, чем все пресные озёра земного шара, и является самым глубоким на Земле – его наибольшая глубина 1741 м. За ним стоит Танганьика – наибольшая отметка глубины 1435 м.
Болота – это весьма своеобразные водные объекты, в них нет больших открытых водных пространств; это, в сущности, переувлажнённые участки суши, покрытые специфической влаголюбивой растительностью. Общая площадь болот на земном шаре – приблизительно 3 млн. км2, или 2% суши. Почти 60% болот расположено в СНГ, меньше всего – в Австралии (0,005% площади). На остальных континентах болота занимают в среднем 2% территории, хотя в некоторых районах, например в Финляндии, они охватывают до 40% территории (Финляндия по-фински называется Суоми, т.е. «страна болот»), а в северной половине Западной Сибири даже 50-70%. Суммарный объём болотных вод мира составляет 11470 км3.
Ледники, вносящие существенный вклад в баланс пресных вод, покрывают свыше 16 млн. км2 в Гренландии. Объём воды, заключённый в ледниках всего земного шара, составляет 24 млн. км3, из которых 22 млн. км3 – в Антарктиде. Следует отметить, что ледники выполняют функции конденсации и хранения запасов пресной воды, давая начало многим рекам мира. По одному из принятых определений ледник – это ледяное тело, возникшее выше снеговой границы на земной поверхности из различных атмосферных осадков, преимущественно снежных. За снеговую границу, выше которой возникают ледники, в среднем условно можно принять высоту 4 км над уровнем моря. Общая масса распределённых по поверхности земного шара снега и льда достигает 2×1022 г. От массы всей Земли это составляет всего 0,0004%. Однако такого количества достаточно, чтобы покрыть всю поверхность планеты 53-метровым слоем. Если бы вся эта масса вдруг растаяла, превратившись в воду при температуре 0°С, то уровень мирового океана поднялся бы по сравнению с нынешним примерно на 64 м. Распределение снега и льда на планете приведено в табл. 6. Данные, приведённые в таблице, требуют некоторых уточнений. Прежде всего следует ещё раз подчеркнуть, что происхождение ледников обусловлено выпадающим снегом, постепенно спрессовывающимся под воздействием как ветра, так и, главным образом, последующего наслоения нового снега, который превращается в зернистый лёд (фирн) и далее в обычный лёд. Зоны вечной мерзлоты, расположенные в Сибири, на Аляске и в северных районах Канады, на равнине достигают глубины 65 м, а в гористой местности – 900 м.
Таблица 6
Снег и лёд на Земле
| Формы существова- ния снега и льда | Масса | Площадь | ||
| г | % | км2 | % | |
| Ледники Вечная мерзлота Морские льды Снежный покров Айсберги Лёд в атмосфере | 2,4×1022 4,5×1020 3,5×1019 1,1×1019 7,7×1018 1,7×1018 | 98,95 0,83 0,14 0,04 0,03 0,01 | 1.6×107 2,1×107 2,6×107 7,2×107 6,4×106 5,1×108 | 10,9 (от площади суши) 14,0 (от площади суши) 7,2 (от площади Мирового океана) 14,2 (от площади всей земной поверхности) 1,9 (от площади Мирового океана) 100,0 (от площади всей земной поверхности) |
Айсберги представляют собой громадные ледяные горы, отломившиеся от сползающих в океан материковых ледников, преимущественно из Антарктиды и Гренландии, в результате приливов и отливов, а также штормов. Встречаются айсберги длиной 120 км, шириной 75 км и высотой, доходящей до 450 м, большая часть массы которых находится под водой. Айсберги могут существовать до 3 лет, проплыв 4000км. В тропосфере постоянно присутствуют во взвешенном состоянии частицы снега и льда. Вообще вода в атмосфере находится главным образом в виде водяного пара и
его конденсата (капельки воды и ледяные кристаллы). Почти весь водяной пар (90%) сосредоточен в нижнем слое атмосферы. Атмосферный воздух при данной температуре может содержать только определённое количество водяных паров. Как только это количество достигается, воздух становится насыщенным, водяной пар начинает конденсироваться, превращаясь в туман или облако; чем выше температура воздуха, тем больше водяного пара он может содержать. Собственно, поэтому в тропиках воздух всегда более влажный, чем в Арктике. Обычно количество водяного пара в воздухе, или абсолютную влажность, выражают массой водяного пара в граммах на кубический метр воздуха. Отношение же абсолютной влажности при данной температуре воздуха к абсолютной влажности для состояния насыщения при той же температуре, выраженное в процентах, называется относительной влажностью. Таким образом, относительная влажность показывает, насколько воздух насыщен влагой, сколько процентов остаётся ещё до его полного насыщения. В умеренных широтах абсолютная влажность колеблется от 2-3 г/м3 зимой до 10-12 г/м3 летом, а относительная - 80-90% зимой до 60-70% летом. В жарком климате абсолютная влажность увеличивается, а относительная - уменьшается. В атмосфере содержится единовременно 12900 км3 влаги. Если бы она сконденсировалась и равномерно выпала на поверхность Земли в виде осадков, то покрыла бы её слоем воды 25 мм – это примерно то количество осадков, которое выпадает во время сильного продолжительного ливня в умеренных широтах.
Если говорить о биологической воде, то, как известно, все без исключения живые существа на Земле и растения содержат в своём организме воду – в среднем 80% по весу. Принимая, согласно последним данным, общую массу живого вещества биосферы равной 1400 млрд. т, получим массу биологической воды 1120 млрд. т, или 1120 км3. Этот объём соизмерим с объёмом всех рек Европы, Азии, Африки и Северной Америки. На углерод живого вещества приходится лишь 10%, а 90% падает на водород и кислород, причём на последний только 25%. Без воздуха (кислорода) жизнь возможна (анаэробные организмы), без воды - нет. Подавляющая масса вод биосферы неоднократно проходит через живые организмы в результате обмена веществ (метаболизма). Поэтому все воды биосферы (по крайней мере 99% их) являются биогенными, образовавшимися за счёт либо космогенных вод, поступающих на Землю из окружающего её пространства, либо эндогенных, поступающих из глубин Земли. Вод, образовавшихся за счёт деятельности человека, относительно немного. Они образуются как при «сгорании» любых видов топлива, так и в результате окисления в живом организме и при его разложении.
Воду, синтезированную в организмах человека и животных, называют «ювенильной». Многими учёными высказывалось суждение о том, что кровь человека и животных повторяет химический состав той среды, из которой в далёком прошлом произошла жизнь. Это суждение основано на том, что кровь животных и человека по элементарному составу очень близка составу солей океанической воды (табл. 7), в которой, согласно многим мнениям, и зародилась органическая жизнь.
Таблица 7
Сопоставление элементарного состава
крови человека и вод мирового океана
| Компоненты | Содержание, % от суммы растворённых солей | |
| в крови | в водах мирового океана | |
| Хлор Натрий Кислород Калий Кальций | 49,3 30,0 9,9 1,8 0,8 | 55,0 30,6 5,7 1,1 1,2 |
Процессы растворения в биосфере почти всегда сопровождаются сложными биохимическими реакциями, протекающими с помощью микроорганизмов. Некоторые микроорганизмы развиваются даже в весьма высокоминерализованных растворах хлористого натрия и погибают при их опреснении. Имеются микроорганизмы, способные разрушать такие труднорастворимые соединения, как алюмосиликаты.
Природные процессы растворения, а также процессы выщелачивания, выпадения в осадок, ионного обмена протекают не только и даже не столько в результате чисто физико-химических воздействий, сколько в результате очень сложных биохимических процессов, связанных с микроорганизмами. Морские осадки образуются при активном участии биогенных процессов. Например, почти вся история появления кремния в океане обусловлена этими процессами. Кремний поставляется в морские осадки диатомеями, радиоляриями, губками обычно в виде опала, который впоследствии может переходить в чистый кварц. Некоторые водоросли концентрируют алюминий, другие – известь. Во многих природных водах с помощью одних анаэробных микроорганизмов (нитрифицирующих бактерий) образуются азотная и азотистая кислота, с помощью других (тионовокислых бактерий) окисляются сера, сульфиды, полисульфиды и образуется серная кислота. Известны бактерии, окисляющие сернистый цинк, кадмий и мышьяк, а также пирит, марказит и образующие в воде даже свободную серную кислоту. Многие образования месторождений серы, железа, меди, цинка, свинца, серебра, ванадия, кобальта обязаны своим происхождением биохимическим процессам, протекающим в водной среде.
Заслуживает дополнительного рассмотрения затронутый выше вопрос о воде растений. Здесь важную роль играет процесс физиологического испарения, названный транспирацией. К этому процессу не относится обычное испарение с поверхности листьев, если вода попала на них из атмосферы (дождь, роса, снег). Установлено, что из одного килограмма впитанной корнями из почвы воды только 1 часть (т.е. 1/1000) используется самими растениями на построение ткани, а 99% её уходит на транспирацию. В основе транспорта растворённых в воде питательных веществ из корней в листья лежат процессы осмоса через органические перегородки-мембраны в тканях растений, а также широко распространённое перескакивание водорода с одной молекулы воды на другую, обусловленное структурной упорядоченностью воды на основе водородных связей. Лучшей иллюстрацией грандиозности этого процесса служат эвкалипты – деревья высотой до 152 м с диаметром ствола у основания 8 м. Подъём жидкости на такую высоту требует уникального нагнетательного насоса с затратой очень больших энергий. За счёт ударов тех молекул, которые не пропускаются мембраной, возникает одностороннее давление на неё – осмотическое. У человека и животных оно достигает 8 атм., у рыб – 15, у растений пустыни – 100, у семян – до 400 атм. Факт незамерзания воды в тончайших субкапиллярных тканях растений даже при температуре - 50°С говорит не только о возможности переохлаждения воды в тонких капиллярах живой материи, но и о специфике электрохимических свойств органических растворов, а также обменных процессов между клетками живой ткани. Вследствие идентичности физического строения и химического состава растения количество незамёрзшей воды в живой ткани на 60-70% больше, чем в мёртвой. Большое значение для сохранения жизни растений в условиях отрицательных температур имеют водяной пар и туман, поглощающие инфракрасное излучение, а также конденсация пара до росы, сопровождающаяся выделением значительного количества тепла.
Проницаемость растительных мембран для отдельных ионов значительно изменяется при раздражении растения. Электрические процессы у растений возникают между жидкостью и стенками капиллярных сосудов. При выходе ионов через клеточную мембрану клетке сообщается отрицательный заряд. Особенно активно электрические процессы протекают в клетках корней, так как через них питательные соки поступают вверх к растущим побегам. Многие исключительные особенности воды были использованы живыми организмами для своих целей. Так, большая теплоёмкость воды использована живой клеткой для более устойчивой температуры внутри неё в сравнении с подчас резкими колебаниями её окружения; весьма высокая теплота испарения воды у позвоночных – против перегрева организма с помощью потовыделения. Но самое главное то, что макромолекула белков и нуклеиновых кислот оптимально взаимодействует с окружающими их водными молекулами.
Рассмотренные выше вопросы касались в основном характеристики поверхностных вод, составляющих основную часть гидросферы. Между тем в плане процессов, протекающих в биосфере, существенную роль играет и так называемая подземная гидросфера. Подробное её рассмотрение целесообразно изложить в разделе, относящемся к характеристике литосферы, а здесь ограничимся лишь отдельными сведениями, относящимися к запасам пресной воды.
Из табл. 6 видно, что пресные воды после ледников вносят основной вклад в общий баланс пресной воды на планете. Обширные запасы подземных вод находятся в верхней части земной коры, на разной глубине под почвой. Эти воды местами пропитывают рыхлые или трещиноватые горные породы, образуя водоносные пласты. Большая часть подземных вод в верхних водоносных пластах образуется в результате просачивания через почву и грунт атмосферных осадков. Некоторая часть подземных вод может образоваться в результате соединения выделившихся из магмы кислорода и водорода. Такие воды аналогично синтезированным в живых организмах называют ювенильными, или юношескими, т.е. впервые вступающими в общий влагооборот земного шара. Достоверных сведений об общем объёме их в балансе влаги Земли пока не имеется.
Горные породы по гидрологическим свойствам разделяют на водопроницаемые и водоупорные. Наибольшей водопроницаемостью обладают рыхлые породы – пески, галечники и трещиноватые известняки. Водоупорными, или водонепроницаемыми, являются глины и монолитные скальные породы. Водоносные пласты образуются в водопроницаемых породах, лежащих на водоупорных, задерживающих дальнейшее движение подземных вод вниз.
К естественным запасам подземных вод обычно относят объём свободной – химически не связанной, движущейся главным образом под влиянием силы тяжести – воды, которая содержится в порах и трещинах горных пород, слагающих земную кору. В земной коре до глубины 2000 м находится 23,4 млн. км3 таких вод – солёных и пресных. Пресные воды, как правило, залегают до глубины 150 – 200 м, ниже они переходят в солоноватые воды и рассолы. Имеется предположение, что до глубины 200 м объём пресных подземных вод составляет 10,5 млн. км3 – это примерно в 100 раз больше, чем объём поверхностных пресных вод, содержащихся в озёрах, руслах рек и болотах. Даже самая сухая почва обязательно содержит некоторое количество влаги в виде гигроскопической воды, а также водяного пара. Частицы почвы удерживают на себе отдельные, изолированные молекулы воды, которые иногда сливаются, образуя плёнку толщиной в 1-2 молекулы. Эта гигроскопическая вода поглощается сухой почвой из воздуха, не подчиняется силе тяжести и может быть удалена из почвы только путём нагревания до 100°С. Когда толщина плёнки становится больше, вода называется плёночной. Между частицами почвы, окружёнными слоем плёночной воды, находится воздух. Плёночная вода под действием сил молекулярного притяжения перемещается от толстой плёнки к тонкой.
Мельчайшие капиллярные промежутки между частицами почвы иногда заполнены капиллярной водой, которая под действием капиллярных сил может подниматься вверх от сплошного слоя подземной воды. Вода, заполняющая крупные промежутки в почве, не удерживается капиллярными силами и свободно стекает вниз в виде струек и капелек. Это гравитационная вода. В воздухе, заключённом в порах между частицами почвы, влага содержится в виде водяного пара. Практически почти вся почвенная влага находится в верхнем двухметровом слое почвы и подпочвы. Влажность этого слоя в среднем составляет 10% (по весу), что соответствует слою воды 0,2 м. Принимая общую площадь почвенного покрова на Земле (за вычетом площади ледников, многолетней мерзлоты и пустынь) равной 82 млн. км2, получим, что запасы влаги в почве составляют 16500 км3.
Средний элементарный состав поверхностных вод суши отличается от среднего элементного состава Мирового океана. Если в океане резко преобладают хлор и натрий, то в речных и озёрных водах – гидрокарбонаты кальция и магния. Отмечаются различия и по степени концентрации ионного состава. В Мировом океане концентрация растворённых веществ в среднем в 175 раз превышает таковую в водах рек и озёр. Из этого, конечно, не следует, что не может быть сильноопреснённых морских вод и сильноосолонённых озёрных и даже речных вод. Состав речной и озёрной воды зависит главным образом от типа почвы и горных пород, через которые она проходит, а также от типа источника питания в виде поверхностного стока или грунтовых вод: обычно в грунтовой воде содержание растворённых веществ больше, чем в водах поверхностного стока. Кроме того, определение состава воды рек и озёр зависит от точки отбора проб и изменяется со временем. Проведена огромная работа по оценке среднего химического состава речных вод мира. Основные результаты сведены в табл. 8.
Таблица 8
Средний состав речных вод мира
| Анион | мг/л или г/т | ммоль/л | Катион | мг/л или г/т | ммоль/л |
| НСО-3 SO2-4 Cl- NO-3 Сумма анионов SiO2 | 58,4 11,2 7,8 1,0 78,4 13,1 | 0,958 0,117 0,220 0,017 1,312 0,218 | Са2+ Mg2+ Na2+ K+ Сумма катионов | 15,0 4,1 6,3 2,3 27,7 | 0,375 0,171 0,059 0,059 0,87 |
Растворение диоксида углерода в воде соответствует реакции
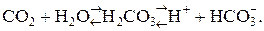
При равновесии устанавливается величина рН 5,6, а содержание НСО-3 не может превышать 100 г/т. В результате взаимодействия воды с минералами повышается величина рН, так как ионы водорода связываются в воде соединениями Н4SiO4 и НСО-3. Водородный показатель речных и озёрных вод регулируется также равновесием с атмосферным диоксидом углерода, за исключением случаев отсутствия контакта с атмосферой для вод глубинных частей некоторых озёр. Cодержание О2 в воде и величина рН контролируются также процессами дыхания организмов и разложения органических веществ. Интервал значения рН большинства рек и озёр – от 6 до 8. Однако встречаются величины как более высокие, так и более низкие.
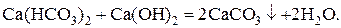 |
Важной характеристикой природных вод является их жёсткость. Как известно, различают жесткость карбонатную (временную) и некарбонатную (постоянную). Первая обусловлена присутствием в воде бикарбонатов Са(НСО3)2 и Mg(HCO3)2, вторая – сульфатов СаSO4 и MgSO4 или их хлоридами. Карбонатная жёсткость устраняется кипячением или прибавлением к воде Са(ОН)2:
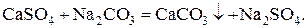 |
Постоянная жёсткость устранима прибавлением к воде соды:
Сумма временной и постоянной жёсткости воды составляет общую жёсткость, выраженную в миллиграмм - эквивалентах ионов Са2+ и Mg2+ на литр воды. Вода с жёсткостью менее 4 мг-экв/л называется мягкой, от 4 до 8 – средней, от 8 до 12 – жёсткой, больше 12 мг-экв/л – очень жёсткой. Жёсткость отдельных естественных вод колеблется в весьма широких пределах. Для открытых водоёмов она часто зависит от времени года и погоды. Наиболее «мягкой» природной водой является атмосферная вода, почти не содержащая растворённых солей.
Date: 2015-09-27; view: 1232; Нарушение авторских прав