
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Вопрос 25
|
|
Электролиты – вещества, растворы (или расплавы) которых проводят электрический ток. Переносчиками электричества являются ионы, образо- вавшиеся в результате диссоциации молекул электролита. Способность деле- ния молекул на ионы у разных веществ неодинакова. Количественно она оценивается степенью диссоциации α, которая определяется отношением числа диссоциированных молекул к числу растворенных молекул.
По величине α электролиты делятся на слабые и сильные. Сильные – это те, которые практически полностью диссоциированы (α велика) и поэто- му хорошо проводят ток, слабые же электролиты диссоциируют незначи- тельно (α мала) и, вследствие этого, проводят ток хуже. Механизм и особен- ности поведения ионов описываются теориями Аррениуса и Дебая-Хюккеля.
Для растворов электролитов различают два основных вида электропро-
водности: удельную κ и эквивалентную λ. Удельной электропроводностью называется электропроводность 1 см3 раствора, заключенного между двумя параллельными электролитами площадью 1 см2 и расположенными на рас- стоянии 1 см друг от друга.
Удельная электропроводность κ – величина, обратная удельному со- противлению ρ:
= ρ1. По закону Ома
R = ρ Sl.
Отсюда
ρ = R Sl, где R – сопротивление проводника, Ом;
(1)
(2)
l S
– длина проводника, см;
– площадь поперечного сечения проводника, см2. Тогда
[ρ]=Ом⋅см2 =Ом⋅см; см
[]= 1 =Ом-1⋅см-1. [ρ]
Эквивалентной электропроводностью называется электропроводность раствора, содержащего 1 г-экв электролита и находящегося между двумя па- раллельными электродами, расположенными на расстоянии 1 см друг от дру- га.
[λ]=Ом-1⋅г-экв-1⋅см2 (Ом-1⋅см2).
Таким образом, κ – проводимость постоянного объема раствора (1 см3) с переменным количеством растворенного электролита, в то же время λ – проводимость различных объемов раствора, содержащих постоянное (1 г- экв) количество электролита.
Между собой они связаны уравнением
где С – концентрация раствора, выраженная в г-экв/л.
(3)
Электропроводность растворов электролитов зависит от концентрации, давления, температуры, природы вещества и растворителя, вязкости, диэлек- трической проницаемости.
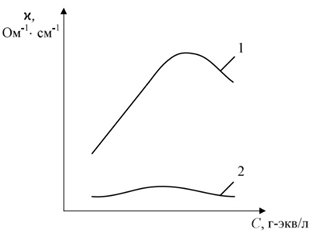
Характер зависимости удельной электропроводности от концентрации раствора выражается кривой с максимумом, приведенной на рисунке 1.
1 – сильный электролит; 2 – слабый электролит.
Рисунок 1 – Зависимость удельной электропроводности от концентрации раствора электролита
В области малых концентраций κ с возрастанием концентрации увели- чивается (так как с увеличением концентрации возрастает число ионов в 1 см3 раствора), достигает максимального значения, а затем уменьшается. В растворах сильных электролитов это уменьшение объясняется замедлением движения ионов из-за релаксационного эффекта и эффекта электрофоретиче- ского торможения, а в растворах слабых электролитов – снижением степени диссоциации.
Рассмотрение влияния концентрации раствора на величину λ удобнее начать с анализа зависимости эквивалентной электропроводности от разбав- ления раствора. Разбавление (разведение) раствора V = 1 C – величина, об-
ратная концентрации С. Как показывают опыты, с увеличением разбавления (уменьшением концентрации) эквивалентная электропроводность возрастает и достигает некоторого предельного значения, как показано на рисунке 2. Это предельное значение λ называется электропроводностью при бесконеч- ном разведении и обозначается λ∞ (илиλ0).
Date: 2015-09-22; view: 632; Нарушение авторских прав