
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Холодильная машина
|
|
Осуществим цикл Карно в обратном направлении. Рабочее тело с начальными параметрами точки а расширяется адиабатно, совершая работу расширения за счет внутренней энергии, и охлаждается от температуры Т1 до температуры T 2 Дальнейшее расширение происходит по изотерме, и рабочее тело отбирает от нижнего источника с температурой T 2 теплоту q2. Далее газ подвергается сжатию сначала по адиабате, и его температура от Т2 повышается до T 1, а затем — по изотерме (T 1=const). При этом рабочее тело отдает верхнему источнику с температурой T 1количество теплоты q 1.
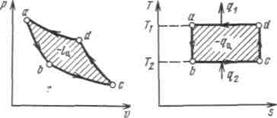
Рисунок 4.4 - Обратный цикл Карно в р,v- и T, s -диаграммах
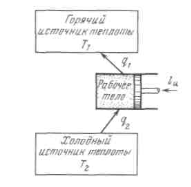
Рисунок 4.5 - Термодинамическая схема холодильной машины
Поскольку в обратном цикле сжатие рабочего тела происходит при более высокой температуре, чем расширение, работа сжатия, совершаемая внешними силами, больше работы расширения на величину площади abcd, ограниченной контуром цикла. Эта работа превращается в теплоту и вместе с теплотой q2 передается верхнему источнику. Таким образом, затратив на осуществление обратного цикла работу l ц, можно перенести теплоту от источника с низкой температурой к источнику с более высокой температурой, при этом нижний источник отдаст количество теплоты q2, а верхний получит количество теплоты ql = q2lц.
Обратный цикл Карно является идеальным циклом холодильных установок и так называемых тепловых насосов.
В холодильной установке рабочими телами служат, как правило, пары легкокипящих жидкостей — фреона, аммиака и т.п. Процесс «перекачки теплоты» от тел, помещенных в холодильную камеру, к окружающей среде происходит за счет затрат электроэнергии.
Эффективность холодильной установки оценивается холодильным коэффициентом, определяемым как отношение количества теплоты, отнятой за цикл от холодильной камеры, к затраченной в цикле работе:
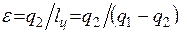 .
.
Для обратного цикла Карно 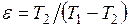 .
.
Заметим, что чем меньше разность температур между холодильной камерой и окружающей средой, тем меньше нужно затратить энергии для передачи теплоты от холодного тела к горячему и тем выше холодильный коэффициент.
Холодильную установку можно использовать в качестве теплового насоса. Если, например, для отопления помещения использовать электронагревательные приборы, то количество теплоты, выделенное в них, будет равно расходу электроэнергии. Если же это количество электроэнергии использовать в холодильной установке, горячим источником, т. е. приемником теплоты, в которой является отапливаемое помещение, а холодным — наружная атмосфера, то количество теплоты, полученное помещением,
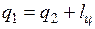
где q2 — количество теплоты, взятое от наружной атмосферы, а 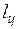 — расход электроэнергии. Понятно, что q1>
— расход электроэнергии. Понятно, что q1> 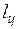 , т. е. отопление с помощью теплового насоса выгоднее простого электрообогрева.
, т. е. отопление с помощью теплового насоса выгоднее простого электрообогрева.
20.Адиабатный процесс.
Процесс, происходящий без теплообмена с окружающей средой, называется адиабатным, т. е. 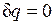 . Для того чтобы осуществить такой процесс, следует либо теплоизолировать газ, т. е. поместить его в адиабатную оболочку, либо провести процесс настолько быстро, чтобы изменение температуры газа, обусловленное его теплообменом с окружающей средой, было пренебрежимо мало по сравнению с изменением температуры, вызванным расширением или сжатием газа. Как правило, это возможно, ибо теплообмен происходит значительно медленнее, чем сжатие или расширение газа.
. Для того чтобы осуществить такой процесс, следует либо теплоизолировать газ, т. е. поместить его в адиабатную оболочку, либо провести процесс настолько быстро, чтобы изменение температуры газа, обусловленное его теплообменом с окружающей средой, было пренебрежимо мало по сравнению с изменением температуры, вызванным расширением или сжатием газа. Как правило, это возможно, ибо теплообмен происходит значительно медленнее, чем сжатие или расширение газа.
Уравнения первого закона термодинамика для адиабатного процесса принимают вид: 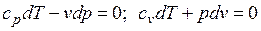 . Поделив первое уравнение на второе, получим
. Поделив первое уравнение на второе, получим

Интегрируя последнее уравнение при условии, что k =cp/cv= const, находим

После потенцирования имеем
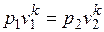 . *
. *
Это и есть уравнения адиабаты идеального газа при постоянном отношении теплоемкостей (k = const). Величина
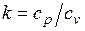
называется показателем адиабаты. Подставив cp = cv-R, получим k. Согласно классической кинетической теории теплоемкость газов не зависит от температуры, поэтому можно считать, что величина k также не зависит от температуры и определяется числом степеней свободы молекулы. Для одноатомного газа k =1,66 для двухатомного k =1,4, для трех- и многоатомных газов k =l,33.
Поскольку k> 1, то в координатах р, v линия адиабаты идет круче линии изотермы: при адиабатном расширении давление понижается быстрее, чем при изотермическом, так как в процессе расширения уменьшается температура газа.
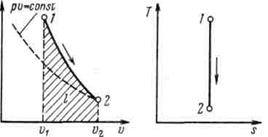
Рисунок 5.4 - Изображение адиабатного процесса в р, v- и Т, s-координатах
Определив из уравнения состояния, написанного для состояний 1 и 2, отношение объемов или давлений, получим уравнение адиабатного процесса в форме, выражающей зависимость температуры от объема или давления:
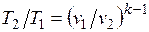 ;
;
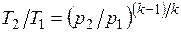 .
.
Работа расширения при адиабатном процессе согласно первому закону термодинамики совершается за счет уменьшения внутренней энергии и может быть вычислена по одной из следующих формул:
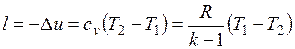 .
.
Так как 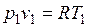 и
и 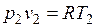 , то
, то
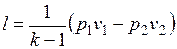 .
.
В данном процессе теплообмен газа с окружающей средой исключается, поэтому q=0. Выражение 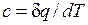 показывает, что теплоемкость адиабатного процесса равна нулю.
показывает, что теплоемкость адиабатного процесса равна нулю.
Поскольку при адиабатном процессе  = 0, энтропия рабочего тела не изменяется (ds =0 и s =const). Следовательно, на Т, s-диаграмме адиабатный процесс изображается вертикалью.
= 0, энтропия рабочего тела не изменяется (ds =0 и s =const). Следовательно, на Т, s-диаграмме адиабатный процесс изображается вертикалью.
Date: 2015-09-18; view: 544; Нарушение авторских прав