
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Задачи и задания для самостоятельного решения
|
|
Задача 1. В таблице для реакций N2O4→N2O3+1∕2O2 приведены значения констант скоростей при двух температурах. Необходимо вычислить:
а) энергию активации;
б) константу скорости при Т3;
в) температурный коэффициент скорости;
г) количество вещества, израсходованное за время τ
Порядок реакции считать по молекулярности.
Таблица
| Реакция | Т1,К | 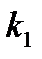
| 2,К | 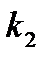
| 3,К | 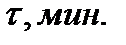
| 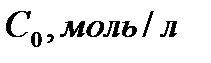
|
| N2O4 → N2O3 + 1/2O2 | 98,2 | 0,00203 | 88,2 | 0,47510 | 88,2 | 0,93 |
Решение.
а) для нахождения энергии активации воспользуемся интегральной формой уравнения Аррениуса:

б) для нахождения к 3 при Т3 воспользуемся той же формулой уравнения Аррениуса:

в) для определения температурного коэффициента скорости воспользуемся математическим выражением правило Вант – Гоффа:
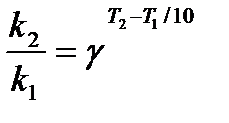

г) порядок реакции первый, поэтому воспользуемся кинетическим уравнением для реакций названного порядка:

Задание 1. В таблице приведены значения констант скоростей при двух температурах.
Вычислите:
а) энергию активации;
б) константу скорости при Т 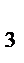
в) температурный коэффициент скорости;
г) количество вещества, израсходованное за время τ.
Порядок реакции считать по молекулярности. Начальные концентрации реагирующих веществ (с 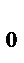 ) – одинаковы.
) – одинаковы.
Таблица
| Вар. | Реакция | Т 1,К | 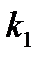
| Т 2,К | 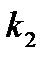
| Т 3,К | 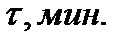
| 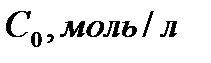
|
| H2+Br2→2HBr | 574.5 | 0.0856 | 497.2 | 0.00036 | 483.2 | 0.03 | ||
| H2+Y2→2HY | 599.0 | 0.00146 | 679.0 | 0.0568 | 648.2 | 2.83 | ||
| SO2Cl2 → SO2+Cl2 | 552.2 | 0.60910 | 593.2 | 0.13210 | 688.2 | 2.5 | ||
| COCl2→CO+Cl2 | 655.0 | 0.5310 | 745.0 | 67.710 | 698.2 | 104.5 | 0.8 | |
| 2NO→N2+O2 | 1525.2 | 0.47059 | 1251.4 | 0.1073 | 1423.2 | 2.83 | ||
| (CH2)3→CH3CH=CH2 | 833.2 | 0.00687 | 923.2 | 0.146 | 956.2 | 1.52 | ||
| PH3→1∕2H2+3∕2H2 | 953.2 | 0.00183 | 918.2 | 0.0038 | 988.2 | 0.87 | ||
| 2HY→H2+Y2 | 628.4 | 0.80910 | 780.4 | 0.1059 | 976.2 | 1.87 |
Date: 2015-09-17; view: 1635; Нарушение авторских прав