
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Контактное окисления оксида серы (IV)
|
|
Процесс окисления оксида серы (IV) является одним из немногочисленных простых химико-технологических процессов, осуществляемых в промышленном масштабе, а кончный продукт производства –серная кислота- одним из основных продуктов химической промышленности.
Объем и эффективность производства серной кислоты непрерывно возрастает. Получение серной кислоты контактным методом включает в себя следующие стадии: обжиг колчедана или сжигание серы, контактное окисление SO2 в SO3 и абсорбцию оксида серы (VI) с получением концентрированной серной кислоты.
В основе процесса контактного окисления оксида серы (IV) лежит реакция:
SO2 + 0,5O2 =SO3 + Q (6.1.)
Процесс протекает с выделением теплоты и уменьшением объема.
При температурах ниже 4000С равновесие почти полностью смещено в сторону продукта реакции, при температурах выше 10000С – в сторону исходных веществ. В интервале температур 400-10000С реакция обратима.
Таким образом, процесс окисления SO2 в SO3 простой, обратимый, экзотермический.
В соответствии с принципом Ле-Шателье на степень контактирования положительно влияют снижение температуры, повышение давления, увеличение концентрации кислорода и вывод продукта из сферы реакции.
Реакция из-за высокого значения энергии активации (Е=300 кДж/моль) протекает лишь при участии катализаторов. Процесс окисления с заметной скоростью для различных катализаторов начинается при определенной температуре- температуре зажигания. Реакция ускоряется в присутствии платины при температуре 2500С, оксида железа (III) при температурах не ниже 5500С, оксида ванадия (V) при температурах не ниже 4000С.
Платиновый катализатор обладает наибольшей активностью, однако дорог и быстро отравляется ядами. Оксид железа (III) – малоактивный катализатор.
Наиболее широкое применение нашли ванадиевые катализаторы (активный комплекс – V2O5 .K2S2O7). Ванадиевая
контактная масса наносится на поверхность пористого кремнеземистого носителя. Рабочий интервал температур 400-6500С.
Процесс гетерогенного катализа на пористом носителе, покрытым тонким слоем катализатора, многостадиен:
1) перенос газообразных веществ из объема к поверхности катализатора (внешняя диффузия),
2) диффузия реагирующих веществ внутри пор катализатора (внутренняя диффузия),
3) абсорбция O2 и SO2 на катализаторе,
4) химическое взаимодействие исходных веществ с участием катализатора,
5) десорбция SO3,
6) диффузия SO3 внутри зерна катализатора к его поверхности (внутренняя диффузия),
7) отвод продуктов реакции в объем (внешняя диффузия).
Скорость всего процесса определяется скоростью самой медленной стадии. В промышленных условиях общая скорость процесса определяется скоростью химической реакции, т.е. процесс протекает в кинетической области.
Выбор технологического режима.
Температура. Для получения высокого выхода оксида серы (VI) необходима температура 400-4250С. Однако скорость процесса при этой температуре мала даже при наличии катализатора. Выбор температурного режима, обеспечивающего высокую скорость экзотермической обратимой реакции, довольно сложен, так как изменение температуры различно сказывается на равновесном выходе продукта и на средней скорости процесса.
Если вести процесс при постоянной температуре 6000С, то реакция идет быстрее, однако равновесие смещается в сторону исходных веществ и выход SO3 падает.
Для обеспечения высокой интенсивности процесса необходимо проводить окисление оксида серы (IV) при меняющемся температурном режиме.
На рис.6.1. приведен график зависимости равновесного и практических выходов от температуры. С увеличением времени контактирования максимумы на кривых смещаются в сторону более низких температур. Кривую, соединяющую эти максимумы, называют линией оптимальных температур (ЛОТ). При проведении процесса по линии оптимальных температур окисление оксида серы (IV) протекает с максимально возможными скоростями в каждый момент. Понижение температуры к концу процесса с 600 до 4200С позволяет получить высокий выход продукта.
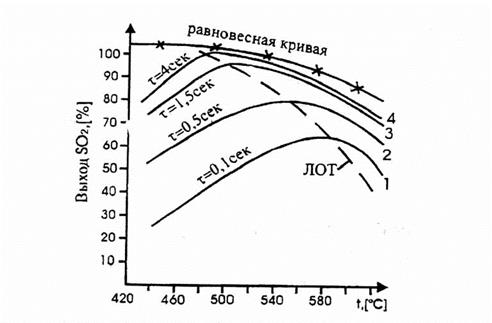
Рис.6.1. Зависимость практического выхода продукта от температуры при различном времени контактирования.
Соотношение исходных компонентов. При стехиометрическом соотношении компонентов превращение протекает недостаточно полно. Увеличение количества кислорода положительно сказывается на выходе. Обычно газ, поступающий в реакционный аппарат, содержит: 7% SO2, 11% O2 и 82% N2.
Давление. В зависимости от выбранной температуры эффективность воздействия давления различна. При низких температурах, когда равновесные степени контактирования оксида серы (IV) высокие, давление незначительно сказывается на смещении равновесия. При высоких температурах, когда окисление происходит далеко не полностью, давление может стать одним из решающих факторов повышения выхода SO3.
Процесс окисления оксида серы (IV) проводят при давлении 0,1 МПа, так как другими путями добиваются высокого выхода.
Date: 2015-09-18; view: 1711; Нарушение авторских прав