
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Давление
|
|
Давление в процессе окисления аммиака связано с температурой. Чем выше давление, тем требуется более высокая температура для достижения одного и того же выхода NO (рис.5.1.).
Проведение процесса под давлением имеет ряд преимуществ: повышается скорость процесса, увеличивается интенсивность катализатора, значительно возрастает скорость реакции 2NO+O2 =2NO2, которая является лимитирующей в производстве азотной кислоты.
Таким образом, процесс окисления аммиака до оксида азота (II) в промышленности проводят на платиново-родиевых катализаторах при температуре 9000С, давлении 0,8 МПа, при соотношение кислорода к аммиаку 1,7-1,9.
Технологические расчеты.
На основании полученных данных рассчитывают приближенный материальный баланс контактного аппарата. Определяют содержание аммиака и воздуха в аммиачно-воздушной смеси в объемных процентах. Для этого пользуются формулой:
C 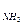 =
= 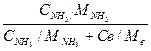 .100, (% объемн.)
.100, (% объемн.)
Где C 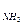 , Cв – концентрации аммиака и воздуха, %масс.,
, Cв – концентрации аммиака и воздуха, %масс.,
M 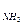 , Mв – молекулярные массы аммиака и воздуха.
, Mв – молекулярные массы аммиака и воздуха.
По известному расходу воздуха и объемным концентрациям аммиака и воздуха рассчитывают расход аммиака. Приводят расходы аммиака и воздуха к нормальным условиям. Затем определяют массовые количества введенных веществ, используя плотность газа при нормальных условиях.
Материальный баланс контактного аппарата для окисления аммиака.
| Приход | Расход | ||||||
| Наименование | л | г | % | Наименование | л | г | % |
| Аммиак | Оксид азота (II) | ||||||
| Воздух: | Азот по реакции | ||||||
| Кислород | Азот из воздуха | ||||||
| Азот | Кислород | ||||||
| Вода | |||||||
| Всего | Всего | ||||||
В таблице материального баланса приводятся литры при нормальных условиях, проценты –массовые.
По реакции 5.1. определяют количество полученного оксида азота (II), считая, что количество аммиака, израсходованного по этой реакции, равно общему количеству аммиака, умноженному на степень превращения его в оксид азота (II), выраженному в долях единицы.
Степень превращения аммиака в оксид азота (II) рассчитывают по формуле:
X = 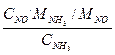 . 100, (%).
. 100, (%).
Остальной аммиак в основном окисляется непосредственно до азота по реакции (5.2.).
При составлении приближенного материального баланса можно пренебречь образованием из аммиака других веществ.
Количество оставшегося в газовой смеси кислорода определяют как разность между введенным и израсходованным по реакциям (5.1.) (5.2.).
Количество реакционной воды рассчитывают по уравнению (5.1) или (5.2.), так как независимо от того, окисляется аммиак до оксида азота (II) или азота, в обоих случаях из четырех молей аммиака получается шесть молей воды.
Date: 2015-09-18; view: 791; Нарушение авторских прав