
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Выбор оптимальных условий
|
|
1). Катализатор.
В качестве катализатора можно использовать металлы Iб подгруппы Периодической системы элементов: Ag, Au, Cu. В промышленности в основном используют серебряные катализаторы, так как на золотых и медных катализаторах идут реакции глубокого окисления метанола до НСООН и СО2.
Серебро применяют в виде сеток, гранул и чаще всего нанесенным на различные носители. Носители должны обладать достаточной механической и термической прочностью, а также химической инертностью. В настоящее время в качестве носителей используется природная пемза, корунд, алюмосиликаты.
Кислород, адсорбируясь на серебряном катализаторе, диссоциирует на атомы и образует с серебром по меньшей мере три вида комплексов:
О2 ↔2О
1 - Ag2O; 2 – AgO; 3 – Ag2O2
Соотношение между комплексами зависит от количества адсорбируемого кислорода и температуры процесса.
В комплексе 1 кислород связан с серебром наиболее прочно. Поэтому он будет ускорять реакцию дегидрирования (4.2.), в которой кислород участия не принимает.
Ag2O + CH3OH = Ag2O + CH2O + H2 (4.8.)
На комплексе 2 с менее прочно связанным кислородом, идет окисление метанола в формальдегид:
AgO + CH3OH = Ag + CH2O + H2O (4.9.)
Комплекс 3 ускоряет реакцию глубокого окисления метанола:
Ag2O2 + CH3OH = 2Ag + CO2 + 2H2O (4.10.)
Таким, образом, активными центрами поверхности катализатора являются атомы серебра, связанные в комплексы – кислородные соединения.
Процесс получения формальдегида является гетерогенно-каталитическим, идет при температуре выше 5000С во внешнедиффузионной области.
Температура.
Оптимальный температурный режим, прикотором достигается максимальный выход и селективность процесса – 600-7000С, рис, 4.1.
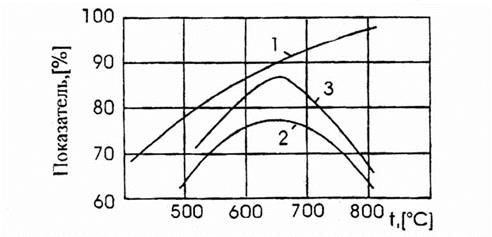
Рис.4.1. Зависимость конверсии спирта Х, выхода формальдегида 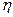 и селективности
и селективности 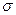 от температуры процесса: 1 –Х, 2 -
от температуры процесса: 1 –Х, 2 - 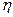 , 3 -
, 3 - 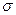 .
.
Конверсия или степень превращения метанола с повышением температуры увеличивается, так как растут скорости основных и побочных реакций. Как видно из рис.(4.1.), до температуры 6000С выход целевого продукта растет. Происходит это вследствии того, что скорость реакций образования формальдегида увеличивается с повышением температуры значительней, чем скорость побочных реакций. При температуре 600-7000С выход формальдегида достигает максимального значения.
В этом температурном интервале серебряный катализатор избирательно ускоряет основные реакции. Причем в пределах температурного интервала работы катализатора с ростом температуры увеличивается доля формальдегида, образующегося по реакции дегидрирования (4.2.). При дальнейшем повышении температуры выход формальдегида уменьшается. Объясняется это тем, что способность катализатора ускорять основные реакции падает, так как значительная часть поступающего кислорода начинает расходоваться на глубокое окисление метилового спирта до СО2, реакция (4.3.). Увеличивается скорость распада и окисления образовавшегося формальдегида (4.4.) и (4.6.).
Такое резкое снижение селективности процесса приводит к уменьшению выхода формальдегида. Следовательно оптимальный температурный режим процесса- 600-7000С.
Окислительное дегидрирование метанола в формальдегид в промышленности осуществляют в адиабатических реакторах, где совмещаются экзотермическая реакция окисления метанола с эндотермической реакцией дегидрирования. Реактор работает в автотермичном режиме. В этом состоит одно из основных преимуществ рассматриваемого процесса.
Состав реакционной смеси.
Конверсию метанола в формальдегид проводят кислородом воздуха. При выборе соотношения между кислородом и метанолом учитывают, что часть формальдегида образуется по реакции дегидрирования (4.2.) без участия кислорода. Поэтому количество кислорода, рассчитанное по реакции окисления (4.1.) на поступающий в процесс метанол, оказывается избыточным, что приводит к образованию продуктов глубокого окисления (4.3.) и увеличению температуры в реакционной зоне.
Максимальный выход формальдегида достигается при соотношении О2:СН3ОН = 0,35:1.
Следовательно, оптимальное соотношение кислорода и метанола составляет – 70% от стехиометрически рассчитанного по реакции (4.1.).
Время контактирования.
Зависимость выхода формальдегида от времени контактирования имеет максимум, что характерно для сложных процессов с последовательными побочными реакциями.
Оптимальное время контактирования – 0,01-0,03 с.
При уменьшении времени контактирования падает конверсия метанола, т.е. наблюдается его “проскок” через слой катализатора. При увеличении времени контактирования начинают протекать последовательные побочные реакции, в основном распад формальдегида:
НСОН = Н2 + СО (4.6.)
Для предотвращения распада проводят “закалку” образовавшейся паро-газовой смеси, т.е. резко снижают ее температуру с 600-7000С до 1000С.
Date: 2015-09-18; view: 1361; Нарушение авторских прав