
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Применение
|
|
Вулканизация каучука, получение эбонита, производство спичек, пороха, в борьбе с вредителями сельского хозяйства, для медицинских целей (серные мази для лечения кожных заболеваний), для получения серной кислоты.
СЕРОВОДОРОД
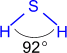
Газ, бесцветный, с запахом тухлых яиц, ядовит, растворим в воде. Ядовит. Получение
1) H2 + S → H2S↑ (при t) 2) FeS + 2HCl → FeCl2 + H2S↑
Химические свойства
1) Раствор H2S в воде – слабая двухосновная кислота.
Диссоциация происходит в две ступени:
H2S → H+ + HS- (первая ступень) HS- → 2H+ + S2- (вторая ступень)
Na2S – сульфид натрия;NaHS – гидросульфид натрия;
2) Взаимодействует с основаниями:
H2S + 2NaOH(избыток) → Na2S + 2H2O
H2S (избыток) + NaOH → NaНS + H2O
3) H2S проявляет очень сильные восстановительные свойства:
H2S-2 + Br2 → S + 2HBr
H2S-2 + 2FeCl3 → 2FeCl2 + S0 + 2HCl
H2S-2 + 4Cl2 + 4H2O → H2S+6O4 + 8HCl
3H2S-2 + 8HNO3(конц) → 3H2S+6O4 + 8NO + 4H2O
H2S-2 + H2S+6O4(конц) → S + S+4O2 + 2H2O
4) Сероводород окисляется:
· при недостатке O2 2H2S-2 + O2 → 2S0 + 2H2O
· при избытке O2 2H2S-2 + 3O2 → 2S+4O2 + 2H2O
5) Качественная реакция на сероводород и растворимые сульфиды - образование черного осадка PbS:
H2S + Pb(NO3)2 → PbS↓ + 2HNO3
Na2S + Pb(NO3)2 → PbS↓ + 2NaNO3
При обработке сульфида свинца (II) пероксидом водорода происходит реакция:
PbS + 4H2O2 = PbSO4 + 4H2O,
при этом образуется сульфат свинца (II), соединение белого цвета.
Таким образом реставрируют почерневшие масляные картины.

7) Реставрация:
PbS + 4H2O2 → PbSO4(белый) + 4H2O
Получение сульфидов
1) нагреванием металла с серой: Hg + S → HgS
2) Растворимые сульфиды получают действием сероводорода на щелочи:
H2S + 2KOH → K2S + 2H2O
3) Нерастворимые сульфиды получают обменными реакция
Pb(NO3)2 + Na2S → 2NaNO3 + PbS↓
Химические свойства сульфидов
1) Растворимые сульфиды сильно гидролизованы, вследствие чего их водные растворы имеют щелочную реакцию:
K2S + H2O → KHS +КОН
2) Сульфиды металлов, стоящих в ряду напряжений левее железа (включительно), растворимы в сильных кислотах:
ZnS + H2SO4 → ZnSO4 + H2S
Серная кислота
Особые свойства концентрированной серной кислоты
1. С водой образуются гидраты:
H2SO4 + nH2O = H2SO4 · nH2O + Q
Органические вещества обугливаются!!!
C12H22O11 (сахароза) → 12С (уголь) +11H2O
2. Серная кислота окисляет неметаллы:
C + 2H2SO4 = 2H2O + CO2 + 2SO2 S + 2H2SO4 = 3SO2 + 2H2O 2P + 5H2SO4 = 2H3PO4 + 5SO2 + 2H2O 3. Взаимодействие серной кислоты с металлами: H2SO4 (конц.) + Me = соль + H2O + Х
|
а) концентрированная H2+6SO4 – сильный окислитель; при взаимодействии с металлами (кроме Au, Pt) может восстанавливаться до S+4O2, S0 или H2S-2 (без нагревания не реагируют также Fe, Al, Cr - пассивируются):
2Ag + 2H2+6SO4 → Ag2+1SO4 + SO2 + 2H2O
8Na + 5H2+6SO4 → 4Na2SO4 + H2S + 4H2O
б) концентрированная H2SO4 реагирует при нагревании с некоторыми неметаллами за счет своих сильных окислительных свойств, превращаясь в соединения серы более низкой степени окисления, (например, SO2): С + 2H2SO4(конц) → CO2 + 2SO2 + 2H2O
S + 2H2SO4(конц) → 3SO2 + 2H2O 2P + 5H2SO4(конц) → 5SO2 + 2H3PO4 + 2H2O
ОКСИДЫ СЕРЫ
Оксид серы IV SO2 (сернистый ангидрид; сернистый газ)
Бесцветный газ с резким запахом; хорошо растворим в воде
Date: 2015-08-22; view: 745; Нарушение авторских прав