
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Кислоты и их соли
|
|
Важнейшие соли:
- 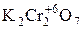 – дихромат калия. Выступает в роли окислителя в кислой среде. Окислителем служит ион –
– дихромат калия. Выступает в роли окислителя в кислой среде. Окислителем служит ион – 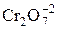 , восстанавливающийся до Cr+3.
, восстанавливающийся до Cr+3.
- 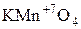 – перманганат калия.
– перманганат калия.
Восстанавливается до:

Кислая среда Нейтральная и слабая Щелочная среда
+2 щелочная среда +6
+4
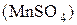
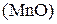
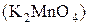
| Важнейшие кислоты | Элемент-окислитель | Уравнение полуреакции восстановления |
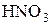
| N | 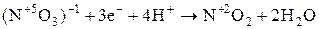
|
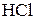
| H | 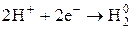
|
Разбавленная 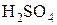
| H | 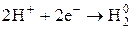
|
Концентрированная 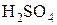
| S | 
|
Кислород-содержащие кислоты галогенов и их соли
(пример: 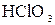 ) )
| Cl | 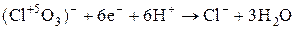
|
Состав продуктов восстановления 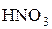 зависит от активности восстановителя и концентрации кислоты; чем активнее восстановитель и более разбавлена кислота, тем глубже протекает восстановление азота:
зависит от активности восстановителя и концентрации кислоты; чем активнее восстановитель и более разбавлена кислота, тем глубже протекает восстановление азота:
Продукты восстановления 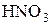 :
:

 концентрация
концентрация 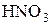

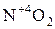

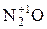
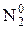
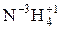
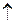 активность восстановителя
активность восстановителя
Состав продуктов восстановления 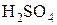 определяется главным образом активностью восстановителя:
определяется главным образом активностью восстановителя:
Продукты восстановления 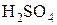


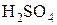
малоактивные металлы (Cu, Sb), акт. Ме
НВr,
некоторые неметаллы (С)
+4 0 -2
S+4O2 S0 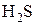 -2
-2
3) Ионы металлов в высшей степени окислен ия (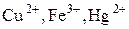 ).
).
Степень окисленности уменьшается при взаимодействии с восстановителем.
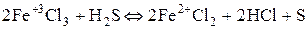 .
.
4) Н в с.о.. +1 выступает как окислитель главным образом в растворах кислот (при взаимодействии с Ме, стоящими в ряду напряжений до водорода)
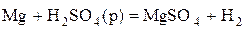 .
.
Date: 2015-07-27; view: 523; Нарушение авторских прав