
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Энтропия является величиной, характеризующей вероятность состояния термодинамической системы
|
|
Свойства энтропии:
1) В ходе необратимого процесса энтропия изолированной системы возрастает.
2) Энтропия изолированной системы, находящейся в равновесном состоянии максимальна.
Для обратимого процесса величина полученного количества теплоты определяется соотношением:
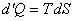 . .
| (25) |
Для изотермического процесса количество теплоты, полученного в ходе этого процесса равно:
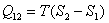 . .
| (26) |
Для адиабатического процесса – Q 12 = 0; то S 2 – S 1 = 0, и S 2 = S 1
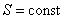 , ,
| (27) |
т.е. и адиабатический процесс также называют изоэнтропийным.
Получим для различных процессов формулы расчёта приращения энтропии.
1) Рассмотрим изобарный процесс: Р = const; m = const;
Запишем первое начало термодинамики для изобарного процесса в дифференциальной форме:
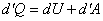 . .
| (28) |
Тогда приведённое количество теплоты можем записать в виде:
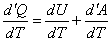 . .
| (29) |
Проинтегрировав соотношение, получим:
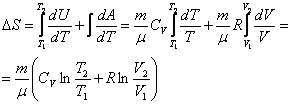
| (30) |
Соотношение (30) определяет приращение энтропии в процессах идеального газа.
2) Рассмотрим изохорный процесс: V = сonst; m = const;
Тогда из формулы (30) получим для изохорного процесса:
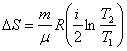
| (31) |
3) Рассмотрим изотермический процесс: Т = const; m = const;
Из формулы (30) получаем для изотермического процесса:
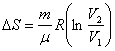
| (32) |
4) Рассмотрим адиабатный процесс: Δ Q = 0, следовательно Δ S = 0, тогда
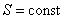
| (33) |
Date: 2015-07-27; view: 582; Нарушение авторских прав