
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Зависимость скорости химической реакции от различных факторов
|
|
Подставим уравнение Аррениуса в формулу 10.1. В результате получим:
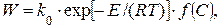 (10.3)
(10.3)
где k 0 – пред экспоненциальный множитель (константа);
E – энергия активации, кДж/к моль;
R – газовая постоянная, кДж/(к моль· К);
Т – абсолютная температура, К;
С – концентрация реагирующих веществ.
На величину скорости реакции (уравнение 10.3) влияют следующие факторы: природа реагирующих веществ, температура, концентрация, давление и катализаторы.
Зависимость  от природы реагирующих веществ проявляется через величину энергии активации. Чем больше
от природы реагирующих веществ проявляется через величину энергии активации. Чем больше 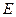 , тем меньше
, тем меньше  . И наоборот, чем меньше
. И наоборот, чем меньше 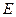 , тем больше величина
, тем больше величина  .
.
На величину  существенное влияние оказывает температура. Повышение температуры примерно на 10 градусов приводит к увеличению W в два раза. Для метановоздушных смесей повышение абсолютной температуры в два раза приводит к увеличению скорости горения в 5· 108 раза.
существенное влияние оказывает температура. Повышение температуры примерно на 10 градусов приводит к увеличению W в два раза. Для метановоздушных смесей повышение абсолютной температуры в два раза приводит к увеличению скорости горения в 5· 108 раза.
Из уравнения 10.3 видно, что с повышением концентрации  возрастает. Однако в газоиспользующие приборы и установки газ подается непрерывно, поэтому величина
возрастает. Однако в газоиспользующие приборы и установки газ подается непрерывно, поэтому величина  остается постоянной.
остается постоянной.
С повышением давления  возрастает, т.к. при сжатии газов возрастает концентрация. В большинстве случаев сжигание газового топлива производится при атмосферном давлении, поэтому влияние давления на величину W не проявляется. В случае сжигания газового и жидкого топлива в двигателях влияние давления существенно.
возрастает, т.к. при сжатии газов возрастает концентрация. В большинстве случаев сжигание газового топлива производится при атмосферном давлении, поэтому влияние давления на величину W не проявляется. В случае сжигания газового и жидкого топлива в двигателях влияние давления существенно.
Катализаторы ускоряют протекание реакций. Как правило, для ускорения реакций горения используются металлы и их оксиды переходных периодов системы Д.И. Менделеева: хром, марганец, железо, кобальт, родий, осмий, платина и другие. Горение газов протекает достаточно быстро, поэтому при гомогенном горении катализаторы используются редко. В противоположность катализаторам есть вещества замедляющие протекание реакций – это ингибиторы.
Date: 2015-07-27; view: 468; Нарушение авторских прав