
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Примеры. Пример 1. Определить ТПР пламени метилового спирта, если температура его кипения равна 65оС
|
|
Пример 1. Определить ТПР пламени метилового спирта, если температура его кипения равна 65оС.
Решение.
Расчет проводим по формуле (3.1.1), значение констант определяем по табл. 8 приложения для нормальных жирных спиртов
tH =0,5746·65-33,7=3,6°С=276,6 К;
tВ =0,6028·65-15,0=30оС=303 К.
Определим относительную ошибку расчета. По табл. 16 приложения находим, что ТПР пламени метилового спирта составляют 280 - 320К:

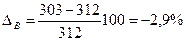
Следовательно, результаты расчета занижены менее чем на 3%.
Пример 2. Определить температурные пределы распространения пламени ацетона, если его концентрационные пределы в воздухе равны 2,2 - 13,0%. Атмосферное давление – нормальное.
Решение.
По формуле (3.1.2) определим давление насыщенного пара ацетона, соответствующее нижнему и верхнему температурным пределам распространения пламени,

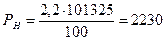 Па;
Па; 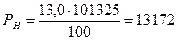 Па
Па
 мм.р.ст.;
мм.р.ст.;  мм.р.ст.
мм.р.ст.
Из уравнения Антуана следует
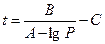
Из табл. 12 приложения находим значение констант А, В и С для ацетона
А =7,25058; В =1281,721; С =237,088.
lgPН =1,2235; lgPВ =1,9994.
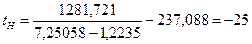 оС=248 К;
оС=248 К;
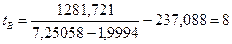 оС=281 К.
оС=281 К.
Для решения этой же задачи можно воспользоваться данными табл.7 приложения. Из табл.17 следует, что НТПР пламени находим между температурами 241,9-252,2оС, а ВТПР пламени - между 271,0 и 280,7 К.
Линейной интерполяцией определим ТПР пламени:
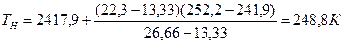
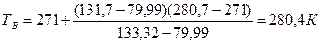
3.2. Расчет температуры вспышки и воспламенения
Температура вспышки - минимальная температура жидкости, при которой в условиях, специальных испытаний, происходит воспламенение паров жидкости при кратковременном воздействии высоко энергетического источника без последующего перехода горения в стационарный диффузионный режим.
Температура воспламенения - минимальная температура жидкости, при которой в условиях, специальных испытаний, происходит воспламенение паров жидкости при кратковременном воздействии высоко энергетического источника с последующим переходом горения в стационарный диффузионный режим.
Наиболее распространенным и достаточно точным является Ра - счет температур вспышки и воспламенения по формуле В.И. Блинова
 (3.2.1)
(3.2.1)
где 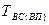 -температура вспышки (воспламенения)
-температура вспышки (воспламенения)
Р НП- давление насыщенного пара при температуре вспышки (воспламенения); Д - коэффициент диффузии поров горючего в воздухе;
n - стехиометрический коэффициент при кислороде - количество молей кислорода, необходимое для полного окисления (до CO2, Н2О, SO2:) одного моля горючего вещества;
А - константа метода определения (табл. 3.2.1).
Таблица 3.2.1
| Температура, К | Значение параметра А, 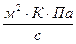
|
| Вспышки в закрытом тигле | 28,0 |
| Вспышки в открытом тигле | 45,3 |
| Воспламенения | 53,3 |
Коэффициенты диффузии некоторых газов и паров в воздухе при нормальных условиях (Д0) приведены в табл. 7 приложения. При их отсутствии последние определяют по формуле
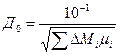 (3.2.2)
(3.2.2)
где 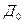 - коэффициент диффузии, м3/с;
- коэффициент диффузии, м3/с;
μi - количество i-го элемента в молекуле горючего вещества;
ΔМi - атомные (элементные) составляющие (табл. 3.2.2).
При температуре, отличающейся от нормальной, коэффициент диффузии Д может быть рассчитан по соотношению
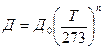 (3.2.3)
(3.2.3)
где n - показатель значение которого приведено в табл. 7 приложения
Таблица 3.2.2
| Название i -го элемента | Значение ΔМ * |
| Углерод | 25-50 |
| Водород | |
| Кислород | |
| Азот | |
| Сера | |
| Хлор | |
| Бром | |
| Йод | |
| Фтор |
* значение ΔМ зависит от числа атомов углерода и их положения в молекуле горючего:
1) ΔМ =25 для атомов углерода, входящих в ароматический цикл;
2) ΔМ =25+ЗС - для атомов углерода в открытой цепи, если их количество меньше или равно восьми (С, 8);
3) ΔМ =50 - для атомов углерода в открытой цепи при С>8;
4) ΔМ =25+2С - для атомов углерода, входящих в неароматический цикл при С<8;
5) ΔМ =42 - для атомов углерода, входящих в неароматический цикл при С>8.
Простым, но менее четным является расчет температур вспышки в закрытом тигле по формуле Элея
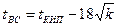 (3.2.4)
(3.2.4)
где tВС - температура вспышки, оС;
tКИП - температура кипения, оС;
k – коэффициент, определяющий по формуле:
k=4mC+mH+4mS+mN-2mO-2mCl-3mF-5mBr (3.2.5)
где mC, mH, mS, mN, mO, mCl, mF, mBr – количество элементов углерода, водорода, серы, азота, кислорода, хлора, фтора, брома в молекуле горючего вещества.
Температура вспышки в закрытом тигле может быть определена по нижнему температурному пределу воспламенения
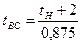 (3.2.6)
(3.2.6)
эта формула применима, если 0< tВС <160oC.
Date: 2015-07-27; view: 1937; Нарушение авторских прав