
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Электрофизиологические свойства нейрона
|
|
Мембранный потенциал и ионные механизмы его формирования. Мембранный потенциал (МП) покоя нервной клетки - постоянная электрическая поляризация ее мембраны, т.е. существование разности потенциалов между цитоплазмой нейрона и внеклеточной средой, причем внутренность клетки оказывается электроотрицательной. В типичном случае его величина находится в пределах от -60 до - 70 мВ. Любое снижение этого потенциала (сдвиг по направлению к нулю) называется деполяризацией, а повышение - гиперполяризацией. МП поддерживается до тех пор, пока клетка жива, и исчезает вместе с ее гибелью. Причины возникновения МП - общие для всех клеток, в том числе и нервных: асимметрия ионных концентраций по обе стороны мембраны и неодинаковая ее проницаемость для этих ионов.
Концентрация ионов внутри и снаружи только что изолированного аксона кальмара [1]:
| Ион | Концентрация, мМ | ||
| аксоплазма | кровь | морская вода | |
| Калий | |||
| Натрий | |||
| Хлор | 40-150 | ||
| Кальций | 0,0003 |
Суммарное влияние различных ионов на МП можно обобщить уравнением постоянного поля Гольдмана, которое хорошо описывает наблюдаемые в экспериментах значения трансмембранной разности потенциалов:
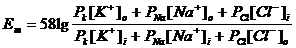 ,
,
где 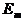 - МП (мВ), а
- МП (мВ), а 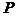 - относительная мембранная проницаемость.
- относительная мембранная проницаемость.
МП нейрона не совпадает с равновесными потенциалами ни одного из ионов, которые могут быть рассчитаны по уравнению Нернста (мВ):
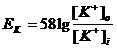 и
и 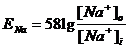
Поэтому даже в состоянии покоя через мембрану идут потоки ионов, которые взаимно компенсируют друг друга и суммарный ток равен нулю. Вкладом ионов хлора можно пренебречь, т.к. равновесный потенциал этого иона очень близок к равновесному калиевому потенциалу. Наиболее удобной формой представления МП служит его электрическая модель, или эквивалентная схема (рис. 2). Равновесный потенциал для каждого иона изображен источником тока соответствующей полярности и электродвижущей силы (Е). С этим источником последовательно соединено сопротивление (R), отражающее проницаемость мембраны для ионов. При этом следует иметь в виду то, что в большей степени обычно интересует проводимость G (R= 1/ G), которая связана с проницаемостью (например, для калия): GK = PK [K+]o / [K+]i. Каналы для каждого иона расположены отдельно и не зависят друг от друга. Благодаря наличию липидов, мембрана обладает электрической емкостью (С) и служит как бы конденсатором. Липиды, будучи плохими проводниками электричества способны накапливать заряды по обе стороны мембраны. Регистрируемый МП соответствует алгебраической сумме потенциалов, создаваемых ионными «источниками тока».
Рис. 2. Эквивалентная электрическая схема участка мембраны нейрона. Rm - сопротивление трансмембранному току утечки. H-H отмечает Na+ и K+ проводимости, соответствующие модели Ходжкина-Хаксли [6]:
Проводимости (G) создаются работой соответствующих каналов, свойства которых описаны в тексте и отмечены на рис. 6.
1 - цитоплазматическая и 2 - внеклеточная стороны нейрональной мембраны
Мембранный потенциал и метаболизм. Неравновесное распределение ионов по обе стороны мембраны поддерживается на протяжении жизни клетки системами активного транспорта (метаболический насос), осуществляющими перенос ионов против движущих сил. Лучше всего изучен насос, переносящий через мембрану ионы калия и натрия против их концентрационных градиентов - Na+ , K+ -зависимая АТФ-аза. Этот фермент, катализирующий реакцию расщепления АТФ, одновременно выполняет функцию переносчика. Это крупный белок, связанный с мембраной и состоящий из двух полипептидных компонентов с молекулярной массой около 100 000 Д. Молекула этого белка, состоящая из двух субъединиц a и b, пронизывает мембрану насквозь, прикрепляясь к ее наружной стороне небольшими гликопротеиновыми цепями. С внутренней стороны мембраны происходит преимущественной связывание Na+ и АТФ, а с наружной - K+ и различных ингибиторов типа гликозидов (например, уабаина) (рис.3). Метаболический насос, осуществляющий перенос ионов Na+ и K+ в пропорции 1:1 поддерживает концентрационные градиенты ионов по обе стороны мембраны, но не вносит вклада в создание МП. При отклонении от такой пропорции (например, 2:1 или 3:2) насос участвует в формировании МП покоя - электрогенный насос.
Рис. 3. Схема работы механизма Na+ - K+ -насоса [6]:
А. Происходящее в присутствии ионов К+ внеклеточной среды аллостерическое конформационное изменение a-субъединицы насоса вызывает ее дефосфорилирование в месте связывания АТФ. При этой конформации возникает входящий ток ионов К+ против электрохимического градиента. Б. Внутриклеточное связывание ионов Na+ в специфическом месте молекулы вызывает конформационное изменение, способствующее фосфорилированию в месте связывания АТФ. Возникающий выходящий ток ионов Na+ также направлен против их электрохимического градиента. Приведенный на схеме процесс совершается при стехиометрическом соотношении 3 иона Na+ к 2 ионам К+. Насос выполняет свою функцию чередованием двух конформационных состояний.
a, b - субъединицы насоса; 1 - цитоплазма; 2 - внеклеточная среда; 3 - место связывания K+ и гликозида уабаина; 4 - места связывания АТФ; 5 - место связывания Na+.
Таким образом, МП создается в результате как пассивных, так и активных механизмов, причем степень их относительного участия может быть различной. Из этого следует, что МП не должен быть одинаков во всех типах нейронов и, кроме того, их реакции на те или иные воздействия также должны быть разными. В некоторых клетках или волокнах МП может быть достаточно высоким - порядка -80 мВ, в других - он значительно ниже - до -40 мВ (например в фоторецепторах сетчатки позвоночных его низкое значение обусловлено большим значением входящего тока ионов Na+). Метаболические насосы, ответственные за активный перенос, зависят от температуры, и поэтому у пойкилотермных животных их вклад в создание МП претерпевает, в соответствии с колебаниями температуры, суточные и сезонные изменения. Активность насосов зависит также от диаметра нервного волокна: чем это волокно тоньше, тем отношение поверхности к объему выше, и активность насосов, необходимая для поддержания распределения ионов, больше. Таким образом, МП в покое в значительной степени зависит от различных функций нервных клеток.
Потенциал действия. Изменение заряда мембраны, которое вызывается внешним током, носит название физического электротона, деполяризация соответствует катэлектротону, а гиперполяризация - анэлектротону (при этом изменения МП вытекают из закона Ома). Постепенное нарастание и спад заряда мембраны при включении и выключении тока отражает наличие ее емкости. Пассивные изменения МП имеют место только в том случае, когда пропускаемый через мембрану ток не очень велик. При усилении гиперполяризующего тока изменения на мембране продолжают подчиняться простым физическим законам - более сильный ток вызывает более сильную гиперполяризацию. При нарастании катэлектротона до критического уровня возникает электрическая реакция, которая не может быть дальше контролируема; она протекает самопроизвольно независимо от того, будет ли дальше пропускаться внешний поляризующий ток или нет. Заряд мембраны начинает резко падать, доходит до нуля, и мембрана перезаряжается. Затем, через короткий промежуток времени, измеряемый миллисекундами, этот процесс завершается, и заряд на мембране возвращается к исходному состоянию. Эти электрические явления соответствуют возникновению распространяющегося возбуждения (нервного импульса) и получили название потенциала действия (ПД). Единственным путем создания активной реакции этого типа является деполяризация мембраны до критического уровня, независимо от того имеет ли место искусственное пропускание электрического тока или естественное раздражение (синаптическое действие, действие адекватного раздражения на рецептор и т.д.).
Величина критической деполяризации может быть измерена по отношению как к нулевому уровню МП (абсолютный порог возбуждения клетки), так и к уровню потенциала покоя (относительный порог возбуждения клетки). Абсолютный порог возбуждения варьирует у различных нервных клеток в пределах (-40) - (-50) мВ. В относительных величинах для возбуждения нервной клетки нужно снизить ее МП покоя примерно на 10%, чтобы появился нервный импульс.
Свойства потенциала действия. Первое свойство: амплитуда ПД не зависит от силы раздражения, т.е. от величины деполяризации мембраны (правило «все или ничего»). Причина заключается в природе клеточной реакции, которая сама себя поддерживает (носит регенеративный характер), а раздражение - только запускающий момент для этого внутриклеточного механизма. Искусственно можно варьировать амплитуду ПД в широких пределах, смещая исходный уровень МП. При этом абсолютное значение трансмембранной разности потенциалов, создающееся на вершине ПД, остается постоянным, но относительная его амплитуда изменится. При сильном снижении исходного уровня МП, наступят изменения и абсолютного уровня ПД: он станет меньше и, в конце концов, приобретет недоразвитую, абортивную, форму. Подавление механизма генерации ПД при сильном снижении исходного уровня МП - катодическая депрессия Вериго - отражает инактивацию этого механизма.
Второе свойство - рефрактерность - кратковременное снижение возбудимости нервной ткани. Вызвать второй ПД сразу же после возникновения первого нельзя, т.к. наступает период абсолютной рефрактерности. Способность переходить в активируемое состояние восстанавливается постепенно; через какой-то промежуток времени приложение деполяризующего тока уже вызовет ПД, но последний окажется частично инактивированным, и его амплитуда будет неполной. Период появления неполных ответов называется периодом относительной рефрактерности; он следует за периодом абсолютной рефрактерности (рис. 4 А). Чем медленнее развивается ПД, тем длительнее у него рефрактерный период. Наличие рефрактерного периода ограничивает возможности нервной клетки воспроизводить нервные импульсы, что приводит к существованию предельной частоты возбуждения, которую клетка может пропустить без изменений. Если частота раздражения превысит эту частоту, то последующие импульсы начнут попадать в рефрактерный период предыдущих, и наступит трансформация их частоты. Чем длительнее рефрактерность, тем меньше предельная частота. Лабильность - максимальное число импульсов, которое данная структура может передать в единицу времени без искажений (Н.Е.Введенский). У мотонейронов эта величина составляет 500,а у интернейронов - до 1000 импульсов в секунду.
Рис. 4. Инактивация Na+-тока и рефрактерность [3]:
А. ПД, вызванные сдвигом напряжения (пассивная деполяризация, пунктир). В течение 2 мс после первого ПД повторное возбуждение невозможно, т.к. порог бесконечно высок - период абсолютной рефрактерности. Чуть позже при пороге, превышающим нормальное значение (покой), могут возникать уменьшенные ПД - период относительной рефрактерности. Б. Состояния Na+- канала, переход между которыми друг в друга может происходить при деполяризации или реполяризации (стрелки).
Третье свойство: способность оставлять после себя длительные следовые изменения возбудимости, которые проявляются в изменении порога для последующих раздражений: следовая супернормальность и следовая субнормальность (следовые повышение и понижения возбудимости). Нервный импульс, длящийся несколько миллисекунд, оставляет после себя примерно в 100 раз более длительный след. В основе изменения возбудимости клетки при следовых процессах лежат определенные изменения электрической поляризации мембраны. После окончания ПД сначала имеет место следовая деполяризация, а затем следовая гиперполяризация.
Четвертое свойство: способность потенциала действия к самораспространению без затухания за счет тех электрических токов, которые он создает.
Деполяризация мембраны дендритов и сомы, распространяясь, благодаря пассивным электрическим свойствам нейрона, вызывает ПД первоначально в одном участке клетке - аксонном холмике или начальном сегменте аксона (у начала миелинизации), которые являются триггерными зонами (рис. 5). Место возникновения ПД определяется типом нейронов: у сенсорных - начальный сегмент аксона, у мото- и интернейронов - аксонный холмик. Порог возникновения ПД в этих участках мембраны более низок по сравнению с телом и дендритами из-за более высокой плотности потенциалозависимых Na+-каналов.
Рис. 5. Схема функциональной организации нейрона [5]:
А. Функциональные части нейрона. Б. Антеро- и ретроградный транспорт везикул, связанный с транслокацией медиатора.
1 - область входа (локальные потенциалы, амплитудное кодирование), 2 - подведение сигналов от других нейронов, 3- дендрит, 4- синапс, 5- аксонный холмик, 6 - начальный сегмент, 7 - аксон, 8 - синаптическая терминаль, 9 - область выхода (распространяющиеся ПД, частотное кодирование), 10 - антероградный транспорт везикул в аксоне вдоль микротрубочек с помощью кинезина, 11 - пресинаптическая мембрана, 12 - ретроградный (обратный) транспорт, 13 - эндосома, 14 - аппарат Гольджи.
Ионные токи возбуждения. ПД обусловлен временным повышением ионной проницаемости его мембраны для ионов натрия и калия, что создает соответствующие трансмембранные токи. Для регистрации трансмембранных токов применяется метод фиксации потенциала, при котором МП удерживается на определенном уровне. Суммарный ток состоит из раннего входящего и более позднего выходящего компонентов, что отражает различие в скоростях изменений проницаемости мембраны для ионов натрия и калия.
Развитие ПД обусловлено взаимоотношениями процессов повышения натриевой проводимости, повышения калиевой проводимости и натриевой инактивации. Между натриевой проводимостью и степенью деполяризации мембраны существует положительная обратная связь: при деполяризации натриевая проводимость возрастает, что увеличивает исходную деполяризацию; в результате натриевая проводимость еще больше увеличивается, т.к. ионная проницаемость мембраны зависит от ее потенциала. Количественное описание ионных токов возбудимой мембраны аксона, а также расчет изменений трансмембранного потенциала было выполнено А.Ходжкиным и А.Хаксли.
Молекулярные механизмы возбуждения. Проницаемость мембраны обусловлена существованием в ней сквозных пор - ионных каналов, диаметр которых около 0,3 - 0,5 нм. Предполагается существование молекулярных «ворот», обусловливающих открытие (активацию), закрытие и инактивацию каналов. Состояние каналов зависит от величины МП (потенциалозависимые, или потенциалоуправляемые, каналы). Как полагают, натриевый канал выстлан шестью отрицательно заряженными атомами кислорода, обеспечивающими прохождение через него положительно заряженного иона. Избирательность данного канала для ионов Na+ определяется его диаметром; способность других ионов (кальция, лития и т.д.) проходить через этот канал зависит от их размеров. Различные участки или компоненты ионных каналов служат местами воздействия ряда лекарственных препаратов, ядов и т.п. При изменениях МП возникают изменения конформации молекул канального белка, что сопровождается появлением воротных токов очень малой амплитуды. Плотность натриевых каналов может быть весьма высока: в мембране гигантского аксона кальмара от 100 до 600 на 1 мкм2, в мембране перехвата Ранвье миелинизированного волокна кролика 12000 на 1 мкм2.
Многообразие ионных каналов обеспечивает соответствующее разнообразие ионных токов. Ниже перечислены некоторые из них (рис.6):
Входящие токи:
1) INa -быстрый натриевый (классический канал Ходжкина-Хаксли). Обеспечивает быструю деполяризацию во время развития ПД. Обнаружен в мембране гигантского аксона кальмара, тел и аксонов многих нейронов, скелетных мышц. Блокируется тетродотоксином и сакситоксином.
2) ICa - кальциевый. Обеспечивает умеренно быструю деполяризацию и длительные ПД с «плато». Обнаружен в эмбриональных клетках, конусах роста, телах и дендритах многих нейронов, клетках желез и сердца. Блокируется ионами Co2+ и Ni3+. Вклад ионов кальция в создание ПД может иметь важное значение. Во-первых, этот ион участвует в работе целого ряда клеточных механизмов. Во-вторых, ионы Ca2+ регулируют проницаемость мембраны для других ионов, в частности для K+. В-третьих, Ca2+ играет важнейшую роль в модуляции проведения в электрических синапсах и в выделении медиатора в химических синапсах.
3) IB - медленный входящий (Na+ и/или Ca2+), пачечный. Обеспечивает медленную деполяризацию (до нескольких секунд), генерацию пачек импульсов, следовую деполяризацию. Обнаружен в нейронах пачечного типа у моллюсков и позвоночных (например, клетки Пуркинье).
4) IT (Ca) - кальциевый кратковременный, быстро инактивирующийся. Возможно, играет важную роль в усилении слабых сигналов в дендритах и, таким образом, в синаптической интеграции.
Выходящие токи:
1) IK(DR) - поздний выходящий ток (классический канал Ходжкина-Хаксли). Обеспечивает реполяризацию после пика ПД, а также регуляцию частоты импульсации. Присутствует в соматических и аксональных мембранах многих нейронов. Блокируется тетраэтиламмонием (ТЭА) и 4-аминопиридином (4-АМП).
2) IK(Ca) - Ca-зависимый калиевый канал. Активируется при деполяризации, повышении внутриклеточной концентрации, участвуя в ее регуляции и поддержании МП. Вызванная этим током гиперполяризация стабилизирует низкую частоту следования ПД. Распространен повсеместно (кроме аксона кальмара). Блокируется ионами Ba2+, а также ТЭА, апамином и харибдотоксином.
3) IA - быстрый выходящий (кратковременный) калиевый ток. Активируется при незначительных изменениях МП и быстро инактивируется. Регистрируется в нейронах моллюсков. Блокируется ТЭА и 4-АМП.
4) IAR - аномальный выпрямляющий K+-ток. Инактивируется при деполяризации и активируется только при гиперполяризации ниже потенциала покоя. При этом ток K+ должен быть направлен внутрь, смещая МП в направлении EK. Выключение соответствующей проводимости при деполяризации приводит к появлению продленных ПД с "плато" (кардиомиоциты, клетки электрического органа).
Рис. 6. Некоторые типы потенциалозависимых ионных каналов, создающих натриевые и кальциевые (А), а также калиевые (Б) токи [6]:
Для каждого типа указано: 1 - диапазоны изменений МП, соответствующие периоду активного состояния каналов (горизонтальные линии); 2 - макроскопические ионные токи (суммированные токи отдельных каналов), которые вызывают это изменение потенциала и 3 - активность ионных каналов, которая лежит в основе макроскопических токов. На графиках 2 и 3 положительный знак тока соответствует его выходящему направлению, отрицательный - входящему. Подробности о свойствах каналов см. в тексте.
Кроме потенциалозависимых каналов (ответственных за ПД) выделяют каналы, состояние которых изменяется механическими деформациями мембраны, процессами фосфорилирования канальных белков или связывания с ними ионов Ca2+, а также каналы, активируемые лишь медиаторами (обусловливающие возникновение синаптических потенциалов). Сейчас, однако, установлено, что в некоторых участках нейрона потенциалозависимые каналы могут обладать рецепторами для медиаторов. И наоборот, во многих случаях синаптические потенциалы, возникающие в ответ на действие медиатора, зависят от уровня МП покоя. Наличие каналов со смешанными свойствами позволяет нервной системе более гибко, в зависимости от функционального состояния организма и уровня активности нейронных сетей, модифицировать ритм импульсации, с одной стороны, и интегрировать синаптические влияния - с другой.
Проведение потенциала действия. При возникновении в каком-либо участке клетки ПД к соседним участкам мембраны текут электротонические, или местные, токи, обусловленные электрическими (кабельными) свойствами нервных клеток. Под действием этих токов деполяризация мембраны, возникающая в момент ПД, распространяется на соседние участки; когда потенциал этих участков достигает критического уровня (порог возбуждения), в них возникает нервный импульс. Таким образом, местные токи распространяются пассивно, а нервный импульс проводится активно. Скорость этого распространения при прочих равных условиях тем выше, чем больше диаметр волокна.
Рис. 7. Распространяющийся вдоль гигантского аксона кальмара ПД (t° = 18,5° C) [3]:
Рисунок можно рассматривать как моментальный снимок потенциала действия, т.е. как распределение разности потенциалов вдоль мембраны волокна (шкала абсцисс, мм) или временной отрезок изменения потенциала в области одной точки этой мембраны (шкала абсцисс, мс). Направление распространения ПД - справа налево. Возникающий во время восходящей фазы ПД входной ток выходит в еще не возбужденной области мембраны и деполяризует ее до порога возбуждения, благодаря чему ПД распространяется дальше. Обратному направлению распространения ПД препятствуют более низкая плотность локальных токов и состояние рефрактерности аксональной мембраны (инактивация Na+ - каналов, см. рис.4 Б). Оси ординат - МП (левая), плотность открытых каналов на мкм2 площади мембраны (правая).
В миелинизированных волокнах позвоночных потенциалозависимые каналы в основном сосредоточены в мембране перехватов Ранвье. Мембрана между перехватами имеет мало таких каналов и поэтому здесь возможно только электротоническое распространение. Последнее весьма эффективно, т.к. вследствие высокого сопротивления и низкой емкости миелиновой оболочки ток проводится вдоль волокна на далекие расстояния без утечки через мембрану. Нервный импульс «перепрыгивает» с одного с одного перехвата к другому - сальтаторный механизм проведения, - благодаря чему достигается максимальная скорость проведения при минимальном диаметре волокна и наименьшей интенсивности метаболических процессов.
Скорости проведения нервных импульсов в различных волокнах теплокровных (классификация по Эрлангеру и Гассеру):
| Тип волокна | Диаметр волокна, мкм | Скорость проведения, м/c |
A 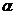
| 13 - 22 | 70 - 120 |
A 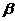
| 8 - 13 | 40 - 70 |
A 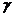
| 4 - 8 | 15 - 40 |
A 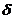
| 1 - 4 | 5 - 15 |
| B | 1 - 3 | 3 - 14 |
| C | 0.5 - 1.0 | 0.5 -2 |
Группа А включает наиболее толстые, хорошо миелинизированные моторные и чувствительные волокна, группа В - слабомиелинизированные, преганглионарные волокна вегетативной нервной системы, Группа С - немиелинизированные, постганглионарные (симпатические) волокна.
Date: 2015-07-17; view: 768; Нарушение авторских прав