
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Водородный электрод
|
|
Водородный электрод состоит из платиновой пластинки, покрытой платиновой чернью (для увеличения активной поверхности электрода) и погруженный в раствор, содержащей катионы водорода, обычно раствор HCl или H2SO4, На пластинку подается ток водорода, который поглощается платиной (учебник Ершова, с. 472).
 (рис.3)
(рис.3)
Водород, растворенный в платине, частично, под действием силовых полей атомов платины, диссоциирует на протоны и электроны:
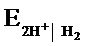

 H2 2H+ + 2е. В результате такая платиновая пластина приобретает способность обмениваться с раствором ионами водорода. Условное обозначение водородного электрода Pt(H2) | 2Н+. Электродный потенциал возникает на границе Pt- раствор кислоты и обозначается.
H2 2H+ + 2е. В результате такая платиновая пластина приобретает способность обмениваться с раствором ионами водорода. Условное обозначение водородного электрода Pt(H2) | 2Н+. Электродный потенциал возникает на границе Pt- раствор кислоты и обозначается.
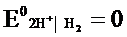 Если водородный электрод находится в стандартных условиях (Т = 298 К, СH+ = 1 моль/л, Р = 1 атм), он называется стандартным водородным электродом. Потенциал стандартного водородного электрода условно принят равным нулю:.
Если водородный электрод находится в стандартных условиях (Т = 298 К, СH+ = 1 моль/л, Р = 1 атм), он называется стандартным водородным электродом. Потенциал стандартного водородного электрода условно принят равным нулю:.
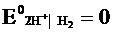 Металлический электрод соединяют проводником с водородным электродом (оба электрода находятся в стандартных условиях) и измеряют ЭДС цепи: ЭДС = Е+ - E–, где E+ и Е– потенциалы положительного и отрицательного электродов. Т.к., то ЭДС будет равна электродному потенциалу данного металла. Такой электродный потенциал называется стандартным электродным потенциалом и обозначается
Металлический электрод соединяют проводником с водородным электродом (оба электрода находятся в стандартных условиях) и измеряют ЭДС цепи: ЭДС = Е+ - E–, где E+ и Е– потенциалы положительного и отрицательного электродов. Т.к., то ЭДС будет равна электродному потенциалу данного металла. Такой электродный потенциал называется стандартным электродным потенциалом и обозначается 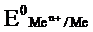 .
.
Стандартный электродный потенциал численно равен электродвижущей силе со знаком «+» или «-» гальваническою элемента, составленного из стандартного водородного и стандартного данного электродов.
Стандартные электродные потенциалы распространенных металлов в водных растворах при 25 °С представлены в соответствующих таблицах.
Последовательность металлов по возрастанию стандартного потенциала Е0 (от больших отрицательных к большим положительным значениям) называется рядомстандартныхэлектродныхпотенциалов или электрохимическим рядом напряжений. У металлов, стоящих до водорода, стандартные электродные потенциалы отрицательные. После водорода - положительные.
Таким образом, при стандартных условиях электродные потенциалы имеют определенные стандартные значения. Величиныстандартныхэлектродныхпотенциаловколичественнохарактеризуютвосстановительнуюспособностьметалловиокислительнуюспособностьихионов. Так, Li - самый сильный восстановитель, а Аu - самый слабый, и наоборот, ион Аu3+ - самый сильный окислитель, а ион Li+ - самый слабый.
Для условий отличных от стандартных (иная концентрация электролита и иная температура) электродные потенциалы будут иметь другие значения. Их можно рассчитать по уравнению Нернста (немецкий физик, 1888г):

где  - электродный потенциал метала.
- электродный потенциал метала.
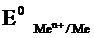 - стандартный электродный потенциал металла,
- стандартный электродный потенциал металла,
R - универсальная газовая постоянная, равная 8,31 Дж/моль*К,
Т - абсолютная температура, К.
n - заряд ионов металлов.
F - число Фарадея, равное 96500 Кл/моль,
ln - натуральный логарифм,
а - активность ионов металла в растворе, моль/л.
Таким образом, величина электродного потенциала зависит от природы металла (E0), активности ионов металла в растворе и температуры.
В разбавленных растворах активность примерно равна молярной концентрации а ≈ с.
Для расчетов при температуре 298 К (25 °С), подставив константы R, F и умножив значение ln на 2,3 (коэффициент перехода от натуральных логарифмов к десятичным), получают уравнение Нернста в следующей форме:
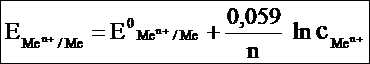 |
Пример. Потенциал медного электрода (n = 2) в растворе CuCl2 с концентрацией ионов меди С = 0,001 моль/л равен:
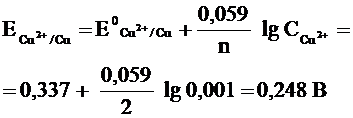
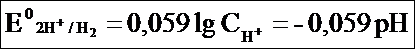 Запишем уравнение Нернста, для водородного электрода, находящегося в нестандартных условиях СH ≠ 1 моль/л при 298° К:
Запишем уравнение Нернста, для водородного электрода, находящегося в нестандартных условиях СH ≠ 1 моль/л при 298° К:
По этой формуле, зная величину электродного потенциала водородного электрода, находящегося в исследуемом растворе, можно рассчитать рН этого раствора. Однако для серийных измерений водородный электрод не применяется в силу громоздкой конструкции и чувствительности к посторонним веществам и каталитическим ядам.
Date: 2015-07-17; view: 1964; Нарушение авторских прав