
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

I – инспираторные (вдох). 4 page
|
|
10-2. Никотин и алкоголь: механизмы действия на организм и ЦНС; причины и последствия формирования привыкания и зависимости.
Алкоголь:

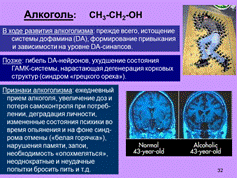

Никтоин:
Известны 2 типа рецепторов к Ацх:
первый из них реагирует на Ацх и агонист никотин (токсин табака);
второй реагирует на Ацх и агонист мускарин (токсин мухомора).
Никотин, как агонист рецепторов Ацх, защищает табак от поедания насекомыми; для человека – слабый «разрешенный» наркотик.

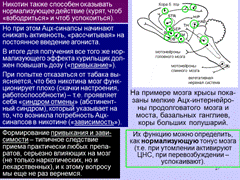
10-3. Гипоталамус как эндокринный центр: реакция на концентрацию гормонов в крови; выделение либеринов и статинов, конкретные примеры их функций.
Промежуточный мозг:
гипофиз и эпифиз (эндокринные железы);таламус,гипоталамус, субталамус
Гипоталамус является главным центром эндокринной и вегетативной регуляции, а также главным центром биологических потребностей (и связанных с ними эмоций).
Ядра, регулирующие деятельность эндокринной системы: прежде всего, это паравентрикулярное и супраоптическое.
Эти ядра содержат нейроэндокринные клетки, аксоны которых идут в заднюю долю гипофиза и здесь выбрасывают гормоны в кровь. Другие нейроны, рас-положенные в основном в средней части гипоталамуса («серый бугор») выделяют в сосудистое сплетение гормоны, регулирующие работу передней доли гипофиза.
Большинство гормонов гипоталамуса и гипофиза – белковые и пептидные молекулы. В гипоталамусе они син-тезируются в телах нейросекреторн. клеток (вырезаются из белков-предшественников), загружаются в везикулы и переносятся по аксонам к месту экзоцитоза.
Далее гормоны выделяются в межклеточную среду с наружной стороны эпителиальных клеток капилляров, путем диффузии попадают в кровь и с кровью доставляются к клеткам-мишеням
Действие гормонов на клетки-мишени развивается обычно теми же путями, что и в случае медиаторов: гормон действует на специфические рецепторы, запуская (через G-белки) синтез вторичных посредников, которые влияют на активность белков-насосов, ферментов, включают и выключают гены (на уровне ДНК) и т.д.
В ряде случаев гормон действует на клетки другой эндокринной железы, управляя ее активностью («тропные гормоны», характерны для передней доли гипофиза).
В ряде случаев гормон действует на клетки другой эндокринной железы, управляя её активностью («тропные гормоны», характерны для передней доли гипофиза).
Рецепторы гормонов имеются и на нервных клетках, благодаря чему эндокринная и нервная системы тесно взаимодействуют.
Гормоны, которые синтезируются в гипоталамусе(парвентрикулярное и супраоптическое ядра) и выбрасываются в кровь в задней доле гипофиза: Это пептиды
• вазопрессин (антидиуре-тический гормон – ADH; влияет на почки)
Основной эффект вазопрессина: усиление обратного всасывания воды в почках (точнее, в нефронах; анти-диурез).
Кроме того, он сужает сосуды («вазопрессор»).
В ЦНС вазопрессин и его фрагменты в очень низких дозах улучшают обучение и память (перспективные ноотропы).
Вазопрессин выделяется при повышении концентрации NaCl в крови: сигнал для почек «экономить воду»; параллельно возникает чувство жажды.
• окситоцин ( матка, молочная железа).
Главные эффекты окситоцина:
запуск сокращений гладкомышечных клеток матки (роды) и протоков молочной железы (лактация; не путать с действием пролактина, усиливающим образование молока).
В ЦНС окситоцин и его фрагменты противодействуют эффектам вазопрессина, ухудшая обучение и память.
Как и пролактин, окситоцин выделяется в ходе акта сосания (при механической стимуляции соска; нервно-эндокринная дуга).
Переходим к гормонам передней доли гипофиза. Их существенно больше; это уже знакомые нам пролактин и опиоидные пептиды (эндорфины; регуляция уровня болевой чувствительности).
Кроме того, в передняя доля гипофиза вырабатывает тропные гормоны:
тиреотропный (тиреостимулирующий – TSН; влияет на щитовидную железу);
адренокортикотропный (АСТН; влияет на кору надпочечников);
FSH и LH влияют на половые железы мужчин и женщин;
гормон роста (соматотропный) – на рост тела, его общий размер.
•Выброс каждого из гормонов передней доли гипофиза регулируется гормонами гипоталамуса («рилизинг»-факторы), которые могут активировать секрецию гипофиза (либерины) либо тормозить ее (статины). Так, дофамин является статином для пролактина и некоторых тропных гормонов.
• Статины и либерины выделяются в кровь нейроэндокринными клетками серого бугра, измеряющими содержание в крови «конечного» гормона (тироксина, половых гормонов и др.).
Избыток конечного гормона ведет к выбросу статина и снижению секреции гипофизом тропного гормона. Если конечного гормона в крови мало, то усиливается выброс соответствующего либерина (и тропного гормона).
Наличие таких отрицательных обратных связей позволяет поддерживать стабильное содержание в крови многих важнейших гормонов.
• Начнем со щитовидной железы. Она выделяет йодсодержащие гормоны тироксины, усиливающие обмен веществ (образование энергии) во всех клетках организма, в т.ч. в мозге.
Выделение тироксинов (Т4 и Т3) усиливает тиреотропный гормон передней доли гипофиза (TSH).
Гипоталамус, измеряя концентрацию тироксинов в крови, усиливает выделение либо статина (его роль играет дофамин) либо либерина (тиролиберина, TRH; является также либерином пролактина).
Тиролиберин активирует выброс TSH.
Опасен как дефицит, так и избыток тироксинов в организме.
При дефиците (например, из-за нехватки йода в пище) – снижение обмена веществ, вялость, депрессии («микседема»); у новорожденных – оставание умственного развития.
При избытке – нервозность, бессонница, повышенный аппетит и худоба, гиперактивность симпатической НС, «выпученные» глаза.
Причиной в обоих случаях могут быть аутоиммунные нарушения.
• Тиролиберин (трипептид Glu-His-Pro) значимо влияет на работу ЦНС.
Он «дополняет» действие тироксинов: увеличивает уровень бодрствования, оказывает антидепрессантное действие, усиливает работу дыхательного центра (в клинике: введение недоношенным детям).
• Соматотропный гормон (гормон роста – GH).
Как тропный гормон, активирует выделение печенью IGF-1 (иммуно-подобного фактора роста) и совместно с ним определяет рост скелета, мышц и конечный рост (размер тела) человека.
Гипоталамус оценивает концентрацию гормона роста и IGF-1, изменяя баланс между выделением соответствующих статина (соматостатина) и либерина (соматолиберина – GHRH = соматотропин-рилизинг фактор).
Нарушение работы этой системы ведет к карликовости; избыточная активность – к гигантизму.
Акромегалия – результат резкого увеличения продукции соматотропного гормона в зрелом возрасте (лишь часть органов способна продолжать рост: гипертрофия сердца, хрящевых тканей и др.).
•Влияния на ЦНС соматостатина: снижение пищевой мотивации, уровня эмоциональности и болевой чувствительности, небольшое снижение уровня бодрствования.
Соматостатин оказывает тормозящее действие на ЖКТ, подавляет активность многих других внутренних органов («всеобщий ингибитор»).
11-1. Постоянно открытые и электрочувствительные ионные каналы: сравнение свойств, разнообразие, функции в синапсах, нервных и мышечных клетках.
Сигнал по мембране нейрона передаётся в виде коротких электрических импульсов – потенциалов действия (ПД). Этот процесс можно сравнить с передачей информации с помощью включения и выключения фонарика (ПД= «вспышка света»).
Но для того, чтобы фонарик работал, нужна батарейка – источник электрической энергии. В случае нейрона таким источником является постоянный внутриклеточный заряд – потенциал покоя (ПП).
Потенциал покоя нейрона – его постоянный отрицательный заряд, равный в среднем –70 мВ. Измерить ПП можно с помощью тончайшей, особым образом вытянутой стеклянной трубочки-микроэлектрода. Его кончик имеет диаметр <1 мкм, что позволяет практически без повреждения мембрану клетки. Микроэлектрод (в т.ч. канал внутри кончика) заполнен раствором соли, проводящим электрический ток. Это позволяет оценить, сравнить заряд цитоплазмы нейрона с зарядом межклеточной среды.
Наличие ПП – результат жизнедеятельности нейрона, совместного функционирования всех биополимеров и органоидов клетки; погибший нейрон быстро теряет ПП. Первопричина ПП – разность концентраций ионов K+ и Na+ внутри и снаружи нейрона. Эту разность создаёт работа особого белка-насоса Na+-K+-АТФазы (Na+-K+-насоса).
Na+-K+-АТФаза обменивает находящиеся внутри клетки ионы Na+ на захваченные в межклеточной среде ионы K+, затрачивая значительное количество АТФ.
В основе этих процессов – открывание и закрывание электрочувствительных Na + - и К + -каналов.
Эти каналы имеют створки, реагирующие на изменение заряда внутри нейрона и открывающиеся, если этот заряд становится выше -50 мВ.
Если заряд внутри нейрона вновь ниже -50 мВ – створка закрывается, т.к. положительные заряды, расположенные на ней, притягиваются к отрицательно заряженным ионам цитоплазмы.
Положительные заряды створки – это заряды аминокислот, входящих в состав соответствующей молекулярной петли белка-канала.
Открытие электрочувствительного Na + -канала «разрешает» вход Na + в клетку. Открытие электрочувствительного К + -канала «разрешает» выход К + из клетки.
Na + -каналы открываются очень быстро после стимула и самопроизвольно закрываются примерно через 0.5 мс.
К + -каналы открываются медленно – в течение примерно 0.5 мс после стимула; закрываются они в большинстве своем к моменту снижения заряда нейрона до уровня ПП. Именно разная скорость открытия Na + -каналов и К + -каналов позволяет возникнуть сначала восходящей, а затем – нисходящей фазе ПД.
(сначала ионы Na + вносят в нейрон положительный заряд, а затем ионы К + выносят его, возвращая клетку в исходное состояние). Для закрытия Na + -каналов на пике ПД служит дополнительная (внутриклеточная, инактивационная, И-) створка – h-ворота. Вторая створка (активационная, А-) – m-ворота.
· Реполяризация: абсолютная рефрактерность (полная нечувствительность к стимуляции из-за закрытой h-створки)
· Гиперполяризация:относительная рефрактерность (пороговый стимул >, чем обычно)
Поскольку К + -каналы начинают закрываться довольно поздно (вслед за проходом уровня -50 мВ), заряд нейрона после ПД нередко опускается ниже ПП (следовая гиперполяризация, относит. рефрактерность).
Вершина ПД («овершут») – момент равенства токов натрия и калия; она не м.б. выше равновесного потенциала для натрия, который составляет 61.5 мВ при соотношении Na +out: Na +in = 10: 1 (по уравнению Нернста).
· тетродотоксин –яд рыбы фугу (аминогруппа работает как «пробка» для Na+-канала)
ТЕА – тетраэтиламмоний: работает как «пробка» по отношению к К + -каналу.
В результате восходящая фаза ПД изменяется мало, нисходящая – затягивается до 50 и > мс (реполяризация происходит за счет постоянно открытых К + -каналов, которых примерно в 100 раз <, чем электрочувствительных); ТЭА вызывает глубокую потерю сознания.
Na + -K + -АТФаза постоянно откачивает из клетки избыток Na + и возвращает назад K +. Без этого нейрон потерял бы ПП уже через несколько сотен ПД. Важно также, что чем > проникло в клетку Na+, тем активнее работает насос. Если ПД возник хотя бы в одной точке мембраны нейрона – он распространяется по всей мембране.
Причина: деполяризация в точке появления ПД играет роль запускающего (надпорогового, около 100 мВ) стимула по отношению к соседним точкам. Это сходно с «кругами на воде», а точнее – с горением бенгальского огня.
Скорость такого распространения низка и не превышает у человека 1-2 м/с (диаметр аксона 1-2 мкм). ДП от исходной точки распространяется во все стороны и, убегая по аксону, запускает выброс медиатора
· Открытие Na+-каналов «разрешает» вход Na+ в клетку; развивается волна деполяризации – «возбуждающий постсинаптический потенциал» (ВПСП).
· Открытие K+-каналов «разрешает» выход K+ из клетки; развивается волна гиперполяризации – «тормозный постсинаптический потенциал» (ТПСП).
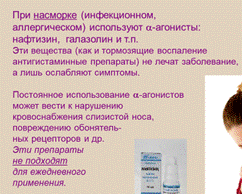
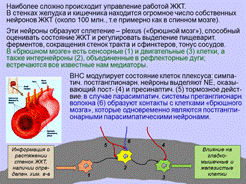
Управление работой сердца.
С клетками-пейсмекерами («водители ритма») контактируют как симпатические, так и парасимпатические волокна, выделяя Ne и Ацх, они регулируют соотношение постоянно открытых Na+- и K+-каналов, управляет частотой сердцебиений. С «рабочими» клетками сердца контактируют только симпатические волокна; выделяя Ne, они увеличивают открывание Ca2+ каналов. В результате на фазе плато в мышечную клетку входит больше Ca2+, сокращение усиливается. Стимуляция симпатических нервов: частота разрядов пейсмекера растёт за счёт увеличения Na+- проводимости и снижения K+-проводимости.
!! Ø Для возникновения потенциала покоя также необходимо существование в мембране нервных клеток открытых ионных каналов, в результате чего мембрана становится проницаемой для определенных ионов, получающих возможность свободно перемещаться между цитоплазмой и межклеточной средой. Ключевое значение для появления ПП имеют постоянно открытые (проточные) К+-каналы. Они представляют собой белковые молекулы, проход внутри которых специфически настроен на пропуск ионов К+.
!! Ø Ионы, участвующие в генерации ПД, те же, что и в случае потенциала покоя — Na+ и К+. При развитии ПД натрий входит в нейрон, а калий выходит. Ионные каналы, через которые они движутся, относятся к отдельному классу — потенциал-зависимым (электрочувствительным) ионным каналам.
Запуск импульсной активности в нервной системе осуществляют два основных фактора.
· Первый из них — стимулы, действующие на чувствительные клетки сенсорных систем и изменяющие проницаемость их мембраны. Это приводит к развитию особых рецепторных потенциалов и в итоге — к генерации ПД.
· Второй фактор — выделение медиатора из пресинаптического окончания. Попав в синаптическую щель, медиатор воздействует на постсинаптическую мембрану, возбуждая или тормозя следующий нейрон. Процессы подобного возбуждения или торможения связаны с деятельностью еще одного типа ионных каналов — лиганд-зависимых (хемочувствительных). Они находятся на мембране, непосредственно окружающей синаптический контакт. Обычно они закрыты. Их открывание происходит лишь при появлении медиатора, несущего сигнал химического вещества (отсюда термин «хемочувствительные»). Лиганд-зависимые каналы можно разделить на три основных класса: избирательно проницаемые по отношению к ионам Na+, ионам К+ и ионам С1~. Отрывание первых из них приведет к входу в клетку ионов Na+ и деполяризации нейрона (рис. 3.14, а), во время которой разность потенциалов на мембране оказывается приближенной к порогу запуска ПД. В этот момент меньший, чем обычно, стимул может вызвать реакцию нейрона, т. е. нервная клетка находится в относительно возбужденном состоянии. В связи с этим локальная деполяризация мембраны под действием медиатора была названа возбуждающим постсинаптическим потенциалом (ВПСП). Медиаторы, вызывающие ВПСП, отнесены к группе возбуждающих медиаторов. Открывание хемочувствительных С1~-каналов приводит к входу в клетку ионов хлора; открывание К+-каналов — к выходу ионов калия.
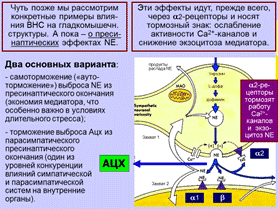
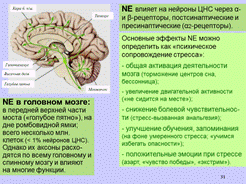
11-2. Типы и подтипы рецепторов норадреналина (НА). Агонисты и антагонисты рецепторов НА: примеры, разнообразие эффектов, практическое применение.

Рецепторы:

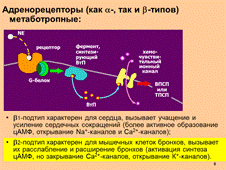



Ослабить деятельность сердца при гипертонии наиболее эффективно можно с помощью
Б1-антагонистов (атенолол) и антагонистов Сa2+-каналов (верапамил).

 |
11-3. Тропные гормоны гипофиза: регуляция выделения, общая характеристика, функции, конкретные примеры. Влияние тропных гормонов на работу ЦНС.
Промежуточный мозг:
гипофиз и эпифиз (эндокринные железы);таламус,гипоталамус, субталамус
Гормоны гипофиза:
Тиреокальцитонин-отложение кальция в костной ткани
Тиреотропный гормон -регуляция работы щитовидной железы
Соматотропный гормон -регуляция роста и дифференцировки системы орагнов, органов, клеток
Соматотропный гормон (гормон роста – GH).
Как тропный гормон, активирует выделение печенью IGF-1 (инсулино-подобного фактора роста) и совместно с ним определяет рост скелета, мышц и конечный рост (размер тела) человека.
Гипоталамус оценивает концентрацию гормона роста и IGF-1, изменяя баланс между выделением соответствующих статина (соматостатина) и либерина (соматолиберина – GHRH = соматотропин-рилизинг фактор).
Нарушение работы этой системы ведет к карликовости; избыточная активность – к гигантизму.
Гонадотропный гормон -регуляция работы половых желез
LH и FSH – лютеинизирующий и фолликулостимулирующий гормоны («гонадотропины»).
Несмотря на названия, в равной мере влияют на семенники мужчин и яичники женщин. Их функции:
активация синтеза и выделения половых гормонов;
стимуляция образования и созрева-ния половых клеток – сперматозои-дов и яйцеклеток (в пузырьках-фол-ликулах, далее следует овуляция).
Рилизинг-фактор гонадотропинов – пептид люлиберин (GnRH).
В ЦНС он активирует половое пове-дение, повышает эмоциональность, улучшает обучение
Липотропин-регуляция обменов жиров
Меланоцитостимулирующий г-н
Теперь речь пойдет о ядрах(гипоталамуса), регулирующих деятельность эндокринной системы: прежде всего, паравентрикулярном и супраоптическом.
Эти ядра содержат нейроэндокринные клетки, аксоны которых идут в заднюю долю гипофиза и здесь выбрасывают гормоны в кровь. Другие нейроны, рас-положенные в основном в средней части гипоталамуса («серый бугор») выделяют в сосудистое сплетение гормоны, регулирующие работу передней доли гипофиза.
Переходим к гормонам передней доли гипофиза. Их существенно больше; это уже знакомые нам пролактин и опиоидные пептиды (эндорфины; регуляция уровня болевой чувствительности).
Кроме того, передн. доля гипофиза вырабатывает тропные гормоны:
тиреотропный (тиреостимулирующий – TSН; влияет на щитовидную железу);
адренокортикотропный (АСТН; влияет на кору надпочечников);
гонадотропные FSH и LH влияют на половые железы мужчин и женщин;
соматотропный (гормон роста) – на рост тела, его общий размер.
Выброс каждого из гормонов передней доли гипофиза регулируется гормонами гипоталамуса («рилизинг»-факторы), которые могут активировать секрецию гипофиза (либерины) либо тормозить ее (статины). Так, дофамин является статином для пролактина и некоторых тропных гормонов (см. лекцию о DA и 5-НТ).
Выделение тироксинов(щитовидка) (Т4 и Т3) усиливает тирео-тропный гормон передней доли гипофиза (TSH; тиреостимулирующий гормон). Гипоталамус, измеряя концентрацию тироксинов и TSH в крови, усиливает выделение статина (его роль играет дофамин) либо либерина (тиролиберина, TRH; является также либерином пролактина).
Тиролиберин активирует выброс TSH.
Акромегалия – результат резкого увеличения продукции соматотроп-ного гормона в зрелом возрасте (лишь часть органов способна продолжать рост: гипертрофия сердца, хрящевых тканей и др.).
Влияния на ЦНС соматостатина: снижение пищевой мотивации, уровня эмоциональности и болевой чувствительности, небольшое снижение уровня бодрствования.
Соматостатин оказывает тормозящее действие на ЖКТ, подавляет активность многих других внутренних органов («всеобщий ингибитор»).
12-1. Нейроны-пейсмекеры, их свойства, функции, регуляция активности; участие в работе дыхательных и локомоторных центров. Клетки-пейсмекеры сердца.
Интересным вариантом генерации ПД являются пейсмекерные нейроны (клетки-пейсмекеры). Они обладают большой постоянной проницаемостью мембраны для ионов Na+. В результате у клеток-пейсмекеров не существует стабильного ПП. Разность потенциалов на их мембране постоянно стремится вверх. Когда она достигает порогового значения, происходит запуск ПД.
После ПД заряд внутри клетки оказывается на довольно низком уровне, ПП вновь растет и запускается следующий ПД, в целом же наблюдается ритмический рисунок разрядов. Рост заряда 1 внутри клетки, связанный с большим током утечки Na+, приводит к периодической самопроизвольной генерации потенциалов действия. Нейроны-пейсмекеры находятся в дыхательном центре продолговатого мозга, сходные же свойства имеют клетки центра сердечного автоматизма
Нейроны-пейсмекеры (водители ритма): у некоторых клеток так много постоянно открытых Na+-каналов, что заряд цитоплазмы не способен удерживаться на стабильном уровне и медленно смещается вверх (деполяризация).
При достижении порога запуска ПД происходит генерация импульса, после заряд нейрона отбрасывается к «минимуму» (около -60 мВ и даже ниже). Затем вновь начинается деполяризация, запуск ПД и т.д. В ЦНС человека такими свойствами обладают нейроны дыхательного центра. Пейсмекерами являются и клетки – водители сердечного ритма. Чем больше постоянно открытых Na+-каналов, тем чаще следуют ПД. Регуляция частоты разрядов идет также за счет открывания особых типов К+-каналов, реагирующих на гормоны, медиаторы и др. Чем > таких каналов открыто, ниже «минимум» и реже частота ПД.
• у пейсмекеров сердца нет фазы плато, ПД гораздо более короткий;
суммарный ПД всех клеток сердца – электрокардиограмма (ЭКГ);
распространение ПД по сердцу – за счет электрических синапсов.
Основное скопление клеток-пейсмекеров сердца – в верхней части правого предсердия («водитель сердечного ритма»). Отсюда ПД распространяется сначала по предсердиям, потом по желудочкам. Пейсмекеры сердца – видоизмененные мышечные клетки.
• Дыхательные нейроны, активность которых вызывает инспирацию (вдох) или экспирацию (выдох), называются соответственно инспираторными и экспираторными нейронами. Инспираторные и экспираторные нейроны иннервируют дыхательные мышцы.
Среди нейронов вдоха ключевую роль играют клетки-пейсмекеры, находящиеся в ядрах нижней части ромбовидной ямки.
Врождённо обусловленная частота их активации у человека: примерно 1 волна в 5 сек (12 раз в минуту = частота дыхания во сне).
От клеток-пейсмекеров (генераторов ритма)(Интересным вариантом генерации ПД являются пейсмекерные нейроны (клетки-пейсмекеры). Они обладают большой по-
постоянной проницаемостью мембраны для ионов Na+. В резульрезультате у клеток-пейсмекеров не существует стабильного ПП.Разность потенциалов на их мембране постоянно стремится вверх.
Когда она достигает порогового значения, происходит запуск ПД.) ПД передаются к другим дыхательным нейронам и мотонейронам шейных и грудных сегментов спинного мозга, запускающим сокращение диафрагмы и межрёберных мышц.
Вдох приводит к постепенному растяжению лёгких и стенок грудной клетки. Растяжение активирует особые механорецепторы (отростки чувствительных нервных клеток, входящие в состав X нерва), передающие сигнал в продолговатый мозг и мост. Этот сигнал тормозит инспираторные и включает экспираторные нейроны (вдох сменяется выдохом). После выдоха возникает пауза (до нового включения пейсмекеров). На частоту работы пейсмекеров (долю постоянно открытых Na+-каналов) влияют сигналы от хеморецепторов и ствола мозга.
Хеморецепторы: концентрация O2 и CO2 в крови; влияния ствола: эмоции (голубое пятно), температура (гипоталамус), центры бодрствования, боль, стресс и др. Возможен, кроме того, произвольный контроль дыхания.
Ещё о дыхательных центрах:
• инспираторные нейроны – это не только пейсмекеры, но и клетки, «зацикливающие» ПД по замкнутому контуру, что даёт возможность оказывать на мотонейроны стабильное активирующее действие;
• хеморецепторы CO2 (и H+) представляют собой нейроны на дне ромбовидной ямки; активируются в основном при физической нагрузке;
• хеморецепторы O2 расположены в каротидном синусе (область разветвления на наружную и внутреннюю сонные артерии); важны, например, при подъёме в горы (на высоте 5км воздуха в 2 раза меньше);
• пробуждение приводит к активации пейсмекеров центрами бодрствования, и частота дыхания растёт до 16-18 в мин; при эмоциях и физической нагрузке – до 30-40 в мин.
12-2. Глутаминовая кислота (ГлК) и формирование памяти: пути модификации ГлК-синапсов (роль NMDA-рецепторов, фосфорилирование и синтез новых рецепторов).
Глутаминовая кислота (Glu) – главный возбуждающий медиатор (около 40% всех нейронов); проведение основных потоков информации в ЦНС (сенсорные сигналы, двигат. команды, память).
Память – способность мозга сохранять информацию и воспроизводить её через некоторые промежутки времени. По времени сохранения информации память бывает кратковременной и долговременной. В основе кратковременной памяти лежит циркуляция нервных импульсов в замкнутых нейронных цепях. Долговременная память связана со структурными изменениями в нейронных сетях. Специальные пептиды, синтезируемые нейронами, облегчают процесс возбуждения клеток в моменты извлечения информации «из памяти». В формировании памяти участвуют нейроны височных долей больших полушарий, ретикулярная формация ствола мозга, гипоталамус. Различают следующие виды памяти: двигательную, зрительную, слуховую, осязательную, смешанную.
Наиболее изучены NMDA-рецепторы. Уникальная особенность NMDA-рецепторов состоит в том, что их канал может блокировать ион Mg2+ («магниевая пробка»). В такой ситуации рецептор выключен, и ВПСП не возникает. Однако, если заряд в нейроне оказывается выше уровня -30 мВ, Mg2+ удаляется из канала («выбивание пробки»), и рецептор переходит в рабочее состояние.
Этот механизм – один из важнейших способов резко усилить эффективность работы синапса, создать новый канал для передачи информации. Подобные изменения лежат в основе процессов обучения и формирования памяти. Наиболее очевидный способ
удаления Mg2+: ПД, запущенный с помощью не-NMDA-рецепторов (например, АМРА), находящихся на той же постсин. мембране. Данный синапс исходно не пропускал слабые сигналы, вызывающие небольшой выброс Glu.
После однократной сильной стимуляции, запустившей ПД через не-NMDA-рецепторы, произошло «выбивание пробок».
Теперь на постсин. мембране включились NMDA-рец. (их м.б. в неск. раз больше, чем не-NMDA), и даже слаб. сигнал вызывает большой ВПСП, запуская ПД.
Подобного рода синапсы, способные практически мгновенно увеличить эффективность работы, характерны для коры больш. полушарий и, особенно, гиппокампа, избирательно связанного с кратковременной памятью.
Входящий в клетку Са2+ может запускать цепь хим. реакций, активиру-ющих не-NMDA-рецепторы (прежде всего, за счет присоединения фосф. кислоты к АМРА-рецепторам – фосфорилирования).
В обоих случаях измененное состояние синапса сохраняется в течение нескольких минут-часов («кратковременная память»).
Date: 2016-11-17; view: 606; Нарушение авторских прав