
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Белковая буферная система.
|
|
Белковая буферная система представляет собой совокупность альбуминов и глобулинов - белков, составляющих основную часть плазмы крови (~90%).
Изоэлектрические точки этих белков лежат в интервале значений рН = 4,9-6,3, т. е., в слабокислой среде. Поэтому в физиологических условиях (при рН = 7,4) белки находятся преимущественно в формах «белок-основание» и соль «белка-основания».
Соответствующее кислотно-основное равновесие:

смещено в сторону преобладания формы «белок-основание».
Буферная емкость, определяемая белками плазмы, зависит от концентрации белков, их вторичной и третичной структуры и числа свободных протонакцепторных групп. Эта система может нейтрали-зовать как кислые, так и основные продукты. Однако вследствие преобладания формы «белок-основание», ее буферная емкость значи-тельно выше по кислоте и составляет: для альбуминов 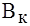 = 10 ммоль/л, а для глобулинов
= 10 ммоль/л, а для глобулинов 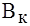 = 3 ммоль/л.
= 3 ммоль/л.
4. Аминокислотная буферная система.
Буферная емкость свободных аминокислот плазмы крови незначительна как по кислоте, так и по щелочи. Это связано с тем, что почти все аминокислоты имеют значения  , заметно отличающиеся от 7,4. Поэтому при физиологическом значении рН = 7,4 их мощность мала. Практически только одна аминокислота - гистидин (
, заметно отличающиеся от 7,4. Поэтому при физиологическом значении рН = 7,4 их мощность мала. Практически только одна аминокислота - гистидин ( = 6,0) - обладает значительным буферным действием при значениях рН, близких к рН плазмы крови.
= 6,0) - обладает значительным буферным действием при значениях рН, близких к рН плазмы крови.
Таким образом, мощность буферных систем плазмы крови уменьшается в ряду:

гидрокарбонатная > белковая > фосфатная > аминокислотная
Эритроциты
Во внутренней среде эритроцитов норме соответствует рН = 7,25. Здесь также действуют гидрокарбонатная и фосфатная буферные системы. Однако их мощность отличается от таковой в плазме крови. Кроме того, в эритроцитах большую роль играет белковая система гемоглобин-оксигемоглобин, на долю которой приходится около 75% всей буферной емкости крови.
Гемоглобин является слабой кислотой ( = 8,2) и диссоци-ирует по уравнению:
= 8,2) и диссоци-ирует по уравнению:
HHb ⇄ H+ + Hb-
При физиологическом значении рН = 7,25 этот описывается уравнением Гендерсона-Гассельбаха:
 ,
,
из которого видно, что:
 .
.
Таким образом, при рН = 7,25 кислота HHb диссоциирована только на 10% и концентрация солевой формы гемоглобина (Hb-) значительно меньше, чем концентрация кислоты (HHb).
Система HHb/Hb- может активно нейтрализовать кислые и основные продукты метаболизма, однако обладает более высокой емкостью по щелочи, чем по кислоте.
В легких гемоглобин реагирует с кислородом. При этом образуется оксигемоглобин HHbО2:
HHb + O2 ⇄ HHbО2,
который переносится артериальной кровью в капиллярные сосуды, откуда кислород попадает в ткани.
Оксигемоглобин - слабая кислота ( = 6,95), но существенно более сильная, чем гемоглобин (
= 6,95), но существенно более сильная, чем гемоглобин ( = 8,2). При физиологическом значении рН = 7,25 кислотно-основному равновесию:
= 8,2). При физиологическом значении рН = 7,25 кислотно-основному равновесию:
HHbО2 ⇄ H+ + HbО2-
соответствует уравнение Гендерсона-Гассельбаха:
 .
.
Отсюда можно заключить, что С(HbО2-)/С(HHbО2) = 2:1 и доля продиссоциировавших молекул HHbО2 составляет примерно 65%.
При добавлении кислот нейтрализовать ионы H+ в первую очередь будут анионы гемоглобина Hb-:
Hb- + H+ ⇄ HHb,
так как они имеют большее сродство к протону, чем ионы HbO2-.
При действии оснований в первую очередь будет реагировать более сильная кислота оксигемоглобин HHbO2:
HHbO2 + OH- ⇄ HbO2- + H2O,
однако и кислота гемоглобин также будет участвовать в нейтрализации поступающих в кровь ионов OH-:
HHb + OH- ⇄ Hb- + H2O.
Система гемоглобин-оксигемоглобин играет важную роль как в процессе дыхания (транспортная функция по переносу кислорода к тканям и органам и удалению из них метаболического СО2), так и в поддержании постоянства рН внутри эритроцитов, а в результате и в крови в целом.
В организме человека все буферные системы взаимосвязаны. Так, в эритроцитах гемоглобин-оксигемоглобиновая буферная система тесно связана с гидрокарбонатной буферной системой. Поскольку внутри эритроцитов рН равен 7,25, то соотношение концентраций соли (НСО3-) и кислоты Н2СО3 здесь несколько меньше, чем в плазме крови. Действительно, из уравнения Гендерсона-Гассельбаха следует, что в эритроцитах C(НСО3-)/С(Н2СО3) = 14:1. Тем не менее, несмотря на то, что буферная емкость этой системы по кислоте внутри эритроцитов несколько меньше, чем в плазме, она эффективно поддерживает постоянство рН.
Фосфатная буферная система играет в клетках крови гораздо более важную роль, чем в плазме крови. Прежде всего это связано с тем, что в эритроцитах содержится большое количество неорганичес-ких фосфатов, главным образом, KH2PO4 и K2HPO4. Кроме того, большую роль в поддержании постоянства рН имеют эфиры фосфорных кислот - главным образом, фосфолипиды, составляющие основу мембран эритроцитов.
Фосфолипиды являются относительно слабыми кислотами. Значения  фосфатных групп находятся в пределах от 6,8 до 7,2. Следовательно, при физиологическом значении рН = 7,25 фосфолипиды мембран эритроцитов находятся как в виде неионизированных, так и в виде ионизированных форм, т.е. в виде слабой кислоты и ее соли. При этом соотношение концентраций соли и кислоты приблизительно составляет (1,5-4):1. Таким образом, сама мембрана эритроцитов обладает буферным действием и поддерживает посто-янство рН внутренней среды эритроцитов.
фосфатных групп находятся в пределах от 6,8 до 7,2. Следовательно, при физиологическом значении рН = 7,25 фосфолипиды мембран эритроцитов находятся как в виде неионизированных, так и в виде ионизированных форм, т.е. в виде слабой кислоты и ее соли. При этом соотношение концентраций соли и кислоты приблизительно составляет (1,5-4):1. Таким образом, сама мембрана эритроцитов обладает буферным действием и поддерживает посто-янство рН внутренней среды эритроцитов.
В случаях, когда буферная и выделительная защита организма исчерпывает свои возможности и развивается тяжелая форма ацидоза (алкалоза), прибегают к медикаментозному подавлению этих наруше-ний. Так, при газовой форме ацидоза внутривенно вводят препараты основного характера, представляющие собой соли слабых кислот: 4%-й раствор NaHCO3, раствор натриевой соли лимонной кислоты - цитрат натрия (Na3Cit) и др., которые нейтрализуют избыточную кислотность, связывая ионы H+ в слабые кислоты:
H+ + HCO3-  H2CO3
H2CO3  H2O + CO2
H2O + CO2
Ликвидацию метаболической формы ацидоза также проводят пу-тем введения солей слабых кислот и других препаратов, обладающих свойством проходить через фосфолипидные мембраны.
При алкалозе вводят растворы слабых кислот, например, 4%-й раствор аскорбиновой кислоты.
Однако перечисленные методы медикаментозного вмешательства не имеют, строго говоря, лечебного эффекта: они позволяют лишь «выиграть время» для более детального установления причин возник-новения отклонений и назначения курса лечения или профилактики.
Date: 2016-11-17; view: 1835; Нарушение авторских прав