
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Классификация причин пороков развития человека (Лазюк Г.И.)
|
|
I. Эндогенные причины (внутренние факторы)
- изменения наследственных структур (мутации): геномные (полиплоидии, трисомии, моносомии, частичные или полные), хромосомные (дупликации, транслокации, инверсии, делеции, кольцевидные хромосомы), генные
- "перезревание" половых клеток
- эндокринные заболевания
- возраст родителей (слишком юный или старый)
II. Экзогенные причины (факторы внешней среды)
- физические факторы: радиационные, механические
- химические факторы: лекарственные вещества, химические вещества, применяемые в быту и промышленности, эндокринные заболевания, гипоксия, неполноценное питание
- биологические факторы: вирусы (вирус краснухи, токсоплазмы, вирус цитомегалии и др.), простейшие.
Эндогенные причины
1. Генные мутации связаны с изменением внутренней структуры отдельных генов и обуславливают превращение одних аллелей в другие. Они могут возникать за счет замены отдельных нуклеотидов в цепи ДНК на
другие, выпадения или вставки отдельных нуклеотидов, их групп или генов. ВПР наследственного характера в большинстве случаев обусловлены генными мутациями.
Хромосомные мутации - изменения структуры хромосом, различимые при помощи светового микроскопа:
- транслокации - обмен сегментами между хромосомами: реципрокные транслокации - две хромосомы взаимно обмениваются сегментами, нереципрокные - сегменты одной хромосомы переносятся в другую, робертсоновские - две акроцентрические хромосомы соединяются своими центромерными районами.
- делеции (p-, q-)- "поломки" хромосом с утратой части ее короткого (p) или длинного (q) плеча. Частой формой делеций являются кольцевые хромосомы (r), которые образуются в результате поломки в обоих плечах хромосомы с последующим замыканием оставшейся структуры в кольцо.
- дупликация - удвоение участка хромосомы
- инверсия - результат двух поломок в одной хромосоме с последующим поворотом участка между поломками на 1800.
Транслокации и инверсии могут быть сбалансированными (ни увеличения, ни уменьшения генетического материала не происходит), несбалансированными. Следствием дисбаланса являются частичная трисомия (трисомия по части хромосомы)(рис.1) или частичная моносомия. Делеции и дубликации всегда несбалансированными, следствием делеций являются частичные момносомии, дупликаций - частичные трисомии.
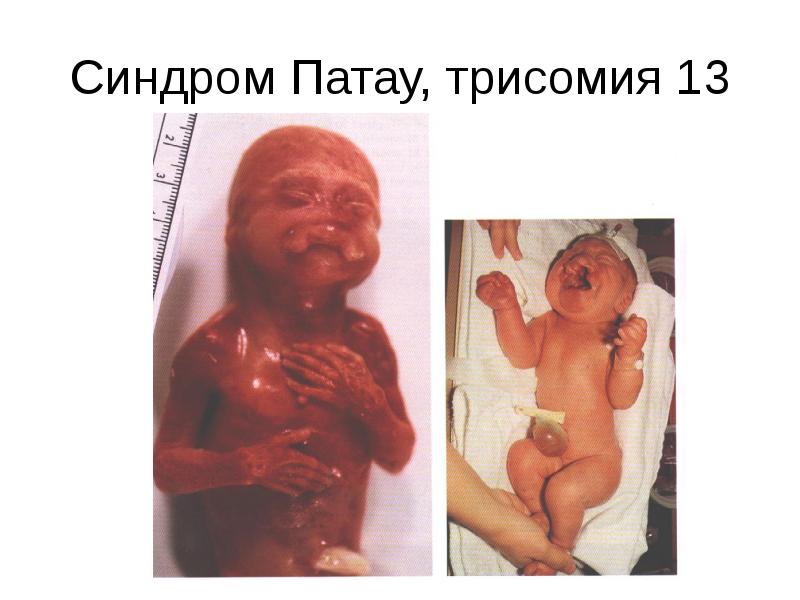
Рис.1. Трисомия 13 – синдром Патау.
Наличие у одного индивидуума нескольких вариантов хромосомного набора называется мозаицизмом.
Удельный вес хромосомных мутаций в происхождении врожденных пороков развития не определен (около 7-8% всех хромосомных болезней вероятно связаны с нарушениями структуры хромосом).
Геномные мутации - изменения количества хромосом. Чаще наблюдаются трисомии) увеличение количества хромосом на одну) или моносомии (отсутствие одной из хромосом). Геномные мутации обычно сопровождаются измнениями фенотипа и приводят к самопроизвольному аборту или хромосомной болезни.
Мутации возникают постоянно как в процессе обычных физиологических функций организма (спонтанный или естественный мутагенез), так и в результате дополнительных воздействий на наследственные структуры физических, химических и биологических факторов (индуцированный мутагенез). Спонтанные мутации обусловлены биохимическими изменениями в клетке, воздействием естественного радиоактивного фона или ошибками репликации. Индуцированные мутации могут быть обусловлены воздействием ионизирующего излучения, многими химическими веществами и вирусами.
2. Различные гормональные расстройства и дефекты метаболизма у беременных нередко приводят к самопроизвольным абортам или нарушениям морфологической и функциональной дифференциации органов плода, определяющим высокую антенатальную и раннюю детскую смертность. Тератогенный эффект в этой группе заболеваний женщин доказан для сахарного диабета, эндемического кретинизма, вирилизирующих опухолей, фенилкетонурии, галактоземии и гистидинемии. Наибольшее значение в клинической практике имеют поражения плода при сахарном диабете I типа и фенилкетонурии.
Диабетическая эмбриопатия проявляется комплексом ВП, из которых 37% приходится на пороки костно-мышечной системы, 24%- на пороки сердца и сосудов, 14%- на пороки ЦНС.
Диабетическая фетопатия проявляется большой массой тела ребенка при рождении, обусловленной главным образом отложением жира в подкожной клетчатке (особенно в области грудной клетки), гиперплазией эндокринной части поджелудочной железы, жировой дистрофией печени, уменьшением запасов гликогена в миокарде, печени и мышцах, микроангиопатиями почек, сетчатки глаза и кожи. В дальнейшем такие дети нередко отстают в умственном развитии.
Причины развития врожденных пороков при диабете не установлены. Большинство исследователей считают, что решающую роль в патогенезе пороков при диабете играют гипогликемия и гипоинсулинемия, в качестве дополнительных факторов - гипоксия, сосудистые расстройства, нарушения обмена жиров и аминокислот.
Фенилаланиновая эмбриопатия развивается у плодов женщин, страдающих фенилкутонурией, или (много реже) у гетерозиготных носителей по гену ФКУ и проявляется спонтанным абортом или при донашивании беременности микроцефалией, пороками сердца(рис.2), пренатальной гипоплазией. В дальнейшем у таких детей развивается умственная отсталость.

Рис.2. Наиболее распространенные врожденные пороки сердца у детей.
Наиболее ярким примером действия "эндогенных" регуляторов тератогенеза являются влияние кортизона и его аналогов на развитие верхней челюсти у мышей. При введении кортизона на 12- й день беременности самкам у всех зародышей формируется волчья пасть, при отсутствии иных морфологических дефектов развития. Формирование волчьей паcти происходит за счет блокирования элевации и сращения отростков. Биохимическими методами установлено два основных типа нарушений метаболизма в небных отростках:
1) торможение синтеза РНК, быстро наступающее вслед за введением кортизона беременной самке
2) торможение синтеза гликозаминогликанов в зачатках. Предполагается, что оба дефекта имеют отношение к возникновению аномалий. Остановку синтеза РНК связывают с блоком митозов и частичной гибелью клеток в отростке, что соответствует морфологическим данным. нарушение синтеза гликозаминогликанов приводит к нарушению формирования хрящевой и соединительной ткани. Остается неизвестным, какое соединение в данном случае является непосредственным триггером тератогенеза: сам гормон или вторичные метаболиты, возникающие под его действием (цикло-3,5-АМФ, полиамины, простагландины и т.д.).
4. Зависимость состояния здоровья потомства от возраста родителей общеизвестна. Учащение рождения детей с ВПР у немолодых родителей обусловлено рядом эндогенных и экзогенных факторов. Ведущее значение имеет старение половых клеток - предшественников яйцеклеток и сперматозоидов и "перезревание" гамет. Старение половых клеток сводится в основном к увеличению частоты мутаций, это связано с тем, что:
1. к концу репродуктивного периода снижается активность различных ферментов и интенсивность обмена веществ, это создает худшие условия для репарации мутационных повреждений в половых клеток. Гормональные расстройства, наблюдаемые у женщин в возрасте старше 35-40 лет, также способствуют "перезреванию" и нарушению плацентации, увеличивается частота декомпенсированных форм сахарного диабета.
2. увеличивается повреждаемость яйцеклеток
3. снижается резистентность хромосом к химическим мутагенам
Экзогенные причины
1. Физические факторы.
Радиационная эмбрио-, фетопатия - комплекс изменений у зародышей после воздействия на них ионизирующим излучением. Последствия такого воздействия зависят от:
- вида ионизирующего излучения (наиболее изучены быстрые нейтроны и рентгеновы лучи)
- суммарной дозы (менее 5 сГр за период органогенеза не индуцирует ВПР)
- срока и длительности воздействия
- индивидуальной чувствительности и др.
Суммарная доза в 10сГр, полученная в период бластогенеза, приводит к прекращению развития, эта же доз в эмбриогенезе может индуцировать пороки развития, а в фетогенезе - пренатальную гипоплазию и функциональные расстройства (преимущественно ЦНС). В общей сложности радиационные поражения зародыша не дают четкого синдрома, а проявляются микроцефалией(рис.3), задержкой психического развития, катарактой, способствуют увеличению детской заболеваемости и перинатальной смертности.

Рис.3. Микроцефалия.
ВП под воздействием ионизирующего облучения могут возникать путем прямого повреждения внутриутробного плода, а также в результате нарушений обмена веществ, ферментативных процессов, нарушения проницаемости клеточных мембран, происходящих в организме облученной женщины.
2. Среди механических факторов, индуцирующих ВПР, известны амниотические сращения, чрезмерное давление матки или опухоли на развивающийся плод при маловодии, сдавление органов плода опухолью или другим неправильно сформированным органом.
3. Среди химических факторов, имеющих определенное значение в происхождении ВП у человека, можно выделить медикаменты, химические соединения, применяемые в быту, промышленности и сельском хозяйстве, гипоксию и неполноценное питание.
При определении тератогенности того или иного химического фактора необходимо учитывать особенности как организма, так и самого фактора. Тератогенный эффект химических факторов зависит от химического строения вещества, его молекулярной массы, дозы и пути введения в организм. Химические соединения с молекулярной массой более 1 000 через неповрежденную плаценту не проникают и не могут быть тератогенами, т.к. для химических тератогенов характерно прямое повреждение клеток эмбриона. Лекарственные вещества и продукты их обмена в большинстве случаев могут проникать через плацентарный барьер.
Из группы транквилизаторов тератогенная активность на эмбрионы человека доказана лишь для талидомида и диазепама. Талидомид - малотоксичный для взрослого организма препарат - введенный в организм женщины на 4-10-й неделе беременности, приводит к развитию синдрома талидомидной эмбриопатии (синдрома Видемана)(рис.4).


 Рис. 4. Талидомид и врожденные пороки развития, как следствие его приема.
Рис. 4. Талидомид и врожденные пороки развития, как следствие его приема.
Проявляется различными формами дисмелий верхних (укорочение руки в целом и предплечья, аплазия и гипоплазия радиальной при нормальной ульнарной кости, аплазия I и II пальцев, гипоплазия I пальца, мышц тенара или трехфаланговый I палец) и нижних конечностей (единая рудиментарная кость между тазом и стопой, гипоплазия бедренной кости, деформация больше- и малоберцовой костей, изолированная деформация стоп, вывих бедра). Мехнизм тератогенного действия талидомида изучен недостаточно и, возможно, первично повреждается эмбриональная нервная ткань.
Тератогенной активностью обладают многие противоопухолевые алкилирующие средства, т.к. в организме эти препараты взаимодействуют с нуклеиновыми кислотами и ферментами, оказывая цитостатическое действие на интенсивно пролиферирующие ткани, какими и являются ткани эмбриона. Однако удельный вес ВП, индуцированных алкилирующими препратами невелик, т.к. число беременных женщин, нуждающихся в противоопухолевом лечении, сравнительно невелико.
Тератогенный эффект может оказать гиперавитаминоз А. Комплекс пороков, индуцируемых изотретиноином (синтетический аналог витамина А), специфичен: как правило, поражется головной мозг (гидро- и микроцефалия, нарушения развития гистологических структур, аплазия и гипоплазия червя мозжечка), наблюдаются микрофтальмия, микротия, анотия, атрезия наружного слухового прохода.
Наиболее изученной формой авитаминоза, вызывающего уродства, является дефицит фолиевой кислоты. В этом случае аномалии зародышей возникают в период органогенеза. Однако пути реализации тератогенного эффекта до сих пор точно не установлены, т.к. первичный дефект уровня коэнзимов в фолатном цикле может вызвать множественные метаболические сдвиги:
- аномалия дифференцировки митохондрий и нарушение дыхательного ресинтеза АТФ
- дефекты дыхательной цепи, биосинтеза фосфолипидов
- сдвиги профиля фермнтов в тканях.
Морфологические методы обнаруживают частичную гибель клеток и остновку митозов в зачатках. Однако никем строго не показано, что именно эти изменения приводят к морфологическим аномалиям.
При хроническом употреблении алкоголя во время беременности в большом проценте случаев рождаются дети с алкогольным синдромом(рис.5). Для синдрома характерна врожденная гипоплазия и постнатальный дефицит роста и массы тела, общая задержка физического и психического развития, умеренно выраженные микро- и гидроцефалия, короткие и узкие глазные щели, узкий скошенный лоб, эпикант, утолщенная с узкой красной каймой верхняя губа, гипоплазия нижней челюсти. Развитие синдрома связывают со снижением в тканях эмбриона и плода фолиевой кислоты, которое развивается под воздействием неполных продуктов метаболизма этанола, в частности - ацетельдегида, длительно циркулирующего в крови, поскольку у плода уровень алкогольдегидрогеназы, метаболизирующей алкоголь, составляет всего 10% от нормы для взрослых. Дозовая зависимость не определена, эффект во многом зависит от индивидуальных особенностей матери и плода.

Рис. 5. Алкогольный синдром у детей(фенотип)
Причинно-следственная связь курения с ВП не установлена, однако известно, что масса новорожденных у курящих женщин ниже, чем у некурящих, чаще разрывы плодных оболочек и преждевременная отслойка плаценты. Пренатальную гипоплазию объясняют прямым воздействием никотина на сосуды матки, а также повышением концентрации карбоксигемоглобина в крови матери.
4. Тератогенный эффект доказан для вирусов краснухи и инклюзионной цитомегалии. Возможен тератогенный эффект вирусов простого герпеса, гриппа, кори, эпидемического паротита, инфекционного гепатита, полиомиелита, ветряной и натуральной оспы, Коксаки. Частота дефектов у плодов зависит от срока беременности, в течение которого произошло заражение. Пораженный плод погибает или рождается с синдромом краснухи, который проявляется пренатальной гипоплазией (недостаток массы тела обычно составляет 15-30%), анемией с тромбоцитопенией, сопровождающейся множественными геморрагиями, увеличением печени, селезенки и врожденными пороками развития.
Вирус цитомегалии обычно поражает плод на 3-4- м месяце и приводит к развитию фетопатий, которые вначале проявляются преимущественно альтеративной, а позднее пролиферативной реакцией тканей внутренних органов. Как следствие альтеративно-пролиферативных процессов развиваются вторичные пороки.
Патогенез ВПР
Пути реализации тератогенных эффектов.
Все виды повреждающих воздействий по первичному механизму можно разделить на две группы:
1) генетические повреждения
2) эпигеномные воздействия через негенетические молекулярные структуры клеток, т.е. все типы нарушений динамики обмена или молекулярных структур на постгенетическом уровне.
Все виды превичных генетических и эпигеномных нарушений при тератогенезе реализуются на одной из шести стадий развития зачатка:
1) нарушение жизнеспособности клеток, 2) нарушение детерминации, 3) нарушение клеточной пролиферации, 4) нарушение дифференцировки, 5) нарушение организации и межклеточных взаимодействий, 6) нарушение миграции клеток и клеточных пластов.
Предполагается, что первичный молекулярный механизм действия тератогена полностью предопределяет клеточную стадию, на которой произойдет реализация повреждения.
Date: 2016-05-25; view: 1605; Нарушение авторских прав