
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Фото 20. Пренатально выявленная катаракта
|
|
обоих глаз
(печатается с любезного
согласия автора —
Dr. Georges Haddad)
являются амниоцентез (вхождение иглой в амниотическую полость с целью получения околоплодных вод) и кордоцентез (вхождение иглой в вену пуповины с целью получения крови плода) (фото 21 и 22).
При обеих методиках через переднюю брюшную стенку, обработанную антисептиками, с использованием местных обезболивающих средств (которые имеют скорее психологическое воздействие на саму пациентку и окружающих, так как толщина наиболее часто используемых для амнио- и кордоцентеза одноразовых игл равна толщине иглы для введения местного анестетика, а раствор анестетика не вводится в миометрий) или без них, под контролем УЗ-луча методом свободной руки или через направляющее устройство в свободный карман околоплодных вод или в пупочную вену вводится стерильная игла размером 20-22G. Иногда для проведения кордоцентеза используют прием «игла в игле», когда после проведения амниоцентеза более толстой иглой конец ее подводится к пуповине, извлекается мандрен, а затем по каналу вводится вторая, более тонкая игла, которая толчком посылается в направлении выбранного участка пуповины, выполняя непосредственно кордоцентез по направляющей, роль которой играет канал более толстой иглы. Вмешательства проводятся амбулаторно или с кратковременной госпитализацией.

|
Глава 4
Фото 21. Игла
в амниотической полости
при амниоцентезе
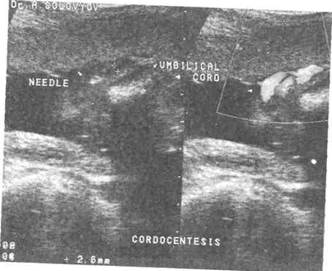
Фото 22. Кордоцентез с одновременным использованием
черно-белого режима и режима цветового допплеровского
картирования. Стрелками указаны пуповина и кончик иглы
в пупочной вене
--------------------------------------- Глава 4 -------------------------------------------
Показанием для проведения инвазивных методов диагностики беременным женщинам из группы высокого риска являются:
— подозрительные серологические данные в ранних сроках беременности (сероконверсия или повышенное содержание IgG, a также наличие IgM-антител), особенно в тех случаях, когда появляются симптомы в виде гриппозной инфекции;
— повышение содержания специфических IgG и появление IgM у женщин, у которых до беременности не определялись серологические признаки перенесенной инфекции;
— наличие у плода УЗ-признаков внутриутробного заражения;
— наличие информированного согласия семьи на проведение внутриматочного вмешательства.
Как правило, при подозрении на внутриутробное заражение плода внутриматочное вмешательство осуществляется не ранее 21-22 недель беременности не столько по техническим причинам получения биологического материала, сколько по причинам повышения надежности полученных лабораторных результатов (см. ниже). И хотя после проведения подобных вмешательств могут встречаться такие грозные осложнения, как хорионамнионит, прерывание беременности, а при кордоцентезе — даже длительное кровотечение с последующей анемизацией и гибелью плода, разрыв артерии пуповины, остановка сердца, общее число осложнений в специализированных перинатальных центрах составляет около 1% от всех проведенных манипуляций. Осложнения наиболее часто встречаются как раз в тех случаях, когда уже имеются какие-либо, патологические состояния плода: дистресс при СЗВУРП, структурные аномалии плода, маловодие, иммунные конфликты, внутриутробное инфицирование.
Для предупреждения развития возможной чувствительности к резус-фактору в некоторых странах, включая страны бывшего СССР, широко рекомендуется применение Rh-иммуноглобулина после инвазивных методов исследования. Но проведенные еще в 1982 году (М. Golbus и соавт., Prenat Diagn) и в 1986 году (A. Tabor и соавт., Br. Med. J.) два больших ретроспективных исследования не выявили увеличения количества случаев изоиммунизации у женщин, не получавших профилактику Rh-иммуноглобулином. Более того, S. Smidt-Jensen и J. Philip, изучая возможные осложнения после амниоцентезов и биопсий ворсин хориона, высказали предположение, что назначение Rh-иммуноглобулина увеличивает частоту самопроизвольного прерывания беременности (Prenat Diagn, 1991).
--------------------------------------- Глава 4 -------------------------------------------
В любом случае внутриматочное вмешательство не является безразличной для организма процедурой, поэтому оно должно выполняться по показаниям и с наличием информированного согласия семьи.
Материалы, полученные в ходе вмешательств, направляются для лабораторных исследований. Поэтому качество инвазивных методов диагностики прежде всего зависит от возможностей лабораторной базы и точности предварительного диагноза. По способности выявления возбудителя инфекции, методы лабораторной диагностики делятся на две группы: прямые, позволяющие выявить в биологических жидкостях или тканях плода вирусы и другие микроорганизмы; непрямые, позволяющие зарегистрировать специфический иммунный ответ плода на воздействие инфекционного агента.
К прямым методам относятся:
— микроскопия (электронная или прямая — например, в темном поле);
— выявление вирусных или бактериальных антигенов (в т. ч. одноэтапными иммуноферментными и иммунохроматографичес-кими методами);
— полимеразная цепная реакция (ПЦР);
— культуральный метод.
Непрямая лабораторная диагностика внутриутробных инфекций, как уже было сказано выше, основана на данных серологических исследований наличия специфических антител IgM и IgA в сыворотке крови плода. Часто применяемым методом выявления антител к инфекционным агентам является метод ELISA (фермент-связывающий иммуно-сорбентный метод).
Цель исследования околоплодных вод и крови плода — выявление возбудителя или специфических IgM и IgA-антител, которые плод в состоянии производить самостоятельно уже с 13 по 20 неделю беременности. Антитела IgM и IgA, в отличие от антител IgG, не передаются трансплацентарно вследствие больших размеров молекулы, поэтому их наличие в крови плода говорит о собственном иммунном ответе плода на попадание возбудителя в свой организм. Для лабораторного определения необходимо накопление достаточной концентрации антител, что обычно происходит не ранее 20-й недели беременности. Поэтому внутриутробные вмешательства необходимо проводить не ранее 22-23-й недели беременности, чтобы снизить вероятность ложноотрицательных результатов. Конечно, серологические исследования могут давать как ложноположитель-ные, так и ложноотрицательные результаты, что связано с техни-
--------------------------------------- Глава 4 -------------------------------------------
ческими возможностями лабораторий, поэтому сочетание прямых и непрямых методов лабораторных исследований значительно повышают точность диагностики.
На примере 98 пренатально выявленных случаев наиболее распространенной внутриутробной инфекции (ЦМВ) Monique Bodeus и соавт. (Prenatal Diagn, 1999) показали, что наибольшая чувствительность (95,5%) культурального и ПЦР-исследования околоплодных вод была получена после 6 недель с момента заражения матери или при проведении диагностического амниоцентеза, начиная с 23-й недели беременности.
В настоящее время отсутствует «золотой стандарт» пренаталь-ной диагностики вирусных инфекций. Но в литературе имеются данные об использовании так называемой ПЦР-обратной записи (Reverse Transcription-PCR, или RT-PCR), которая в пренатальной диагностике плодовой краснухи даже по пробам околоплодных вод показала чувствительность 98% и более, а специфичность — около 100%. Такие высокие показатели достигаются при соблюдении сроков взятия биологического материала в те же предлагаемые сроки беременности — не ранее 22-23-х недель. Также огромное значение имеют условия и способы транспортировки и хранения проб для проведения исследований.
Ранее в англоязычной литературе для обозначения возбудителей внутриутробной инфекции в основном использовался акроним «TORCH» — по первым буквам латинских названий наиболее частых и опасных возбудителей заболеваний. Из англоязычной литературы этот термин перешел в русско- и украиноязычную литературу — как специальную, так и популярную. Широкое использование термина основывалось на том представлении, что основными возбудителями опасных для плода инфекций являются токсоплаз-ма, вирусы краснухи, герпеса и ЦМВ. Такой подход относился и к лабораторной диагностике, основанной на использовании реактивов лишь для определения инфекций так называемой группы «TORCH». Но в связи с открытием множества других возбудителей внутриутробной инфекции, а также в связи с тем, что инфекция вируса простого герпеса не имеет особенностей, присущих другим возбудителям группы «TORCH», в последние годы исследователи и авторы публикаций в той же англоязычной специальной литературе признали акроним «TORCH» архаичным. Из этого следует, что концепции «TORCH» следует избегать. Если есть подозрение на наличие врожденных или перинатальных инфекций, диагностику каждого из возможных инфекционных агентов следует проводить отдельно. Для диагностики используется лишь один образец сыво-
-------------------------------------- Глава 4 --------------------------------------------------------
ротки. Ценность полученных данных нередко бывает Очень низкой (Manual of Neonatal Care. Forth edition. Edited by J.P. Cloherty, A.R. Stark. — Lippincott-Raven Publishers, Philadelphia — New York, 2002).
На практике у нас не существует подходов, позволяющих лабораториям просто получить для работы образец материала, а затем дать ответ с перечнем всех возможно существующих внутриутробно микроорганизмов. То есть теоретически это возможно и может быть результатом проведения значительного объема работ большим научно-исследовательским коллективом, но в клинической практике представляется нереальным. Поэтому перед выполнением каждого вмешательства надо иметь представление оследующем: что именно исследователь хотел бы найти в полученном образце ткани или жидкости; каким из существующих лабораторных методов; в какой лаборатории; имеются ли в данной лаборатории возможности для проведения тех или иных методов диагностики.
Следовательно, определение необходимого и достаточного объема лабораторных исследований для подтверждения предполагаемого диагноза, а также определение источников финансирования этого объема работ являются одними из основных вопросов перед назначением инвазивных методов исследования. Без выполнения необходимого объема исследований может теряться сам смысл проведения внутриматочных вмешательств. Кроме того, следует помнить и объяснять пациентам, что даже в наилучших диагностических условиях отрицательные результаты лабораторных исследований формально не позволяют исключать внутриутробного инфицирования.
Здесь на помощь снова приходят данные анамнеза об особенностях клинических проявлений у матери, о проведенных вакцинациях и о результатах преконцепционных лабораторных исследований, а также данные пренатальных УЗ-исследований. Просеивающие лабораторные исследования, во-первых, малоэффективны по уже рассмотренным причинам, во-вторых, очень затратны. В мировой литературе пока удалось найти лишь одну работу, посвященную изучению экономической целесообразности затрат для проведения рутинного антенатального просеивающего лабораторного исследования антител матерей к вирусу простого герпеса 1 и 2 типа при отсутствии каких-либо проявлений этого заболевания, проведенную Северо-Западным Университетом, Чикаго, США (The cost-effectiveness of routing antenatal screening for maternal herpes simplex virus-1 and -2 antibodies. — Am. J. Obstet Gynecol 192(2):483-488, Febr 2005).
--------------------------------------- Глава 4 -------------------------------------------
Было проведено сравнение трех подходов к диагностике:
1) отсутствие поголовного исследования на герпес (стандарт, существующий ныне в США);
2) поголовное пренатальное исследование как беременной, так и ее полового партнера с последующим консультированием;
3) поголовное пренатальное исследование с необходимым консультированием и профилактическим назначением ацикловира в 36 недель беременности всем серопозитивным женщинам.
Выводы проведенной работы: затраты на поголовное просеивающее исследование вируса простого герпеса при беременности нецелесообразны, так как при 2-м и 3-м подходах экономический эффект, выраженный в виде сохраненного каждого условного года жизни одного ребенка, составил соответственно 219513 и 155988 американских долларов. Следует ожидать появления в будущем подобных работ и в отношении других затратных программ поголовного лабораторного исследования при отсутствии веских клинических и анамнестических данных.
Можно сказать, что, как правило, при отсутствии каких-либо патологических УЗ-признаков (несмотря на то, что во многих случаях УЗ-находки могут быть неспецифическими) получаемые данные лабораторных исследований плода отрицательны. И, наоборот, как правило, при наличии патологических УЗ-признаков, присущих внутриутробным инфекциям, данные лабораторных исследований плода положительны. Так, например, Donner с соавторами сообщает о 16 выявленных методами инвазивных исследований плодах с пренатальной инфекцией среди 52 беременных женщин из группы риска, отобранных по клиническим, лабораторным и УЗ-критериям.
Hogge и соавторы отобрали для инвазивной пренатальной диагностики 8 плодов на основании выявленных признаков внутриутробной инфекции, и у всех восьми внутриутробная инфекция была подтверждена. Lynch с коллегами описывает результаты инвазивных исследований 12 плодов с подозрением на ЦМВ инфекцию, которым проводились амнио- и кордоцентезы. У семи из них не было каких-либо патологических УЗ-находок, хотя у всех семи матерей была документирована первичная ЦМВ-инфекция, лишь один из семи плодов оказался зараженным. У других пяти женщин с документированной первичной ЦМВ-инфекцией все плоды имели те или иные патологические УЗ-признаки, и у всех была подтверждена ЦМВ-инфекция путем определения IgM в крови и околоплодных водах. Twickler и соавторы сообщили о двух случаях врожденной инфекции, и у обоих детей отмечались патологические УЗ-находки.
--------------------------------------- Глава 4 -------------------------------------------
Следовательно, напрашивается вывод об обязательности проведения экспертных УЗ-исследований как перед проведением лабораторных исследований беременных, так и перед назначением внутриматочных вмешательств.
Ниже приводим возможные УЗ-признаки при различных внутриутробных инфекционных поражениях плода, которые могут помочь определиться с объемом лабораторных исследований и с прогнозом жизни и здоровья плода, новорожденного.
При ЦМВ-инфекции могут отмечаться: неиммунная генерализованная водянка плода, вентрикуломегалия, гепатомегалия, спленомегалия, хориоретинит, СЗВУРП, микроцефалия, внутри-мозговые кальцификаты, закрытие овального окна с признаками перегрузки правого сердца, гиперэхогенный кишечник, асцит, иногда — маловодие. Большинство находок определяется уже при сроке около 20 недель. Напоминаем, что врожденная ЦМВ-инфек-ция встречается лишь в 0,2-1,5% всех родов, и только от 5 до 10% инфицированных детей имеют клинические проявления.
При краснухе наиболее частыми УЗ-находками бывают: пороки сердца (особенно дефекты перегородок), глаз (катаракта, микроф-тальмия), микроцефалия, гепатомегалия, спленомегалия, СЗВУРП. Могут встречаться и такие сочетанные аномалии, как ги-поспадия, менингоцеле. Следует обратить внимание, что даже при подтвержденном первичном заболевании матери в I триместре беременности вирусом краснухи заражаются лишь около 50% плодов (Jones KL: Fetal rubella effects. In Smith's Recognizable Patterns of Human Malformation. — Philadelphia, WB Saunders, 1998. — P. 574-575). Другими словами, половина детей, матери которых перенесли краснуху в I триместре беременности, не имеют заболевания краснухой. С другой стороны, обращаем внимание на то, что при краснухе отрицательный ответ о наличии IgM-антител в околоплодных водах и крови плода даже в 22-23 недели беременности не позволяет полностью исключить заболевание плода вследствие возможного недостатка концентрации антител. Поэтому рекомендуется также исследование амниотической жидкости и/или крови плода методом ПЦР или методом ПЦР-обратной записи.
При Varicella Zoster эмбриопатия может развиться вследствие поражения плода в I и II триместрах беременности. Частота материнской инфекции составляет 7:10000. Частота поражения плода составляет от 1 до 20% зараженных беременных женщин. Вирус обладает нейротропностью, непосредственно поражая ткани плода. Наиболее частыми УЗ-признаками могут быть: гибель плода, СЗВУРП, косолапость и аномалии положения кистей плода, огра-
--------------------------------------- Глава 4 -------------------------------------------
ничение движений конечностей, гипоплазия конечностей, хорио-ретинит, катаракта, микрофтальмия, водянка плода, многоводие, гиперэхогенные включения в печени, вентрикуломегалия, микроцефалия. Кроме того, могут встречаться различные сочетанные аномалии других органов и тканей.
УЗ-признаки при поражении вирусом Herpes simplex: СЗВУРП, микроцефалия, гидроцефалия, некроз мозжечка, хориоретинит, катаракта, микрофтальмия, гепатоспленомегалия. Могут встречаться такие сочетанные аномалии, как паховые грыжи и аплазия кожи. На фото 23 можно увидеть матку с придатками в составе грыжевого мешка 2-месячной девочки.
Следует отметить, что даже выделение из околоплодных вод культуры вируса простого герпеса не всегда сопровождается заражением плода. Большинство антенатально пораженных плодов рождается преждевременно.
Токсоплазмоз часто проявляется такими находками, как неиммунная генерализованная водянка плода, гиперэхогенные включения в мозге и в печени плода, цисты головного мозга, гипер-эхогенный кишечник, гепатоспленомегалия, микрофтальмия, анофтальмия, асцит, СЗВУРП. Токсоплазмоз может подтверждаться исследованием околоплодных вод с целью проведения ПЦР либо серологических методов исследования. Следует помнить о том, что эффективных лекарственных препаратов для лечения токео-плазмоза плода сегодня не существует, а применяемые с этой целью препараты вызывают значительные побочные эффекты, незначительно влияя при этом положительно на течение заболевания.
Подозрение о внутриутробном инфицировании парвовирусом В19 должно возникнуть при обнаружении: в I триместре — утолщения воротниковой складки, задержки развития плода; во II триместре — задержки развития плода, водянки плода с наличием/без асцита, плеврального или сердечного выпота, двусторонней водянки яичек, гидроцефалии; утолщения кожи, кардиомегалии, гипертрофической кардиомиопатии, повышенной эхогенности кишечника, микроцефалии, интракраниальных кальцификатов, утолщенного последа, патологического нарушения количества околоплодных вод.
Эмбриопатия при СПИД (врожденный СПИД, СПИД плода, ВИЧ плода) характеризуется группой дисморфических признаков, которые могут проявиться не только после рождения, но и внутриутробно, особенно учитывая тот факт, что большинство случаев трансплацентарного заражения происходит в ранние сроки беременности. Почти 99% детей, зараженных ВИЧ, получили этот ви-
Глава 1
|
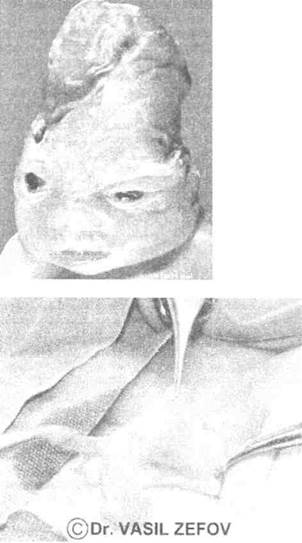
| Фото 23. Лицо плода с внутриутробным поражением Varicella Zoster. Беременность прервана в 26 недель. Обратите внимание на спавшийся череп, неповрежденную кожу, различную степень поражения глаз, уплощенное лицо (печатается с любезного согласия www.TheFetus.net) |
Фото 24. В грыжевом мешке левой врожденной паховой грыжи у 2-месячной пациентки оказалась матка с придатками (печатается с любезного согласия автора — Dr. Vasil Zefov)
--------------------------------------- Глава 4
рус от своих матерей; из них, по данным разных авторов, от 30 до 50% внутриматочно. Возможные УЗ-признаки: гибель плода, СЗВУРП; различные краниофациальные аномалии, включающие микроцефалию, гипертелоризм, короткий нос, плоский выдающийся лоб с возможными боковыми буграми. Кроме того, могут отмечаться признаки сочетанных ВИЧ-инфекций, которые могут быть у матери и которые также поражают плод: токсоплазмоз, пар-вовирус, ЦМВ. Инвазивные методы в этом случае не применяются во избежание возможного заражения еще не инфицированного плода.
Медицина, не являясь наукой точной, почти всегда пользуется понятиями вероятности, специфичности, тенденции и т. д. Поэтому, говоря о возможном внутриутробном инфицировании плода и отдавая себе отчет о серьезности последствий постановки такого диагноза для еще не родившегося ребенка, следует помнить о том, что далеко не всегда заражение матери сопровождается заражением плода. Хотелось бы сделать акцент на том, что при наличии положительных либо сомнительных анамнестических, клинических и лабораторных признаков инфицирования матери, а также при наличии положительных либо сомнительных ультразвуковых и лабораторных признаков инфицирования плода, как правило, плод заражен внутриутробно, и можно ожидать осуществления наихудших прогнозов его жизни и здоровья. Но в случае отсутствия каких-либо положительных или сомнительных ультразвуковых и лабораторных признаков (после проведения инвазивных методов исследования) внутриутробного заражения плода следует делать заключение об отсутствии внутриутробного инфицирования, даже при наличии положительных анамнестических, клинических и лабораторных признаков заражения матери.
Позиция тех, кто настаивает на широком использовании прерывания беременности при подтверждении или даже при предположении (так называемые «контакты в анамнезе») заражения матери, не выдерживает серьезной критики, так как любая беременная женщина в любом сроке беременности может подвергнуться воздействию того или иного повреждающего фактора, способного привести к инвалидизации или гибели ее самой или ее нерожденного ребенка.
Следует помнить, что с юридической точки зрения международного права плод признается ребенком и, являясь пациентом, имеет право на получение медицинской помощи, а его мать имеет право на получение информации о состоянии здоровья своего ребенка. Украина еще 27 сентября 1991 года ратифицировала между-
—----------------------------------- Глава 4 ----------------------------------------------- —
народную Конвенцию прав ребенка, где плод определяется как зачатый, но не рожденный ребенок. В преамбуле этого документа сказано: «Дитина, внаслідок її фізичної і розумової незрілості, потребує спеціальної охорони і піклування, включаючи належний правовий захист як до, так і після народження».
Диагноз внутриутробного заражения плода должен быть выставлен лишь на основании полученных и документированных объективных признаков заражения плода, но не на основании данных заражения матери или подозрений врача. Уместно здесь еще раз привести определение внутриутробного заражения плода: под внутриутробной инфекцией следует понимать установленный факт внутриутробного проникновения к плоду микроорганизмов, при котором в организме плода произошли характерные для инфекционной болезни патофизиологические изменения, выявляемые пренатально.
Большинство случаев предполагаемого внутриутробного инфицирования не сопровождается развитием инфекционного заболевания плода. Никогда не следует забывать о жизнях детей, которые стоят за диагнозом.
Для подтверждения высказанной позиции на цветной вклейке приводим несколько фотографий здоровых детей, рожденных матерями, которые в I триместре беременности перенесли (что было подтверждено анамнестическими, клиническими и лабораторными данными) острое заражение краснухой, ЦМВ, токсоплазмой. Семьи отказались от прерывания беременности; у плодов не было выявлено каких-либо ультразвуковых патологических признаков, наличие патологии также не было подтверждено лабораторными данными в результате проведенных инвазивных методов исследования. Следует задуматься над тем, что эти дети остались в живых лишь благодаря настойчивости родителей, вопреки «заботливым» действующим приказам Министерства здравоохранения и советам врачей.
ЛИТЕРАТУРА
Протоколы диагностики, лечения и профилактики внутриутробной инфекции у новорожденных детей. — 2-е изд., перераб. и доп. — М.: ГОУ ВУНМЦ МЗ РФ, 2002.
Articles. Infections. www.TheFetus.net
Brent Laartz. Viral infections and pregnancy. — 2005, www.emedici-ne.com
------------------------------- Глава 4 ------------------------------
Daffos F., Forestier F„ Capella-Pavlovsky M. et al. (1988) Prenatal management of 746 pregnancies at risk for congenital toxoplasmosis. — N. Engl. J. Med. — 1998. —Vol. 118. — P. 271-275.
Donner C, Liesnard C, Content J. et al. Prenatal diagnosis of 52 pregnancies at risk for congenital cytomegalovirus infection. — Obstet Gynecol. — 1993. — Vol. 82. — P. 481-486.
Hagge WA., Buffone G.J., Hogge J.S. Prenatal diagnosis of cytomegalovirus (CMV) infection: A preliminary report. — Prenatal Diag. — 1993. — Vol. 13. - P. 131-136.
По-Terry L., Terry G.M., Londesborough P. Diagnosis of foetal rubella virus infection by polymerase chain reaction. — J. Gen. Virol. — 1990. — Vol. 7.1. — P. 1607-1611.
Infections in pregnancy / Larry C. Gilstrap III., Sebastian Faro. — 2nd ed. — Willey-Liss, 1997.
Jones K.L. Fetal rubella effects. In Smith's Recognizable Patterns of Human Malformation. — Philadelphia: WB Saunders, 1998. — P. 574-575.
Meer K. Mustafa Hussain: Perinatal infections. Management of perinatal infections. — OOTYPEDICON, 2005. www.pediatriconcall.com
Lynch L., Daffos F. Emanuel et al. Prenatal diagnostic of fetal cytomegalovirus infection // Am. J. Obstet. Gynecol. — 1991. — Vol. 165. — P. 714-718.
Manual of Neonatal Care. — 4th ed. Edited by J.P. Cloherty, A.R. Stark. — Philadelphia-New York: Lippincott-Raven Publishers, 2002.
Monique Bodeus, Corinne Hubinont, Pierre Bernard et al. Prenatal diagnosis of human cytomegalovirus by culture and polymerase chain reaction: 98 pregnancies leading to congenital infection // Prenatal Diag. — 1999. — Vol.4. —P. 314-317.
Muriel Mace, Denis Cointe, Caroline Six et al. Diagnostic value of reverse transcription-PCR of amniotic fluid for prenatal diagnosis of congenital Rubella infection in pregnant women with confirmed primary Rubella infection // J. Clin. Microbiol. — 2004, October. — Vol. 42 (10). — P. 4818-4820.
Pass R.F. Cytomegalovirus infection // Pediatr Rev. — 2002, May. — Vol. 23(5). —P. 163-170.
Sonographische Diagnostik in Gynakologie und Geburtshilfe: Lehrbuch und Atlas; in zwei Banden / Eberhard Merz. — Stuttgart; New York: Thieme. Bd. 2. Geburtshilfe. — 2., neubearb. und erw. Aufl. — 2002. — 576 s.
Stephen F. Thung. William A. Grobman. The cost-effectiveness of routing antenatal screening for maternal herpes simplex virus-1 and -2 antibodies. — Am. J. Obstet. Gynecol. — 2005. — Vol. 192 (2). — P. 483-488.
Tercanli S.. Enders G„ Holzgreve W. Gynakologe. — 1996. — Vol. 29. — P. 144-163.
------------------------------- Глава 4 -----------------------------
Terry G.M., Но Terry L., Warren R.C. et al. First trimester prenatal diagnosis of congenital rubella: a laboratory investigation // Br. Med. J. — 1986. — Vol. 292. — P. 930-933.
The 11-14-week scan. The diagnosis of fetal abnormalities / K.H. Nicolai-des, Neil J. Sebire, Rosalinde J.M. Snijders. — The Parthenon Publishing Group, 2002. — 136 p.
Twickler DM., Perlman J„ Maberry M.C. Congenital cytomegalovirus infection presenting as cerebral ventriculomegaly on antenatal sonography // Am. J. Perinatol. — 1993. — Vol. 10. — P. 404-406.
Ultrasonography in Obstetrics and Gynecology / Edited by Peter W. Cal-len. — 4th ed. — W.B. Saunders Company, 2000. — 468 p.
ГЛАВА 5
ВРОЖДЕННЫЕ ИНФЕКЦИИ
В. К. Чайка, Н.Я. Жилка, Н.В. Сурина, Н.А. Фирсова, Б.А. Иотенко,
И.В. Новикова, Н.Н. Шемякина, СМ. Корниенко, В.А. Каверина,
О.Н. Роговая, Ю.А. Батман, Д.А. Бессонов, Н.Г. Михно,
Г. В. Мещеринова, А. И. Соловьев, Р. Г, Бичевская
5.1. ТОКСОПЛАЗМОЗ
Токсоплазмоз — заболевание, вызываемое простейшими Тохо-plazma gondii у животных и человека. Бессимптомное носительство Toxoplazma gondii широко распространено, тогда как токсоплазмоз, как заболевание, встречается относительно редко.
Частота заражения людей Toxoplazma gondii с возрастом увеличивается и зависит от климатических условий, привычек. В центральной Европе количество случаев заражения в детородном возрасте возрастает с 32% у 20-летних, до 48% у 40-летних. Нет значительной разницы в частоте инфицирования женщин и мужчин. По географическим регионам серопозитивных к Toxoplazma gondii людей меньше в странах с холодным климатом и значительно выше в странах с тропическим климатом. Например, низкий уровень инфицирования токсоплазмой отмечается на Аляске, тогда как на Таити и Тринидаде он высок.
Примерно 1/3 взрослого населения имеет серопозитивные серологические тесты к Toxoplazma gondii, что говорит о перенесенной в прошлом инфекции. Первичное инфицирование Toxoplazma gondii в первую очередь представляет опасность для иммуносупрессив-ных пациентов и для беременных.
--------------------------------------- Глава 5 --------------------------------------------
По данным мировой статистики, ежегодно примерно у 0,6% женщин репродуктивного возраста выявляется первичная инфекция, и в этом случае возможна ее передача от матери плоду. Инфекция плода приводит к воспалительным повреждениям мозга, сетчатки и хориоидной оболочки глаза, что может быть причиной необратимого неврологического нарушения и повреждения зрения. Диссеминированная инфекция редко становится причиной гибели плода или новорожденного. Около 1-10 на 10 тысяч детей появляются на свет с врожденным токсоплазмозом.
Как предотвратить симптомы и инвалидность в результате врожденного токсоплазмоза? Этот вопрос вызывает противоречивые мнения среди врачей на протяжении последних лет. Центральным объектом дебатов является эффективность пренатального лечения, основанного на риске врожденного токсоплазмоза, а также пренатального и постнатального лечения.
Этиология
Toxoplazma gondii — облигатные внутриклеточные паразиты; встречаются повсеместно. Переносчиком инфекции являются животные. Из домашних животных только кошки могут инфицировать человека. Другие домашние животные (например, собаки, морские свинки и птицы) могут инфицироваться токсоплазмой, однако в их организме возбудитель не проходит инфекционной стадии, и поэтому они не могут инфицировать человека при контакте.
Toxoplazma gondii существуют в трех формах:
— трофозоиты или пролиферативная форма;
— тканевые цисты;
— ооцисты.
В клетках кишечника кошек происходит половое размножение паразита с образованием ооцист. Пик продуцирования ооцист приходится на 5-8 сутки после инфицирования. С фекалиями кошек выделяется более 10 млн ооцист в течение 1—3 дней. Ооцисты ток-соплазмы относительно резистентны к неблагоприятным условиям окружающей среды. При благоприятных условиях (достаточной влажности, невысокой температуре) они могут сохраняться в земле в течение года. Ооцисты являются единственно свободной формой токсоплазмы — они содержат зиготы, которые еще не завершили цикл своего развития и поэтому еще не способны инфицировать. После созревания в земле (около недели) ооцисты попадают алиментарным путем в кишечник промежуточных хозяев — различных млекопитающих, в том числе и человека, где под влиянием
--------------------------------------- Глава 5 --------------------------------------------
протеолитических ферментов активно проникают в эпителиальные клетки слизистой оболочки и начинают быстро размножаться.
Трофозоиты обусловливают острую фазу инфекции, в течение которой поражаются все виды клеток организма млекопитающего после внедрения в организм хозяина.
Следующая форма паразитов называется «брадизоит». Брадизо-иты образуют цисты. В тканях паразиты могут существовать в двух формах: цисты и псевдоцисты.
Настоящие цисты — это длительная форма существования паразита.
Тканевые цисты могут содержать 90-3000 организмов. Мозг, скелетная или сердечная мускулатура — наиболее типичные места скопления цист, поддерживающие латентную стадию инфекции.
После высвобождения паразитов из цист наступает фаза парази-темии (может быть как у животных, так и у человека). Паразите-мия всегда характеризует острую фазу.
Через зараженную фекалиями котов почву инфицируются грызуны и птицы, которые, в свою очередь, могут реинфицировать котов, и цикл замыкается. Травоядные животные (овцы, козы, свиньи и крупный рогатый скот) могут также инфицироваться через почву, содержащую ооцисты токсоплазм.
Пути инфицирования человека:
1. Через мясо, содержащее цисты токсоплазмы, прошедшее недостаточную кулинарную обработку.
2. Через фекалии котов, содержащие ооцисты токсоплазмы.
3. Трансплацентарно.
4. Гемотрансфузионно (переливание инфицированной крови).
5. При употреблении немытых овощей или загрязненной воды.
Нет доказательств заражения человека человеком, исключая
трансплацентарный и гемотрансфузионный пути.
Date: 2016-05-15; view: 510; Нарушение авторских прав