
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Методы синтеза алкенов
|
|
Алкены могут быть получены реакциями отщепления (элиминирования) из различных функциональных производных и гидрирования из ацетиленовых углеводородов.
Получение алкенов отщеплением может быть представлено общей схемой:

Здесь X=Y=H, Hal; X=H, Y=Hal, OH
1. Дегидрирование алканов. Алкены от С2 до С4 получают дегидрированием алканов. Например, при дегидрировании бутана образуются бутены. В качестве катализаторов используют оксиды металлов:

2. Крекинг (расщепление) алканов приводит к смеси алкенов:

3. Дегалогенирование вицинальных дигалогенидов:
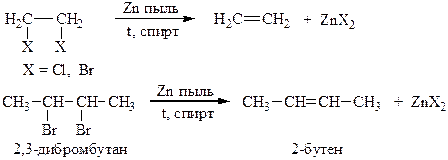
4. Дегидрогалогенирование алкилгалогенидов. В реакции дегидрогалогенирования используют третичные, вторичные и первичные галоидные алкилы. Реакцию проводят в среде этилового спирта в присутствии основания (КОН, NaOH) или при действии третбутилата калия в ДМСО:

Например:


Направление реакции определяется относительными скоростями конкурирующих реакций.

Чем устойчивей алкен, тем легче он образуется в реакции дегидрогалогенирования. Относительная скорость образования алкенов:
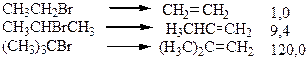
Реакционная способность алкилгалогенидов уменьшается в порядке третичный > вторичный > первичный.
Ряд легкости образования алкенов:
R2C=CR2 > R2C=CHR > R2C=CH2 > RHC=CHR > RHC=CH2
Механизм дегидрогалогенирования Е1:
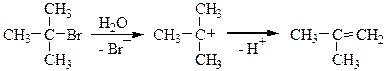
Реакция включает две стадии: первоначально происходит диссоциация связи углерод – галоген с образованием карбкатиона, а затем быстро отщепляется протон, и образуется двойная связь.
Механизм дегидрогалогенирования Е2:

Процесс происходит согласованно, в одну стадию. Галоген отщепляется с парой электронов s-связи в виде аниона, а водород отрывается гидроксид-анионом с образованием молекулы воды. Оставленная водородом пара электронов образует p-связь.
Откуда берется энергия для разрыва связи С-Н и С-Hal?
1. За счет образования связи Н-ОН
2. За счет образования p-связи (60 ккал)
3. За счет энергии сольватации ионов.
Ионные реакции проходят в растворах. Ион водорода вытягивается из молекулы гидроксид-ионом, ион галогена сольватируется молекулами растворителя.
5. Дегидратация спиртов (в присутствии серной или 85%-ной фосфорной кислот):

Легкость реакции дегидратации изменяется в ряду третичные > вторичные > первичные спирты.
Примеры:


Механизм дегидратации спирта Е1
Кислотно – основное равновесие по Бренстеду – Лоури:
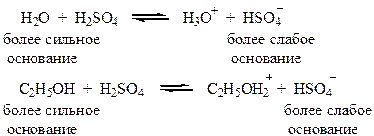
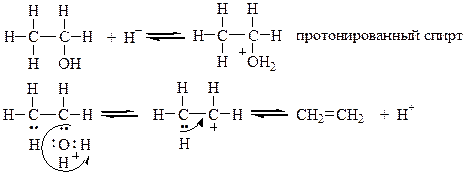
Равновесные реакции сдвигаются в сторону образования алкена при отгонке его из реакционной среды.
Образование карбониевого иона по механизму Е1 происходит в результате отщепления воды от протонированного спирта. Это энергетически более выгодно, чем отрыв гидроксид – аниона от спирта:

Далее происходит отщепление протона. Пара электронов, оставленная водородом, образует p-связь между атомами углерода.
Устойчивость карбониевых катионов

Энергия, необходимая для отрыва электрона от молекулы или атома, называется потенциалом ионизации DН (табл. 3.1).
Таблица 3.1
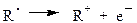
| DН – потенциал ионизации (ккал/моль) |

| DН = 230 |
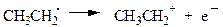
| DН = 202 |

| DН = 182 |
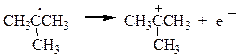
| DН = 171 |
Сверху вниз в таблице потенциалы ионизации уменьшаются, а устойчивость катионов увеличивается. Устойчивость заряженной системы повышается при распределении заряда.
Алкильные группы по сравнению с водородом имеют тенденцию смещать электронную плотность вдоль связи по направлению к электронодефицитным центрам. Смещая электронную плотность, алкильные группы приобретают небольшой положительный заряд, и, следовательно, заряд, первоначально сконцентрированный на одном атоме, оказывается распределенным по молекуле. Таким образом, увеличение числа алкильных заместителей у катионного центра стабилизирует катион:

Один и тот же элемент может обладать различными индуктивными эффектами в зависимости от его состояния гибридизации. По сравнению с Н или С-sp3 – заместителями индуктивные эффекты С – sp2 и С – sp дестабилизируют карбкатион:

Устойчивость карбониевого иона зависит, главным образом, от электронодонорного или электроноакцепторного характера заместителей. Чем устойчивей карбониевый ион, тем легче он образуется. Рассмотрим переходное состояние при образовании карбониевого иона:

В переходном состоянии атомы углерода и кислорода имеют частичные положительные заряды (d+). Группы, подающие электроны, стремятся погасить частичный положительный заряд, имеющийся на атоме углерода, и тем самым стабилизируют переходное состояние. Стабилизация переходного состояния понижает энергию активации и вследствие этого ускоряет реакцию.
Таким образом, тот же самый фактор подачи электронов, который стабилизирует ион карбония, также стабилизирует переходное состояние при образовании карбониевого иона. Более устойчивый ион карбония образуется быстрее:
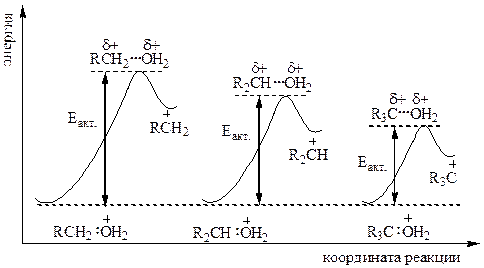
Перегруппировка ионов карбония:
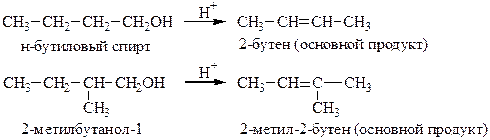
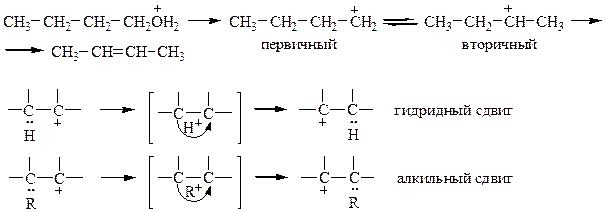
Ион карбония может отщеплять протон с образованием алкена, а также перегруппировываться в более устойчивый карбкатион.
Изомерный состав продуктов в реакциях дегидрогалогенирования и дегидратации находится в соответствии с правилом Зайцева: протон отщепляется от углерода с наименьшим числом водородных атомов, т.е. вторичные или третичные галоиды и спирты при отщеплении образуют олефины с наибольшим числом алкильных групп при кратной связи.
Правило Зайцева объясняет существование наиболее замещенного, термодинамически более устойчивого алкена.
Дегидрогалогенирование алкилгалогенидов и дегидратация спиртов - важнейшие реакции получения алкенов.
6. Восстановление алкинов. Выбор метода восстановления позволяет получить либо цис-, либо транс-изомеры. Так, например, использование катализаторов Линдлара (Pb, PbO и CaCO3) позволяет получить цис-изомер:
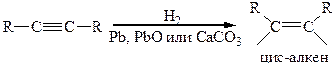
Восстановление натрием или литием в жидком аммиаке или этиламине приводит к транс алкенам:
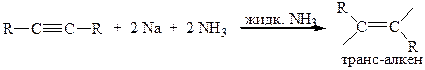
Date: 2016-02-19; view: 2166; Нарушение авторских прав