
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Скорость реакции
|
|
Как правило, химические реакции протекают в несколько стадий, и для того, чтобы верно определить скорость определяющей стадии реакции, необходимо знать механизм реакции.
Суммарный процесс взаимодействия метана с хлором описывается следующим брутто - уравнением:

На самом деле реакция проходит через ряд стадий (табл. 2.1).
Таблица 2.1
| Стадия | Реакция | Название стадий реакции |
| А | 
| инициирование цепи |
| Б | 
| рост цепи |
| В | 
| |
| Г | 
| обрыв цепи |
На каждой из стадий либо поглощается, либо выделяется энергия.
Стадия А: DН = +58 ккал/моль - тепло поглощается.
Стадия Б: DН = -1 ккал/моль - тепло выделяется.
Стадия В: DН = -23ккал/моль - тепло выделяется.
Стадия Г: DН = - 58 ккал/моль - тепло выделяется.
Суммарная энергия (теплота реакции) DНреакции = -24 ккал/моль.
Кравновесия = 1018.
В табл. 2.2 приведены теплоты реакции галогенирования по стадиям для F, Cl, Br, I.
Таблица 2.2
| Стадия | Реакция | Теплота реакции, ккал/моль | |||
| F | Cl | Br | I | ||
| А | 
| +37 | +58 | +46 | +36 |
| Б | 
| -33 | -1 | +15 | +31 |
| В | 
| -71 | -23 | -21 | -17 |
| Г | 
| -37 | -58 | -46 | -36 |
| DНсумм | -104 | -24 | -6 | +14 |
Легкость взаимодействия галогенов с метаном (а следовательно, и скорость реакции) убывает в следующем ряду: F > Cl > Br > I. Как видно из данных приведенной выше таблицы, относительные скорости согласуются с суммарными значениями DН всего процесса.
Энергетические профили для стадий роста цепи при хлорировании и бромировании имеют следующий вид:

Переходное состояние (ПС) - максимум на энергетической диаграмме реакции. Группа атомов, участвующая в переходном состоянии, называется активированным комплексом.
В заключение можно сказать, что скорость галогенирования определяется скоростью первой стадии роста цепи, поскольку именно на этой стадии мы сталкиваемся с энергетическими барьерами (высокие значения Е), которые затрудняют бромирование и препятствуют иодированию.
2. Нитрование. Нитрование - реакция замещения атома водорода на нитрогруппу (NO2).
Нитрование может быть жидкофазным (М.И. Коновалов) и парофазным (Хесс, 1936-1937). В первом случае реакцию проводят с использованием 10 – 12% раствора азотной кислоты при 110 - 140°С, во втором случае температуру повышают до 350 - 400°С.
Общая схема реакции:
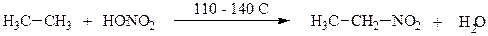
Свободнорадикальный механизм нитрования алканов:

Состав продуктов нитрования, так же, как и в случае галогенирования, определяется относительной активностью различных С-Н связей.
Парофазное нитрование углеводородов, как, например, бутана, сопровождается расщеплением углеродной цепи:
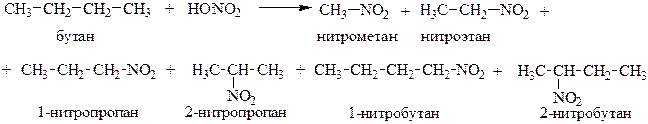
3. Сульфохлорирование. Сульфохлорирование алканов протекает по цепному радикальному механизму при УФ – облучении:

Механизм реакции:

Обрыв цепи происходит при взаимодействии радикалов. Следует отметить, что третичный атом замещению на сульфохлоридную группу не подвергается, вероятно, из-за пространственных эффектов. Однако если в молекуле есть вторичные и первичные углеродные атомы, то замещение протекает в первую очередь у вторичного.
Реакции окисления
Углеводороды - источник энергии. При полном сгорании углеводородов в избытке кислорода образуются углекислый газ и вода, а также выделяется тепло (Q - теплота сгорания)
CnH2n+2 + изб. О2 ¾® n CO2 + (n + 1) H2O + Q
Пример:
С5Н12 + 8 О2 ¾® 5 СО2 + 6 Н2О + 845 ккал/моль
Q = 845 ккал/моль
Реакция полного окисления (сгорания) алканов используется в двигателях внутреннего сгорания, поэтому расчет теплового эффекта этого процесса весьма важен.
Теплота сгорания Q – это теплота реакции сгорания углеводорода. Для ее расчета необходимо знать теплоту образования исходных алканов.
Date: 2016-02-19; view: 986; Нарушение авторских прав