
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Обработка результатов химического анализа подземных вод
|
|
Пример обработки химического анализа подземных вод.
Результат химического анализа воды
| Сухой остаток, мг/л | рН | Температура, 0 С | Содержание основных ионов, мг/л | |||||
| НСО3- | SO42- | Cl- | Na+ | Ca2+ | Mg2+ | |||
| 7.6 |
Обработка химического анализа проводится в следующем порядке.
1) Рассчитаем эквивалентное содержание ионов.
Данные анализа пересчитываем из мг/л в мг-экв, используя пересчетные коэффициенты в табл. 5. Например, содержание в воде гидрокарбонат-иона равно:
930 х 0,0164 = 15,25 мг-экв
2) Выражаем химический состав воды в %-экв форме, приняв суммы анионов и катионов за 100 % каждую и записываем полученные данные в таблицу:
Химический состав воды
| Анионы | Содержание | Катионы | Содержание | ||||
| мг/л | мг-экв | %-экв | мг/л | мг-экв | %-экв | ||
| НСО3- | 15,25 | Na+ | 4,05 | ||||
| SO42- | 1,58 | Ca2+ | 9,68 | ||||
| Cl- | 0,68 | Mg2+ | 3,70 | ||||
| Итого | 17,51 | Итого | 17,43 |
3) Напишем формулу Курлова и название воды.
M1.0 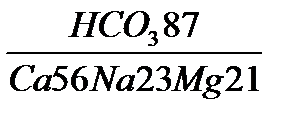 рН7,6 t012
рН7,6 t012
По этой записи воду можно назвать пресной (табл. 7), гидрокарбонатной магниево-натриево-кальциевой, слабощелочной (табл. 8), холодной (табл. 9).
4) Вычисляем виды жесткости и оценим степень жесткости.
Общую жесткость определяем как сумму катионов кальция и магния, выраженных в мг-экв/л: 9,68 + 3,70 =13,38 мг-экв/л. По этому показателю – вода жесткая (табл. 10). Карбонатная жесткость определяется по содержанию гидрокарбонат-иона. В нашем случае НСО3- =15,25 мг-экв/л > Са2+ + Мg2+ = 13,38 мг-экв/л, карбонатная жесткость равна общей, а некарбонатная (остаточная) жесткость отсутствует. Данная вода согласно табл. 10 – очень жесткая.
5) Определяем виды агрессивности по СНиП 2.03.11-85 «Защита строительных конструкций от коррозии» (табл. 11,12,13), данные заносим в таблицу:
| Тип цемента | Вид агрессивности | Степень агрессивности к бетону |
| Любой цемент | Выщелачивающая НСО3- | неагрессивная |
| Общекислотная рН | неагрессивная | |
| Углекислая СО2 | неагрессивная | |
| Магнезиальная Мg2+ | неагрессивная | |
| Сульфатная SO42- | неагрессивная |
Date: 2015-04-23; view: 1319; Нарушение авторских прав