
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Физические свойства. Идентификация органических соединений
|
|
Идентификация органических соединений.
Разнообразие и свойства белков, жиров, углеводов»
Ученицы 10-А класса
УВК ОШ 1-2 ступеней – МТЛ
Колмычек Анастасии
Цель работы: углубление и закрепление знаний об органических веществах, относящихся к классам белков (протеинов), жиров и углеводов; развитие организационных, технических и интеллектуальных умений учащихся; воспитание интереса к химическому эксперименту и к самостоятельному получению знаний.
С правилами техники безопасности ознакомлена и обязуюсь выполнять!
Жиры
Жиры – это гидрофобные соединения, относящиеся к группе липидов; являются сложными эфирами глицерина и высших жирных кислот. Насыщенные (твердые) жиры содержатся в мясе, сале, креветках, яйцах (желток), молоке, шоколаде, сыре, в кокосовом и сливочном масле. Ненасыщенные (жидкие) жиры содержатся в мясе птицы, рыбы, в оливках, миндале, грецких орехах. А также в подсолнечном, льняном, оливковом, соевом и арахисовом масле.
Оборудование и реактивы: бумажные салфетки, сливочное масло, растительное масло, 2-3 семечки, пипетка, ложечка, несколько стеклянных баночек, вода, медицинский спирт, ацетон, бензин, сувенирные эфирные масла, фотоаппарат.
Опыт № 1
| Беру | Делаю | Наблюдаю |
| Бумажную салфетку, 2 семечки, сливочное и растительное масло | Ложу семечку на одну салфетку, кусочек сливочного масла – на другую, капаю пипеткой каплю растительного масла. Сворачиваю салфетки вдвое и прижимаю пальцами. | На каждой из салфеток остались жирные пятна. |
В данных продуктах содержатся жиры, поэтому на салфетках появились жирные пятна. В семечках и маслах содержатся растительные и животные жиры.
Свойства жиров: вязкие жидкости или твердые вещества, легче воды, не имеют четко выраженной температуры плавления; не растворяются в воде, но растворяются во многих органических растворителях. Жиры легко окисляются под воздействием различных факторов: кислорода, температуры, света, ферментов. Прогоркшие жиры имеют неприятный запах, их цвет меняется, ухудшаются органолептические свойства. Чем больше в состав жира входит насыщенных жирных кислот, тем труднее он расщепляется в организме пищеварительными ферментами. Твердые жиры состоят из триглицеридов предельных кислот (пальмитиновой C15H31СООН, стеариновой C17H35СООН), а жидкие – из триглицеридов непредельных кислот (олеиновой C17H33СООН, линоленовой C15H29СООН).
CH2-O-CO-C17H35
I
CH-O-CO-C17H35
I
CH2-O-CO-C17H35
Тристеарат (твердый)
CH2-O-CO-C17H33
I
CH-O-CO-C17H33
I
CH2-O-CO-C17H33
Триолеат (жидкий)
Опыт № 2
| Беру | Делаю | Наблюдаю |
| Три стеклянных стакана. Один – с водой, второй – с ацетоном, а третий – с бензином. Растительное масло. | В каждый стакан с помощью пипетки добавляю по капле растительного масла. Перемешиваю содержимое. | Масло растворилось лучше всего в бензине, немного хуже – в ацетоне и не растворилось в воде. |
Наблюдения доказали свойства жиров: хорошо растворяются во многих полярных и неполярных растворителях (эфирах, бензине, хлороформе), ограниченно растворяются в спиртах, нерастворимы в воде.
Опыт № 3
| Беру | Делаю | Наблюдаю |
| Эфирные растительные масла (пихтовое, сосновое, розмариновое, эвкалиптовое). Стаканы с горячей водой. | В каждый стакан капаю 1-2 капли масла. | Появился приятный аромат, оказывающий расслабляющее действие. |
Эфирные масла – пахучая смесь жидких летучих веществ, выделенных из растительных материалов. В состав этих веществ входят терпены, кетоны, эфиры, альдегиды и др. Бывают разные эфирные масла. Например, пихтовое, сосновое, розовое, шалфейное, лавандовое, цитрусовое, а также масло ромашки и жасмина.
Эфирные масла широко используются в медицине. Они обладают широчайшим спектром биологической активности, проявляют бактерицидные, противовоспалительные, мочегонные и отхаркивающие свойства.
Пахучие свойства эфирных масел определяют преимущественное использование их для создания ароматных композиций. Состав этих композиций часто очень сложен. Важнейшими современными направлениями запаха в парфюмерии являются цветочный (так называемых белых цветов), «восточный», овощной и их комбинации. Эфирное масло иланг-иланга получают из свежих цветов, собранных летом, методом водной или паровой дистилляции, в несколько этапов.
После первого этапа получается сорт Extra или Bourbon - высший сорт эфирного масла иланг-иланга, весьма популярный и ценимый в парфюмерии.
Опыт №4
Углеводы (сахара)
Углеводы – это органические соединения, состоящие из трех элементов – карбона, гидрогена, оксигена. Моносахариды и дисахариды (глюкоза, фруктоза, сахароза) имеют сладкий вкус и растворимы в воде. Полисахариды (крахмал, целлюлоза) обладают другими свойствами. Углеводы – мощный энергетический источник обеспечения жизнедеятельности организмов. Углеводы широко распространены в природе.
Оборудование и реактивы: сахароза, картофельный крахмал, спиртовой раствор йода, пипетка, ложечка, несколько стеклянных банок, вода, электрочайник, кусочек белого хлеба, фотоаппарат.
Опыт №1
| Беру | Делаю | Наблюдаю |
| Сахар. Стакан с горячей и холодной водой. | Добавляю в каждый стакан сахар и размешиваю. | В горячей воде сахар растворяется лучше. |
Сахароза C12H22O11 — дисахарид из группы олигосахаридов, состоящий из двух моносахаридов — α-глюкозы и β-фруктозы..Сахароза является весьма распространённым в природе дисахаридом, она встречается во многих фруктах, плодах и ягодах. Особенно велико содержание сахарозы в сахарной свёкле и сахарном тростнике. Сахароза лучше растворяется в горячей воде.
Физические свойства: она представляет собой бесцветные кристаллы сладкого вкуса, хорошо растворима в воде, температура плавления сахарозы 160 °C, при застывании расплавленной сахарозы образуется аморфная прозрачная масса – карамель.
Химические свойства:
Сахароза имеет более сложное строение, чем глюкоза. Молекула сахарозы состоит из соединенных друг с другом остатков глюкозы и фруктозы. Наличие гидроксильных групп в молекуле сахарозы легко подтверждается реакцией с гидроксидами металлов. Если раствор сахарозы прилить к гидроксиду меди (II), образуется ярко-синий раствор сахарата меди. Альдегидной группы в сахарозе нет: при нагревании с аммиачным раствором оксида серебра (I) она не дает «серебряного зеркала», при нагревании с гидроксидом меди (II) не образует красного оксида меди (I) Сахароза является важнейшим из дисахаридов. Реакция сахарозы с водой.
При кипячении раствора сахарозы появляются молекулы с альдегидными группами, которые и восстанавливают гидроксид меди (II) до оксида меди (I). Эта реакция показывает, что сахароза при каталитическом действии кислоты подвергается гидролизу, в результате чего образуются глюкоза и фруктоза:
С12Н22О11 + Н2О -> С6Н12O6 + С6Н12O6.
Опыт №2
| Беру | Делаю | Наблюдаю |
| Крахмал. Полстакана холодной воды. | Добавляю в стакан крахмал и мешаю. | Не растворяется в воде. |
Физические свойства
Крахмал – это белый безвкусный порошок, нерастворимый в холодной воде и образующий коллоидный раствор (крахмальный клейстер) в горячей воде. Существует в двух формах: амилоза – линейный полимер, растворимый в горячей воде, амилопектин – разветвлённый полимер, не растворимый в воде, лишь набухает.
2. Нахождение в природе
Крахмал (C6H10O5)n – основной источник резервной энергии в растительных клетках – образуется в растениях в процессе фотосинтеза и накапливается в клубнях, корнях, семенах
6CO2 + 6H2O свет, хлорофилл → C6H12O6 + 6O2
nC6H12O6 → (C6H10O5)n + nH2O
глюкоза крахмал
Содержится в клубнях картофеля, зёрнах пшеницы, риса, кукурузы. Гликоген (животный крахмал), образуется в печени и мышцах животных.
Опыт №3
| Беру | Делаю | Наблюдаю |
| Кастрюля с горячей водой. Коллоидный раствор крахмала в холодной воде. | Выливаю в горячую воды раствор крахмала. Все время помешиваю жидкость. | Через некоторое время образуется клейстер – прозрачный студенистый гель. |
В холодной воде крахмал нерастворим, в горячей зерна его набухают и образуют густую жидкость — крахмальный клейстер.
Опыт №4
| Беру | Делаю | Наблюдаю |
| Крахмальный клейстер. Белый хлеб. Стакан с холодной водой. Спиртовой раствор йода. | В стакан капнули раствор йода и размешали. Капнули приготовленный раствор йода на клейстер и хлеб. | Образуется сине-фиолетовое окрашивание. |
Это качественная реакция на крахмал. При взаимодействии йода с крахмалом образуется соединение включения (клатрат) канального типа. Клатрат – это комплексное соединение, в котором частицы одного вещества внедряются в кристаллическую структуру «молекул-хозяев». В роли «молекул-хозяев» выступают молекулы амилозы, а «гостями» являются молекулы йода. Молекулы йода располагаются в канале спирали диаметром ~1 нм, создаваемой молекулой амилозы. Попадая в спираль, молекулы йода испытывают сильное влияние со стороны своего окружения (ОН-групп), в результате чего увеличивается длина связи I–I. Данный процесс сопровождается изменением бурой окраски йода на сине-фиолетовую.
Опыт №5
Крахмал, как полисахарид, состоит из множества остатков глюкозы. Поэтому под действием растворов щелочей, кислот или ферментов крахмал подвергается гидролизу. Ступенчатый ферментативный гидролиз крахмала начинается еще в ротовой полости под воздействием ферментов слюны (амилазы и мальтазы).
| Беру | Делаю | Наблюдаю |
| Небольшой кусочек хлеба. | Тщательно пережевываю в течении минуты. | Почувствовала сладкий вкус. |
Крахмал подвергается кислотному гидролизу, который протекает ступенчато и беспорядочно. При расщеплении он сначала превращается в полимеры с меньшей степенью полимеризации – декстрины, потом в дисахарид мальтозу, и в итоге – в глюкозу. Таким образом, получается целый набор сахаридов.
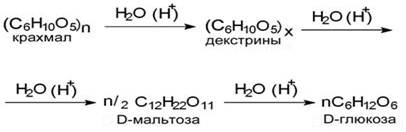
Или краткая форма записи уравнения:
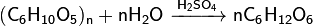
Белки (протеины)
Белки – азотсодержащие биополимеры, состоящие из остатков аминокислот, связанных пептидной связью. В органике белки выполняют множество функций, включая структурную и ферментативную. Под действием различных факторов белки подвергаются денатурации. Белки – это незаменимая часть пищи. Основные источники полноценного белка – продукты животного происхождения.
Оборудование и реактивы: сырое куриное яйцо, клубень сырого и вареного картофеля, раствор перекиси водорода, разбавленный раствор йода, спички, ватные палочки, крахмальный клейстер, бинт, ножницы, столовый нож, пинцет, лист белой бумаги, пипетка, ложечка, стеклянные баночки, вода, электрочайник, фотоаппарат.
Опыт №1
| Беру | Делаю | Наблюдаю |
| Куриное яйцо, два стакана: один – пустой, второй – с водой. | Разбиваю в стакан яйцо. Отделила белок от желтка и налила в стакан с водой. Размешала. | Белок образует коллоидный раствор. |
Date: 2015-05-09; view: 1307; Нарушение авторских прав