
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

При преобразовании работы в теплоту и теплоты в работу
|
|
Преобразование механической работы в теплоту наглядно иллюстрируется необратимым процессом трения. Так, если при механическом взаимодействии двух тел с одинаковой температурой Т1есть трение, то эта работа трения преобразуется в теплоту трения – Lтр=Qтр>0. Эта теплота будет воспринята каждым из тел (Qтр=Qтр1+Qтр2), следовательно, возрастет энтропия каждого тела, а соответственно и всей системы.
Увеличение энтропии системы в этом случае можно аналитически показать на примере процесса, в котором температура обоих тел из-за трения увеличивается. Приняв теплоемкости обоих тел постоянными, увеличение энтропии этой системы можно рассчитать как
ΔSс = ΔS1 + ΔS2 = 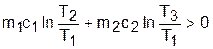 , (8.26)
, (8.26)
где m1, m2 – массы первого и второго тела;
с1, с2 – удельные теплоемкости первого и второго тела;
Т2, Т3 – температуры, до которых были нагреты первое и второе тело в результате трения.
Так как T2>T1 и T3>T1, а с1>0 и с2>0, то и ΔSc>0. Иллюстрацией такого примера может служить добывание огня первобытным человеком путем вращения палочки, зажатой в отверстии деревянного предмета. Необходимо отметить, что преобразование работы трения в теплоту не обязательно должно сопровождаться увеличением температуры тел. Так, в случае трения друг о друга двух кусков льда, имеющих температуру 0 ºС, изменения температуры этих кусков льда не будет, а преобразование работы трения в теплоту будет проявляться в виде плавления льда.
Таким образом, необратимое преобразование механической работы в теплоту всегда приводит к увеличению энтропии системы.
Теперь проанализируем обратный предыдущему процесс преобразования теплоты в работу. В отличие от возможности полного преобразования работы в теплоту полностью преобразовать теплоту в работу невозможно, это было доказано в разд. 8.1.1 и 8.1.2.
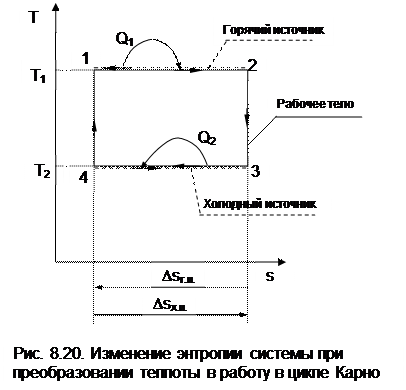 |
Изменение энтропии изолированной системы при обратимом преобразовании теплоты в работу рассмотрим на примере цикла Карно (рис. 8.20). Такая система состоит из горячего (г.и.) и холодного (х.и.) источников теплоты и рабочего тела (р.т.). Изменение энтропии в такой системе соответствует выражению
ΔSc=ΔSг.и+ΔSр.т+ΔSх.и. (8.27)
Поскольку рабочее тело совершает замкнутый процесс (цикл), то изменение его энтропии равно нулю (ΔSр.т=0). Процессы подвода теплоты к рабочему телу 12 и отвода теплоты от рабочего тела 34 обратимые, поэтому изменение энтропии горячего источника (отрезок 21) равно изменению энтропии холодного источника теплоты (отрезок 43), взятому с обратным знаком (ΔSг.и = - ΔSх.и). В результате получили, что изменение энтропии в этой системе
ΔSc=ΔSг.и+ΔSр.т=0. (8.28)
Этот вывод о неизменности энтропии системы (ΔSc=0) при обратимом преобразовании теплоты в работу справедлив для любого обратимого цикла, поскольку любой обратимый цикл можно представить в виде суммы элементарных обратимых циклов Карно.
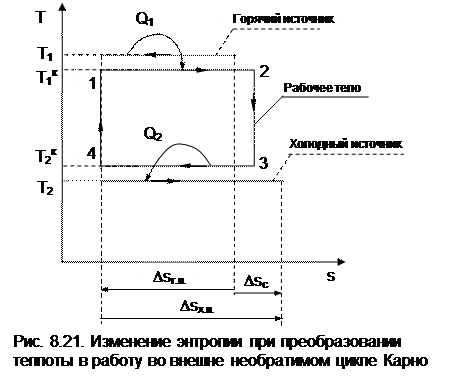 |
При необратимом преобразовании теплоты в работу, когда есть разница температур между горячим источником теплоты и рабочим телом на процессе подвода теплоты и между рабочим телом и холодным источником теплоты на процессе отвода теплоты, энтропия системы возрастает (ΔSc>0). Это наглядно иллюстрируется необратимым циклом Карно (рис. 8.21). В этом случае увеличение энтропии системы обусловлено большим по модулю значением изменения энтропии холодного источника по сравнению с изменением энтропии горячего источника теплоты.
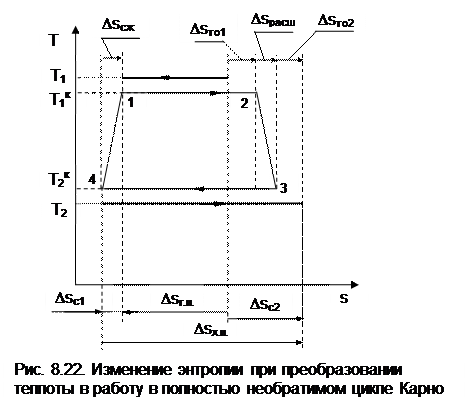 |
В случае, когда кроме внешней необратимости (разности температур между телом, отдающим теплоту, и телом, получающим теплоту) присутствует внутренняя необратимость, вызванная наличием трения в реальных процессах, увеличение энтропии системы будет еще больше по сравнению с циклом, имеющим только внешнюю необратимость. Так, если для цикла Карно с внешней необратимостью (рис.8.21) добавить внутреннюю необратимость, вызванную трением на адиабатных процессах расширения и сжатия рабочего тела, получим полностью необратимый цикл Карно (рис.8.22). У такого цикла увеличение энтропии холодного тела будет еще больше, чем у цикла, изображенного на рис. 8.21, при одинаковых значениях Q1, Т1, Т2, Т1к, Т2к. Расширение процесса отвода теплоты 34 по отношению к процессу подвода теплоты к рабочему телу 12, обусловленное наличием трения в адиабатных процессов 23 и 41, приводит к увеличению энтропии холодного источника теплоты в полностью необратимом цикле Карно по сравнению с внешне необратимым циклом Карно:
ΔSc=ΔSг.и+ΔSх.и=ΔSc1+ΔSс2=ΔSто1+ΔSрасш+ΔSто2+ΔSсж, (8.29)
где ΔSто1 – увеличение энтропии системы за счет необратимости теплообмена между горячим источником теплоты и рабочим телом;
ΔSрасш – увеличение энтропии за счет необратимости процесса адиабатного расширения рабочего тела;
ΔSто2 – увеличение энтропии системы за счет необратимости теплообмена между рабочим телом и холодным источником теплоты;
ΔSсж – увеличение энтропии за счет необратимости процесса адиабатного сжатия рабочего тела.
Принцип возрастания энтропии в изолированной системе относится к любому необратимому циклу теплового двигателя, поскольку, используя понятие среднетермодинамической температуры, любой внутренне обратимый цикл рабочего тела можно представить в виде эквивалентного цикла Карно, а процессы горячего и холодного источников теплоты привести к эквивалентным изотермическим процессам.
Date: 2015-05-09; view: 957; Нарушение авторских прав