
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

При теплообмене
|
|
Рассмотрим процесс обратимого теплообмена между двумя телами, имеющими одинаковую постоянную температуру Т1 (рис. 8.16). В обратимом теплообмене отсутствует разница температур между телами. Первое тело (1т) отдает теплоту Q (процесс 12), и его энтропия уменьшается на величину ΔS1 = Q/T1. Второе тело (2т) согласно первому закону термодинамики получает то же количество теплоты (процесс 21), но с обратным знаком (-Q), и его энтропия увеличивается на величину ΔS2 = - ΔS1 = -Q/T1, так как обратимый процесс получения теплоты идет по траектории 21, совпадающей с процессом отвода теплоты 12. Суммарное изменение энтропии этой системы
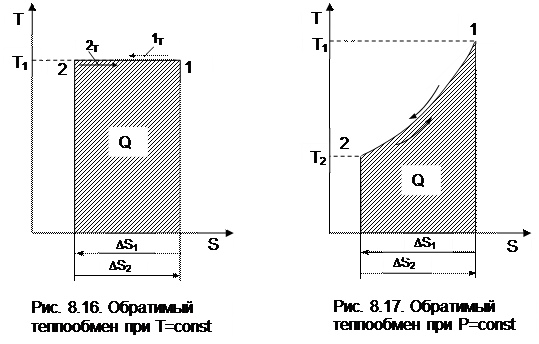 |
ΔSC = ΔS1 + ΔS2 = 0. (8.23)
Выражение (8.23) справедливо для любого случая обратимого теплообмена. Так, при переменной температуре двух тел в случае обратимого теплообмена между ними (рис.8.17) получаем изменение энтропии в этой системы тоже равное нулю:
ΔSC = ΔS1 + ΔS2 = 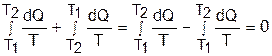 . (8.24)
. (8.24)
Таким образом, при обратимом теплообмене энтропия системы не изменяется.
Реальный процесс теплообмена между телами происходит при конечной разности температур и поэтому необратим.
Рассмотрим теплообмен между двумя телами, имеющими постоянные температуры Т1 и Т2 (рис.8.18). Первое тело отдает теплоту Q (процесс 12), а второе (процесс 34) получает теплоту - Q.
Изменение энтропии системы в этом случае будет больше нуля, так как Т1>T2, а Q>0:
ΔSC = ΔS1 + ΔS2 = 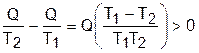 . (8.25)
. (8.25)
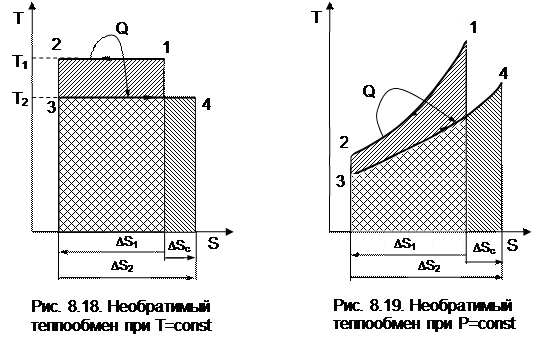 |
Аналогичная ситуация будет и при необратимом теплообмене между телами с переменной температурой (рис. 8.19), такой процесс возможен в поверхностном теплообменнике.
Таким образом, при необратимом теплообмене энтропия системы возрастает.
Date: 2015-05-09; view: 884; Нарушение авторских прав