
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Третье начало термодинамики
|
|
Уравнение (10.1) позволяет легко понять утверждение, составляющее содержание ТРЕТЬЕГО НАЧАЛА ТЕРМОДИНАМИКИ: При стремлении температуры к абсолютному нулю энтропия термодинамической системы тоже стремится к нулю (точнее, в общем случае, к постоянному минимальному значению, которое Макс Планк предложил всегда считать равным нулю). Понятно, что при стремлении температуры к абсолютному нулю, термодинамическая система будет стремиться к своему самому низкому энергетическому состоянию (состоянию с минимальной энергией), которое, естественно, единственное. Следовательно, число способов осуществления этого состояния, при котором все молекулы имеют минимальную энергию, равно единице, то есть W = 1. Поскольку термодинамическая вероятность равна единице, то ее логарифм равен нулю, и, согласно формуле (10.1) энтропия тоже равна нулю.
Это рассуждение не является строгим, но качественно оно дает тот же результат, что и строгое доказательство тепловой теоремы Нернста (как часто называют третье начало термодинамики). Смотрите также вывод формулы (7.14).
ПРИЛОЖЕНИЯ к «ОСНОВАМ ТЕРМОДИНАМИКИ»
ПРИЛОЖЕНИЕ 1
Рассмотрим модель идеального газа с точки зрения кинетической теории газов, основанной на принципах классической механики. Как пришли к этой модели?
Если рассматривать номинально одинаковый объем Vном некоторого вещества в трех агрегатных состояниях, то различие в плотностях пара и жидкости (или пара и твердого состояния) означает различие в концентрациях молекул, то есть nпара << nтв ~ nж, и, следовательно, собственный объем молекул вещества в газообразном состоянии много меньше объема номинального, то есть Vсобств << Vном и, значит, в случае достаточно разреженных газов собственным объемом молекул можно пренебречь, а сами молекулы можно считать материальными точками. Таково первое предположение в модели идеального газа.
Второе предположение вытекает из следующего: Экспериментальные данные показывают, что потенциальная энергия взаимодействия молекул на расстоянии при увеличении расстояний с порядка единиц диаметров молекул до десятков уменьшается в сотни раз, что означает - взаимодействием молекул на расстоянии можно пренебречь. Если потенциальной энергией молекул на расстоянии пренебрегают (отвлекаясь также от потенциальной энергии кратковременных взаимодействий при «соприкосновениях»), то всю энергию идеального газа можно считать кинетической энергией его молекул.
Уравнение состояния идеального газа легко получить, рассматривая давление газа с точки зрения молекулярно-кинетической теории. В основе расчета - классическое представление о силе как быстроте изменения импульса. Сначала рассматривается одна молекула массой m в прямоугольном ящике длиной b и площадью S стенки, перпендикулярной к оси Х. Удары о стенку считаются абсолютно упругими, и рассматривается одна только x-компонента движения. Тогда изменения импульса при ударе о стенку Dpx = 2mvx. Сила действия молекулы на стенку fx = Dpx/Dt = mvx2/b (здесь учтено, что Dt =2b/vx - время, через которое молекула вернется для следующего удара о стенку). Если теперь просуммировать удары всех N молекул, находящихся в ящике, то после деления суммарной силы на площадку S, получим давление на стенку
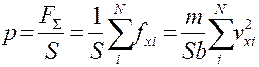 |
Можно ввести среднеквадратичную скорость, учитывая наличие трех измерений пространства, то есть < v2 > = <vx2 > + <vy2 > + <vz2 > = 3<vx2 > (хотя, вообще говоря, эта замена требует специального обоснования, но мы сочтем этот переход справедливым в силу независимости движений во взаимно перпендикулярных направлениях и полной хаотичности движения молекул). Заменив Svxi2 на N<vx2>, получаем для давления
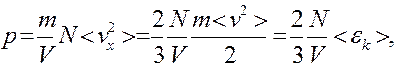 |
где <ek> - средняя кинетическая энергия одной молекулы, а V = Sb - объем нашего «ящика».
Поскольку полная энергия молекул идеального газа Е = Екин = =N<ek>, то
PV = 2Екин/3.
Если ввести энергетическую температуру q = kT = 2<ek >/3, равную 2/3 от средней кинетической энергии молекулы идеального газа, то получим уравнение состояния идеального газа (3.2)
PV = Nq = NkT, (3.2)
где k - коэффициент, переводящий джоули в градусы Кельвина.
При N = NA уравнение принимает вид известного уравнения Клапейрона-Менделеева в расчете на один моль идеального газа
PV = RT. (1.1`)
ПРИЛОЖЕНИЕ 2
Экспериментально измерить показатель адиабаты можно, например, по скорости распространения звука в газе (смотрите § 3.3.), но существует и теоретическое предсказание значения этой величины, основанное на гипотезе о равнораспределении кинетической энергии молекул по степеням свободы.
Как известно, число степеней свободы тела равно числу независимых координат, которые надо указать, чтобы однозначно определить положение этого тела в пространстве. Поэтому у материальной точки число степеней свободы i = 3, а у абсолютно твердого тела – 6 (например, три координаты для указания положения центра масс и три угла поворота относительно координатных осей). Из хаотичности обмена энергией молекулами при взаимодействиях родилась гипотеза (которая после подтверждения на опыте полученных на ее основе выводов стала называться законом) о том, что кинетическая энергия в среднем равномерно распределяется по всем степеням свободы. Обратившись к модели идеального газа для случая и воспользовавшись результатами, полученными в ПРИЛОЖЕНИИ 1, мы видим, что средняя кинетическая энергия одноатомной молекулы (потенциальной энергии у идеального газа нет) записывается в виде <ek> = 3kT/2. Это означает, что если гипотеза о равнораспределении кинетической энергии справедлива, то на одну степень свободы приходится kT/2 джоулей энергии.
Если число степеней свободы у одной молекулы равно i, то внутренняя энергия одного моля идеального газа U = iNAkT/2. Молярная теплоемкость при постоянном объеме (вычисленная по формуле (2.4)) CV = iNAk/2 = iR/2.
Из формулы Майера (2.8) получаем, что CP = CV + R = (i+2)R/2. Следовательно, показатель адиабаты для идеального газа определяется числом степеней свободы, приходящимся на одну молекулу. Например, молекулы воздуха двухатомные, значит, число степеней свободы у такой молекулы i = 5. Отсюда показатель адиабаты для воздуха должен равняться g = (i + 2)/ i = 1,4.
Поскольку экспериментальные данные не противоречат предсказаниям теории, то это считается подтверждением справедливости гипотезы о равнораспределении кинетической энергии по степеням свободы при хаотическом движении молекул.
ПРИЛОЖЕНИЕ 3
Date: 2015-05-09; view: 912; Нарушение авторских прав