
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Адиабатный процесс. В изохорном процессе не совершается работа
|
|
В изохорном процессе не совершается работа. Естественно рассмотреть процесс, в котором не передается теплота. Адиабатный (или адиабатический) процесс — это процесс, при котором не происходит передачи теплоты между газом (системой) и внешними телами. Не вдаваясь в анализ процесса теплопередачи, который не входит в нашу программу, отметим лишь, что быстрые, «горячие» молекулы не успевают ни войти в газ, ни выйти из него. С другой стороны, конечно, предполагается, что адиабатный процесс, как и рассмотренные ранее изопроцессы, протекает столь медленно, что по всему газу (системе) успевают установиться одинаковые значения параметров. Переход от одного значения параметров к другому происходит обратимым образом через равновесные состояния.
Итак, δ Q = 0. Тогда по первому началу dU = –δ А или
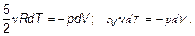 (2.12)
(2.12)
Еще одну связь между малыми изменениями параметров можно найти, продифференцировав уравнение состояния pV = ν RT. По формуле дифференцирования произведения получим
Vdp + pdV = ν RdT. (2.13)
Исключая ν dT, получим из (2.12) дифференциальное уравнение адиабатического процесса:
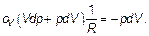 (2.14)
(2.14)
Разделяя переменные, найдем,
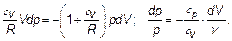 (2.15)
(2.15)
Напомним, что для двухатомных газов молярные теплоемкости при постоянном объеме сV и постоянном давлении ср будут сV = 5 R /2, ср = сV + R = 7 R /2. Отношение теплоемкостей называется показателем адиабаты (называемым также коэффициентом Пуассона) и обозначается γ.
Для двухатомных газов γ = ср / сV = 7/5 = 1,4.
Интегрируя полученное дифференциальное уравнение от параметров начального (первого) состояния V 1и р 1до параметров конечного (второго) состояния V 2и р 2, получим
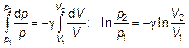 (2.16)
(2.16)
или
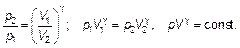 (2.17)
(2.17)
Так как показатель адиабаты γ > 1, то, сравнивая изотермический (с показателем, равным единице, рV = const) и адиабатный процессы, видим (рис. 2.4), что на V – р -диаграмме адиабатный процесс спадает быстрее (круче).
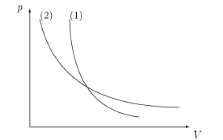
Рис. 2.4. Изотерма (2) и адиабата (1)
Вычислим работу при адиабатном процессе, используя, что в любом состоянии адиабатного процесса
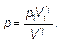 (2.18)
(2.18)
Найдем, интегрируя,
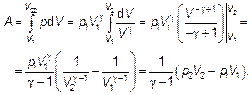 (2.19)
(2.19)
Как уже отмечалось, изменение внутренней энергии в адиабатном процессеравно убыли работы, совершенной газом Δ U = – А.
Date: 2015-05-08; view: 1240; Нарушение авторских прав