
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Квазиравновесный адиабатный процесс
|
|
Адиабатный процесс проводится в системе с постоянным количест-вом вещества v при отсутствии теплообмена с внешней средой (d Q = 0). Для этого система должна быть термодинамически изолирована. При адиабатном процессе температура системы изменяется. Поэтому равновесный адиабатный процесс должен протекать настолько медленно, чтобы его длительность была много больше времени температурной релаксации системы, т. е. t >> 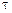 . Отсюда следует часто трудно выполнимое, жесткое требование к качеству тепловой изоляции системы.
. Отсюда следует часто трудно выполнимое, жесткое требование к качеству тепловой изоляции системы.
Чтобы избежать этого затруднения, на практике адиабатный процесс проводят как квазиравновесный: объем системы изменяют настолько быстро, чтобы за время длительности процесса можно было пренебречь теплообменом системы с внешней средой, т. е. d Q ® 0. Ясно, что температурная релаксация системы за такой интервал времени не завершается, и неравномерность температуры в разных частях объема не позволяет считать такой адиабатный процесс равновесным. Однако, выбирая объем системы достаточно малым и проводя процесс при незначительном изменении давления, объема и температуры системы, можно считать его квазиравновесным.
Адиабатный процесс в системе идеального газа с постоянным числом одинаковых молекул аналитически записывается либо уравнением (6.1), либо уравнением (6.2)
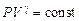 , (6.1)
, (6.1)
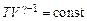 , (6.2)
, (6.2)
где показатель адиабаты g определяется только «числом степеней свободы» i [1] молекулы газа и равен отношению теплоемкостей газа при постоянном давлении СP (изобарический процесс) и при постоянном объеме СV (изохорический процесс)
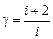 , (6.3)
, (6.3)
 . (6.4)
. (6.4)
Рассмотрим относительное изменение параметров состояния системы, удовлетворяющее условию проведения квазиравновесного адиабатного процесса.
Задавшись приращениями  давления, объема и температуры, из формул (6.1) и (6.2) получим соответственно уравнения
давления, объема и температуры, из формул (6.1) и (6.2) получим соответственно уравнения
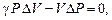
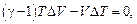
из которых следует, что относительные изменения объема и темпе-
ратуры зависят от относительного изменения давления следующим образом:
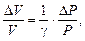
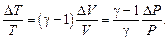
Для одно-, двух- и трехатомных молекул число степеней свободы соответственно равно i = 3, i = 5, i = 6. Пусть i = 5 и g = 1,4.
Условие квазиравновесия требует, чтобы приращения параметров состояния системы были малы. Особенно это относится к температуре. Пусть 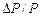 = 0,01, тогда
= 0,01, тогда  V / V = 0,007 и
V / V = 0,007 и  Т / Т = 0,003. Проведем количественную оценку приращения параметров.
Т / Т = 0,003. Проведем количественную оценку приращения параметров.
В качестве наименьшего давления в системе примем атмосферное дав-ление Р = 1,01×105 Па. Тогда приращение давления 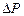 = 1,01×103 Па =
= 1,01×103 Па =
= 103 мм вод. ст. Оно может быть измерено непосредственно U -об-разным жидкостным манометром, один вход которого соединен c системой, а второй, открытый – непосредственно с внешней средой.
Если в исходном состоянии система имеет комнатную температуру, например Т = 300 К, то по окончании адиабатного процесса расширения температура уменьшится на  Т = 1К (или на 1 °С). Столь незначительное уменьшение температуры позволяет считать ее приблизительно постоянной. Следовательно, адиабатный быстропротекающий процесс в этих условиях вполне можно рассматривать как квазиравновесный.
Т = 1К (или на 1 °С). Столь незначительное уменьшение температуры позволяет считать ее приблизительно постоянной. Следовательно, адиабатный быстропротекающий процесс в этих условиях вполне можно рассматривать как квазиравновесный.
Date: 2015-05-08; view: 869; Нарушение авторских прав