
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Опыт 3. Использование комплексометрического титрования для количественного определения жесткости воды
|
|
Реактивы: аммиачный буфер, представляющий собой смесь равных объемов 0,1 М раствора NH4Cl и 0,1 М раствора NH4OH; индикатор для обнаружения ионов жесткости – эриохром черный Т (порошок), 0,01 Н раствор трилона Б, образцы жесткой воды.
Посуда, принадлежности и оборудование: бюретки на 25 см3; пипетки на 50 см3 (1 шт.), на 25 см3 (2 шт.) и на 10 см3 (2 шт.), конические колбы для титрования на 250 см3 (3 шт.)
Трилон Б представляет собой двунатриевую соль этилендиаминотетрауксусной кислоты:
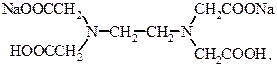
Он образует с ионами жесткости (Ca2+, Mg2+) комплексные соединения.
Эриохром черный Т имеет строение:
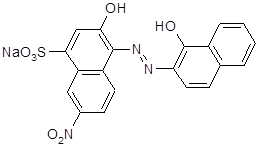
Он является комплексонометрическим индикатором для определения ионов кальция и магния. Индикатор в исследуемом водном растворе вначале имеет вишневую окраску. По мере титрования все ионы жесткости связываются. После этого трилон Б оказывается в избытке, при его гидролизе образуется NaOH, рН раствора повышается, и индикатор изменяет окраску на синюю.
Методика проведения опыта. В коническую колбу на 250 см3 пипеткой отмерьте 50 см3 жесткой воды, добавьте 5 см3 аммиачного буфера с рН=9 и неполную лопаточку индикатора эриохрома черного. Приготовьте аналогично три одинаковых образца.
Бюретку заполните раствором трилона Б, протитруйте образцы воды раствором трилона Б. В ходе титрования проходит реакция с образованием комплексной соли катиона жесткости с трилоном Б. Титрование образца проводите до перехода окраски из вишнево-красной через фиолетовую в сине-голубую. Результаты титрования в трех повторностях не должны отличаться друг от друга более, чем на 0,1 см3. Найдите среднее значение. Результаты титрования запишите в лабораторный журнал. Проведите расчет жесткости воды по закону эквивалентов для реакции между реагентами:
Ж(Н2О) = Vср.∙N∙1000/V(H2O), мэкв/л,
где Vср. − средний объём раствора трилона Б, пошедший на титрование;
N – нормальность раствора трилона Б, моль/л;
V(H2O) – объем образца исследуемой воды, см3.
На основании расчета сделайте вывод об уровне общей жесткости воды (жесткая, мягкая, средней жесткости, см. с. 52). Оцените качество исследуемой воды и ее пригодность или непригодность для технологических, бытовых и питьевых нужд. Предложите универсальные способы устранения одновременно всех солей временной и постоянной жесткости и запишите уравнения этих реакций.
Список рекомендуемой литературы
1. Глинка Н.Л. Общая химия. – М.: Юрайт, 2012. – 898 с. (и др. годы изд.); М.: КноРус, 2012. – 752 с. (и др. годы изд.); М.: Интеграл-пресс, 2011. – 727 с. (и др. годы изд.).
2. Коровин Н.В. Общая химия. – М.: Академия, 2011. – 496 с. (и др. годы изд.); М.: Высшая школа, 2010. – 557 с. (и др. годы изд.).
3. Глинка Н.Л. Задачи и упражнения по общей химии. – М.: КноРус, 2012. – 240 с. (и др. годы изд.); М.: Интеграл-Пресс, 2011. – 240 с. (и др. годы изд.).
4. Денисов В.В., Дрововозова Т.И., Лозановская И.Н. Химия. – М.: Март, 2003. – 464 с. (и др. годы изд.).
5. Гельфман М.И., Юстратов В.П. Химия. – СПб.: Лань, 2008. – 480 с. (и др. годы изд.).
Date: 2015-05-08; view: 807; Нарушение авторских прав