
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Теория рассматриваемого вопроса
|
|
Одной из важнейших теплофизических характеристик вещества является теплоемкость.
Теплоемкостью называется количество теплоты, которое требуется для изменения температуры единицы количества вещества на один градус.
В зависимости от количества вещества, принятого за единицу, различаются теплоёмкости:
массовая – с, кДж / (кг К) – для 1 кг;
мольная – c 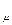 , кДж / (кмоль К) – для 1 киломоля;
, кДж / (кмоль К) – для 1 киломоля;
объёмная – с 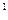 , кДж / (м
, кДж / (м 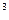 К) – для 1 м
К) – для 1 м 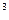 газа, взятого при
газа, взятого при
нормальных физических условиях.
Связь между ними выражается следующими зависимостями:
с 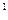 = c
= c 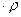 =
= 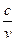 ; (3.1)
; (3.1)
c 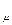 = c
= c 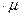 = с
= с 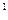
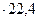 (3.2)
(3.2)
Здесь 22,4 м 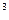 / кмоль – объём киломоля газа при нормальных физических
/ кмоль – объём киломоля газа при нормальных физических
условиях (T 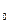 = 273 K, B
= 273 K, B 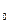 = 760 мм рт.ст.);
= 760 мм рт.ст.);
v – удельный объём газа, м 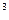 ;
;
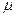 – мольная масса газа, кг / кмоль.
– мольная масса газа, кг / кмоль.
Теплоемкость одного и того же газа не является величиной постоянной и зависит от количества газа, его температуры и от характера процесса.
В связи с зависимостью теплоемкости от температуры введены понятия истинная и средняя теплоемкости.
Если теплоемкость определена в интервале температур от T 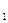 до T
до T 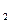 (величина нагрева газа в эксперименте конечна), то она называется средней теплоемкостью в данном интервале.
(величина нагрева газа в эксперименте конечна), то она называется средней теплоемкостью в данном интервале.
Например, для 1 кг газа в изобарном процессе нагрева в интервале температур от T 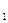 до T
до T 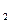 средняя теплоемкость определяется по формуле:
средняя теплоемкость определяется по формуле:
(c 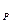 )
) 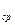 =
= 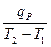 (3.3)
(3.3)
Истинная теплоемкость – это предел, κ которому стремится средняя теплоемкость при приближении интервала температур T 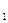 – T
– T 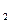 к нулю:
к нулю:
с 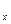 =
=  , (3.4)
, (3.4)
где x – параметр, определяющий характер процесса.
Теплоемкость одноатомных газов не зависит от температуры и её можно считать постоянной величиной. Для двухатомных газов эта зависимость становится ощутимой только при высоких температурах (практически выше 500°С). Для трех- и многоатомных газов указанная зависимость очень существенна и может быть выражена математическим рядом:
c 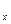 =
= 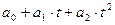 , (3.5)
, (3.5)
где a 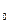 , a
, a 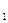 , a
, a 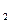 – коэффициенты (постоянные для данного газа), которые
– коэффициенты (постоянные для данного газа), которые
приводятся в справочной литературе;
t – температура газа в 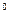 С.
С.
Величина теплоемкости различных газов зависит от атомного веса,
числа атомов в молекуле, пространственной структуры молекул и т.д.
Для идеальных газов, молекулы которых обладают только поступательными и вращательными степенями свободы, мольная теплоемкость в изохорном процессе может быть рассчитана на основе молекулярно-кинетической теории по формуле:
c 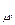 =
= 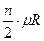 =
= 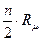 , (3.6)
, (3.6)
где R 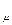 – универсальная газовая постоянная, равная 8314 Дж / (кмоль
– универсальная газовая постоянная, равная 8314 Дж / (кмоль  град);
град);
n – число степеней свободы движения (поступательного и
вращательного) молекул газа.
В зависимости от характера процесса в расчётах используют теплоемкости:
при постоянном давлении (изобарная) – с 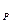 ;
;
при постоянном объеме (изохорная) – с 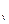 .
.
Изобарная и изохорная теплоемкости идеального газа связаны между собой уравнением Майера:
мольные –
c 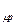 – c
– c 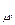 = R
= R 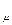 , (3.7)
, (3.7)
массовые –
с 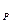 – с
– с 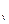 = R (3.8)
= R (3.8)
Поэтому, для одноатомных газов (n = 3):
c 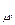 = 12,45 кДж / (кмоль К);
= 12,45 кДж / (кмоль К);
c 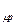 = 20,75 кДж / (кмоль К).
= 20,75 кДж / (кмоль К).
Для двухатомных газов и воздуха (n = 5) при t до 500 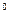 С:
С:
c 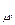 = 20,75 кДж / (кмоль К);
= 20,75 кДж / (кмоль К);
c 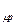 = 29,35 кДж / (кмоль К).
= 29,35 кДж / (кмоль К).
Численные значения средних теплоемкостей различных газов в интервале температур от 0 до +1000 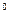 С и выше приводятся в справочной литературе. Их использование позволяет рассчитывать количество тепла в процессе с учетом зависимости теплоемкости от температуры.
С и выше приводятся в справочной литературе. Их использование позволяет рассчитывать количество тепла в процессе с учетом зависимости теплоемкости от температуры.
Например, для изобарного процесса:
Q 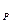 = (c
= (c 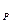 )
) 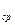
 M
M  (t
(t 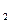 - t
- t 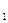 ) = (c
) = (c 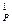 )
) 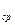
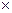 V
V 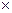 (t
(t 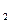 - t
- t 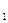 ), (3.9)
), (3.9)
где М – масса газа, кг;
V – объём газа в кубических метрах при нормальных физических условиях.
(c 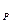 )
) 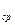 , (c
, (c 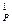 )
) 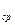 – соответственно массовая и объемная средние изобарные
– соответственно массовая и объемная средние изобарные
теплоемкости (в интервале температур от t 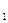 до t
до t 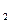 ),
),
определяемые по формулам:
(c 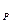 )
) 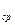 =
= 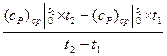 (3.10)
(3.10)
(c 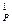 )
) 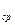 =
= 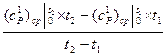 (3.11)
(3.11)
Здесь (c 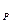 )
) 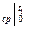 ; (c
; (c 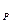 )
) 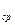
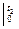 – средние массовые изобарные теплоемкости;
– средние массовые изобарные теплоемкости;
(c 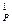 )
) 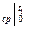 ; (c
; (c 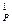 )
) 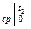 – средние объёмные изобарные теплоемкости.
– средние объёмные изобарные теплоемкости.
Численные значения указанных теплоемкостей в интервале температур от нуля до t 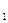 , t
, t 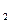 определяют по справочной литературе.
определяют по справочной литературе.
Теплоёмкость веществ определяется опытным путём.
Для вычисления изобарной теплоёмкости воздуха по формуле (3.3) на установке (в данной работе), называемой проточным калорифером, определяются расход воздуха, количество тепла, используемого для его нагрева, и изменение температуры.
Date: 2015-05-08; view: 706; Нарушение авторских прав