
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Основные формулы и законы. · Первый постулат Бора (постулат стационарных состояний)
|
|
· Первый постулат Бора (постулат стационарных состояний)
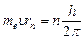 (n = 1, 2, 3,…),
(n = 1, 2, 3,…),
где me = 9,1∙ 10-31 кг – масса электрона, 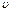 – скорость электрона на n – й орбите, радиус которой равен rn, h = 6,62 ∙ 10-34 Дж∙с – постоянная Планка.
– скорость электрона на n – й орбите, радиус которой равен rn, h = 6,62 ∙ 10-34 Дж∙с – постоянная Планка.
· Второй постулат Бора (правило частот)
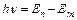 ,
, 
где En, Em – энергии стационарных состояний атома соответственно до и после излучения (поглощения), 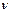 – частота излученного (поглощенного) кванта энергии.
– частота излученного (поглощенного) кванта энергии.
· Обобщенная формула Бальмера, описывающая серии в спектре водорода:
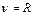
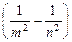 ,
,
где 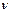 – частота спектральных линий в спектре атома водорода;
– частота спектральных линий в спектре атома водорода;
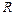 = 3,29 ∙ 1015 1/с - постоянная Ридберга; m – определяет серию линий в спектре атома водорода:
= 3,29 ∙ 1015 1/с - постоянная Ридберга; m – определяет серию линий в спектре атома водорода:
m = 1 - серия Лаймана (расположена в ультрафиолетовой части спектра);
m = 2 - серия Бальмера (расположена в видимой части спектра);
| m = 3 - серия Пашена; m = 4 - серия Брэкета; m = 5 - серия Пфунда; m = 6 - серия Хэмфри. | 
| расположены в инфракрасной части спектра |
n = m + 1 – определяет отдельные линии соответствующей серии m.
· Радиус n – й орбиты электрона в атоме водорода: 
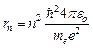 ,
,
где ћ = h/2 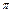 = 1,055∙10-34 Дж ∙ с - постоянная Планка; εо = 8,85∙10-12 Ф/м - электрическая постоянная; е = 1,6∙10-19 Кл – заряд электрона, me - масса электрона.
= 1,055∙10-34 Дж ∙ с - постоянная Планка; εо = 8,85∙10-12 Ф/м - электрическая постоянная; е = 1,6∙10-19 Кл – заряд электрона, me - масса электрона.
· Энергия n – го стационарного состояния
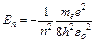 ,
,
где n – номер стационарной орбиты.
· Энергия электрона в атоме водорода:
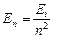 ,
,
где Еi – энергия ионизации атома водорода.
· Потенциал ионизации
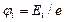
· Потенциал возбуждения
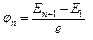 .
.
Date: 2015-05-05; view: 546; Нарушение авторских прав