
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Число электронов, отданных восстановителем, равно числу электронов, принятых окислителем
|
|
Рассмотрим пример составления окислительно-восстановитель-ной реакции между перманганатом калия (KMnO4) и сульфидом калия (K2S) в кислой среде (H2SO4):
KMnO4 + K2S + H2SO4  K2SO4 + MnSO4 + S + H2O.
K2SO4 + MnSO4 + S + H2O.
1. Определяем степени окисления элементов в исходных веществах и продуктах реакции:
 +
+  + H2SO4(среда)
+ H2SO4(среда) 
 +
+  +
+  + H2O.
+ H2O.
В данной реакции изменяются степени окисления атомов серы от –2 до 0 и марганца от +7 до +2.
2. Выбираем восстановитель и окислитель:
Так как в данной реакции степень окисления серы повышается, а марганца понижается, то K2S – восстановитель, а KMnO4 – окислитель.
3. Определяем число электронов, отдаваемых восстановителем и принимаемых окислителем, и записываем схему перехода электронов, состоящую из уравнений процессов окисления и восстановления:
 5 S-2
5 S-2  Sо + 2
Sо + 2 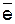 (процесс окисления);
(процесс окисления);
2 Mn+7 + 5 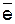
 Mn+2 (процесс восстановления);
Mn+2 (процесс восстановления);

5S-2 + 2Mn+7  5Sо + 2Mn+2.
5Sо + 2Mn+2.
Для нахождения стехиометрических коэффициентов суммарной реакции первую реакцию умножаем на 5, вторую – на 2, так как число отданных восстановителем электронов должно равняться числу электронов, принятых окислителем. Коэффициенты перед веществами, атомы которых не изменяют свою степень окисления, находим методом подбора.
4. Записываем уравнение реакции с учетом найденных коэффициентов:
2KMnO4 + 5K2S + 8H2SO4  2MnSO4 + 5S+ 6K2SO4 + 8H2O.
2MnSO4 + 5S+ 6K2SO4 + 8H2O.
Правильность подобранных коэффициентов определяем балансом кислорода в обеих частях уравнения (8+32=8+24+8).
Date: 2015-10-19; view: 567; Нарушение авторских прав