
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Количественная характеристика
|
|
Любая окислительно-восстановительная реакция состоит из двух процессов: окисления и восстановления. В окислительно-восстано-вительной реакции атомы окислителя и атомы восстановителя находятся в двух степенях окисления каждый, образуя окислительно-восстановительную пару (ОВП).
Рассмотрим в качества примера обратимую реакцию:
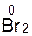 +
+ 
 2
2 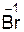 +
+  ;
;
Br2 + 2 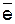
 2Br – (процесс восстановления);
2Br – (процесс восстановления);
2J−  J2+ 2
J2+ 2 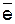 (процесс окисления).
(процесс окисления).
Исходные и полученные в результате реакции ионы образуют две окислительно-восстановительные пары: Br2/2Br− и J2/2J−, в которых Br2 и J2 являются окисленными, а Br− и J− – восстановленными формами. В числителе ОВ пары принято ставить атом в более высокой степени окисления в знаменателе – в более низкой степени окисления.
Состояние атома, отвечающее более низкой степени окисления, представляет его восстановленную форму, а более высокой степени окисления – его окисленную форму.
Восстановленная и окисленная формы каждого элемента характеризуются различной активностью, что зависит, прежде всего, от природы элемента, температуры, концентрации (если реакция протекает в растворе), давления (если один или несколько компонентов реакции – газы), характера среды и пр.
Окислительно-восстановительная способность пары может быть количественно оценена величиной окислительно-восстановительного
потенциала.
Для водных растворов при температуре 25 оС(298 К) и концентрациях окисленных и восстановленных форм, равных 1 моль/л, величины, характеризующие их активность, называются стандартными окислительно-восстановительными потенциалами (Е о), которые измеряются в вольтах (В).
В приложении представлена таблица стандартных окислительно-восстановительных потенциалов (табл. 11), в которой приведены окислительно-восстановительные пары (ОВП), т.е. окисленная (числитель) и восстановленная (знаменатель) формы атома (иона) и значения Е о.
Пары располагаются в порядке уменьшения отрицательного и роста положительного значения потенциала, т.е. в порядке уменьшения восстановительной способности восстановленной формы и роста окислительной способности окисленной формы.
Чем больше величина положительного потенциала, тем большей окислительной способностью обладает эта пара.
Чем больше величина отрицательного потенциала, тем большей восстановительной способностью обладает данная пара.
Date: 2015-10-19; view: 501; Нарушение авторских прав