
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Биоорганическая химия
|
|

ЗАДАНИЕ №1
ВВЕДЕНИЕ В БИООРГАНИЧЕСКУЮ ХИМИЮ. СТРОЕНИЕ, КЛАССИФИКАЦИЯ И ПРИНЦИПЫ СОВРЕМЕННОЙ НОМЕНКЛАТУРЫ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ.
I. Подготовиться к ответам на следующие вопросы:
1. Предмет биоорганической химии, ее значение для биологии и медицины.
2. Строение и классификация органических соединений по типу углеродной цепи и природе функциональных групп.
3. Номенклатура органических соединений. Заместительная номенклатура ИЮПАК.
а) номенклатурные термины: родоначальная структура, характеристи-ческая группа, заместитель;
б) последовательность составления названия органического соедине-ния по общей схеме.
4. Тривиальная и радикально-функциональная номенклатуры органических соединений.
II. Подготовиться к тестированному контролю по теме: «Номенклатура органических соединений»
III. Выполнить письменно задания:
1. Назвать по заместительной номенклатуре ИЮПАК соединения:
а) CH2 = CH – CH – CH = C – COH б) HOOC – CH – CH2 – CH – COOH
½ ½ ½ ½
CH3 OH SH NH2
 в) CH3 – CH – C – CH – CH3 г)
в) CH3 – CH – C – CH – CH3 г)

 I II I -OH
I II I -OH
CH2 O CH3

 I HO- -CH – CH3
I HO- -CH – CH3
CH3 I
CH3
2. Написать структурные формулы соединений:
а) 2,3,4,5 – тетрагидроксипентаналь;
б) 2 – оксопентандиовая кислота;
в) 3,4,4 – триметилпентанамин – 2;
г) 7-метил-4-этилоктен-5-тиол-3;
д) 2-гидрокси-4-сульфоциклопентанкарбоновая кислота.
ЛИТЕРАТУРА:
1. Тюкавкина Н.А., Бауков Ю.И. Биоорганическая химия. – М.: Медицина, 1991. - С. 9 - 29.
2. Руководство к лабораторно-практическим занятиям по биоорганической химии /Н.Н. Артемьева, В.Л. Белобородов, С.К. Еремин и др.; / Под ред. Н.А. Тюкавкиной. – М.: Медицина, 1985. – С. 24-27.
ЗАДАНИЕ №2
ВЗАИМНОЕ ВЛИЯНИЕ АТОМОВ В ОРГАНИЧЕСКИХ МОЛЕКУЛАХ. ЭЛЕКТРОННЫЕ ЭФФЕКТЫ ЗАМЕСТИТЕЛЕЙ.
I. Подготовиться к ответам на следующие вопросы:
1. Сопряженные системы. Сопряженные системы с открытой цепью сопряжения, р,p-сопряжение, p,p-сопряжение.
2. Сопряженные системы с замкнутой цепью сопряжения. Ароматичность, критерии ароматичности. Ароматичность бензоидных и гетероциклических соединений. Энергия сопряжения.
3. Индуктивный и мезомерный электронные эффекты заместителей. Электроноакцепторные /ЭА/ и электронодонорные /ЭД/ заместители.
4. Характеристика заместителей с учетом проявляемых эффектов и прогнозирование свойств органических соединений.
II. Подготовиться к контролю по теме: «Сопряженные системы, ароматичность. Электронные эффекты заместителей».
III. Выполнить письменные задания:
1. Обосновать соответствие критериям ароматичности нафталина и пиримидина.
2. Указать вид и знак электронных эффектов заместителей в следующих соединениях:
а) CH2 = CH – CH = CH – CH = CH – NH2 Гексатриен – 1,3,5-амин-1.
б) в) г)
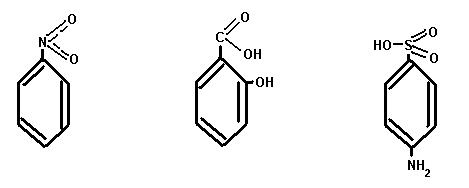
Нитробензол Салициловая Сульфаниловая
кислота кислота
ЛИТЕРАТУРА:
- Тюкавкина Н.А., Бауков Ю.И. Биоорганическая химия. - М. Медицина, 1991. - С. 37-51.
- Руководство к лабораторно-практическим занятиям по биоорганической химии /Н.Н. Артемьева, В.Л. Белобородое, С.К. Еремин и др.; / Под ред. Н.А. Тюкавкиной. - М.; Медицина, 1985. - С. 34-42.
- Материалы лекций.
ЗАДАНИЕ №3
ИЗОМЕРИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
I. Подготовиться к ответам на следующие вопросы:
1. Изомерия как специфическое явление органической химии. Структурная изомерия, ее виды.
2. Стереохимия как область химии, изучающая пространственное строение органических соединений. Конфигурация и конформация как важнейшие понятия стереохимии.
3. Конформации открытых цепей. Проекционные формулы Ньюмена. Энергетическая характеристика конформационных состояний.
4. Конформация циклических соединений. Аксиальные и экваториальные связи.
5. Энантиомерия. Оптическая активность. Д и L – система стереохимической номенклатуры. Проекционные формулы Фишера. Глицериновый альдегид как конфигурационный стандарт. Рацематы.
6. Диастереомерия. s - Диастереомерия. p - Диастереомерия как стереоизо-мерия в ряду соединений с двойной связью.
7. Связь пространственного строения органических соединений с их биологической активностью.
II. Выполнить письменные задания:
1. Изобразить с помощью проекционных формул Ньюмена различные конформации этиленгликоля. Показать энергетику конформационных превращений этого двухатомного спирта.
2. Начертить кресловидную конформацию молекулы миоинозита /циклогексангексаол – 1,2,3,4,5,6/, содержащегося в мышцах и многих органах. При этом необходимо учесть, что 5 ОН – групп занимают экваториальное положение.
3. Определить виды изомерии у a - аминокислоты изолейцина:
СН3 – СН2 – СН – СН – СООН.
I I
СН3 NH2
Ответ обосновать пояснениями и конкретными примерами по каждому из проявляющихся видов изомерии.
ЛИТЕРАТУРА:
1. Тюкавкина Н.А., Бауков Ю.И. Биоорганическая химия. – М.: Медицина, 1991. - С. 51 - 87.
2. Руководство к лабораторно-практическим занятиям по биоорганической химии /Н.Н. Артемьева, В.Л. Белобородов, С.К. Еремин и др.; / Под ред. Н.А. Тюкавкиной. – М.: Медицина, 1985. – С. 27-33.
3. Методическая разработка: «Пространственное строение органических молекул. Конфигурации, конформации, хиральность».
4. Материалы лекций.
ЗАДАНИЕ №4
КИСЛОТНОСТЬ И ОСНОВНОСТЬ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ. ГИДРОКСИСОЕДИНЕНИЯ.
I. Подготовиться к ответам на следующие вопросы:
1. Кислотность и основность органических соединений в соответствии с протолитической /протонной/ теорией кислот и оснований Бренстеда-Лоури.
2. Факторы, влияющие на кислотные и основные свойства органических соединений.
3. Гидроксисоединения. Спирты и фенолы, их классификация, номенклатура, изомерия и медико-биологическое значение.
4. Химические свойства спиртов и фенолов. Реакции окисления спиртов и фенолов. Действие системы НАД+ и НАДН.
5. Реакции нуклеофильного замещения /SN/ в молекулах спиртов, их механизм. Реакции хелатообразования многоатомных спиртов.
6. Реакции электрофильного замещения /SE/ с участием ароматической системы, их механизм /нитрование бензола/. Ориентирующее влияние заместителей в ароматическом ядре на реакционную способность в реакциях электрофильного замещения /нитрование и сульфирование фенола/.
II. Подготовиться к лабораторной работе на тему: «Свойства гидроксисоединений».
III. Подготовиться к контрольной работе по теме: «Кислотные и основные свойства органических соединений. Гидроксисоединения».
IV. Выполнить письменно задания:
CH3
I
1. В молекуле пеницилламина СН3 – С – СН – СООН, используемого в
I I
SH NH2
качестве противоядия при отравлении соединениями тяжелых металлов, указать:
а) кислотные центры и расположить их в порядке уменьшения кислотности;
б) основные центры и определить место протонирования.
2. Сравнить кислотные свойства следующих соединений: этанамина и этантиола, пиррола и имидазола, этанола и метанола, бензойной кислоты и бензолсульфокислоты, метана и бензола. Ответ на этот вопрос обосновать с учетом значений рКа и факторов, влияющих на кислотные свойства органических соединений.
3. Написать уравнения химических реакций:
а) окисления 3,3-диметилгексанола-2 с участием системы НАД+ - НАДН и назвать продукт по заместительной номенклатуре ИЮПАК;
б) хелатообразования многоатомных спиртов сорбита и инозита с участием гидроксида меди (II) в щелочной среде;
в) нуклеофильного замещения /SN/ пропанола-1 с бромоводородной кислотой и показать ее механизм.
ЛИТЕРАТУРА:
1. Тюкавкина Н.А., Бауков Ю.И. Биоорганическая химия. – М.: Медицина, 1991. - С. 100-112, 153-155, 223, 242-246.
2. Руководство к лабораторно-практическим занятиям по биоорганической химии /Н.Н. Артемьева, В.Л. Белобородов, С.К. Еремин и др.; / Под ред. Н.А. Тюкавкиной. – М.: Медицина, 1985. – С. 42-50.
3. Материалы лекций.
ЗАДАНИЕ №5
КАРБОНИЛЬНЫЕ И КАРБОКСИЛЬНЫЕ СОЕДИНЕНИЯ.
I. Подготовиться к ответам на следующие вопросы:
1. Карбонильные соединения, их классификация. Электронное строение карбонильной группы. Реакционные центры в молекулах альдегидов и карбоновых кислот.
2. Реакции нуклеофильного присоединения (AN) в молекулах альдегидов и кетонов. Реакции окисления и альдольного присоединения альдегидов /конденсация/.
3. Карбоновые кислоты, их классификация, номенклатура, изомерия.
4. Химические свойства карбоновых кислот. Реакции диссоциации, галогенирования, декарбоксилирования, этерификации.
5. Медико-биологическое значение карбонильных и карбоксильных соединений.
II. Подготовиться к лабораторной работе по теме: «Химические свойства карбонильных и карбоксильных соединений».
III. Подготовиться к контролю по теме: «Карбонильные и карбоксильные соединения».
IV. Выполнить письменные задания:
1. Показать нуклеофильное присоединение /AN/ на примере взаимодействия ацетона с этанолом.
2. Написать уравнение реакций:
а) конденсации альдегида бутаналя;
б) декарбоксилирования гександиовой кислоты;
в) этерификации с участием бензойной кислоты и пропанола-2.
ЛИТЕРАТУРА:
1. Тюкавкина Н.А., Бауков Ю.И. Биоорганическая химия. – М.: Медицина, 1991. – С. 182-200, 211-212.
- Руководство к лабораторно-практическим занятиям по биоорганической химии /Н.Н. Артемьева, В.Л. Белобородов, С.К. Еремин, и др.; / Под ред. Н.А. Тюкавкиной. – М.: Медицина, 1985.- С. 92-96, 108-110.
- Материалы лекций.
ЗАДАНИЕ №6
ГИДРОКСИКИСЛОТЫ. КЕТОНОКИСЛОТЫ.
I. Подготовиться к ответам на следующие вопросы:
1. Гидроксикислоты и кетонокислоты, их строение, изомерия, номенклатура.
2. Химические свойства гидрокси-и-кетонокислот. Реакции диссоциации, декарбоксилирования, окисления, этерификации (нуклеофильное замещение у sp2 – гибридизированного атома углерода).
3. Пути превращения b - гидроксимасляной кислоты в организме.
4. Медико-биологическое значение гидрокси-и-кетонокислот и их производных. Салициловая кислота и фармпрепараты на ее основе, их получение и применение в медицине.
II. Подготовиться к лабораторной работе: «Химические свойства гидроксикислот и кетонокислот».
III. Подготовиться к контролю по теме «Гидроксикислоты и кетонокислоты».
IV. Выполнить письменно задания:
1. Определить виды изомерии, проявляющиеся у 2,3-дигидроксибутановой кислоты, дать пояснения, привести структурные формулы изомеров.
2. Показать строение энантиомеров яблочной и b - гидроксимасляной кислот. Написать уравнения реакций их окисления, декарбоксилирования и этерификации – для яблочной кислоты по –ОН группе я участием уксусной кислоты, а для b - гидроксимасляной кислоты по –СООН группе с участием этилового спирта.
3. Сравнить кислотные свойства бензойной и ацетилсалициловой кислот.
4. Написать уравнения реакций взаимодействия пировиноградной кислоты с метиловым спиртом. Объяснить, по каким механизмам протекают эти реакции.
ЛИТЕРАТУРА:
1. Тюкавкина Н.А., Бауков Ю.И. Биоорганическая химия. - М. Медицина, 1991. - С.181-202.
2. Руководство к лабораторно-практическим занятиям по биоорганической химии /Н.Н. Артемьева, В.Л. Белобородое, С.К. Еремин и др.; / Под ред. Н.А. Тюкавкиной. - М.; Медицина, 1985. - С. 92-106, 109-110.
3. Материалы лекций.
ЗАДАНИЕ №7
РУБЕЖНАЯ КОНТРОЛЬНАЯ РАБОТА №2
Подготовиться к ответам на следующие вопросы:
1. Строение и классификация органических соединений по типу углеродной цепи, химическим связям и природе функциональных групп.
2. Номенклатура органических соединений. Заместительная номенклатура ИЮПАК. Тривиальная и радикально-функциональная номенклатуры.
3. Сопряженные системы с открытой цепью сопряжения, р,p и p,p - сопряжение.
4. Сопряженные системы с замкнутой цепь сопряжения. Ароматичность, критерии ароматичности. Ароматичность бензоидных и гетероциклических соединений. Энергия сопряжения.
5. Индуктивный и мезомерный электронные эффекты заместителей. Характеристика заместителей с учетом проявляемых электронных эффектов и прогнозирование свойств органических соединений.
6. Изомерия органических соединений. Структурная изомерия. Конфигурация и конформация как важнейшие понятия стереохимии. Конформации открытых цепей и циклических соединений.
7. Энантиомерия. Оптическая активность. D и L – системы стереохимической номенклатуры. Проекционные формулы Фишера. Глицериновый альдегид как конфигурационный стандарт. Рацематы.
8. Диастереомерия. s - Диастереомерия. p - Диастереомерия как стереоизоме-рия в ряду соединений с двойной связью. Связь пространственного строения органических соединений с их биологической активностью.
9. Кислотность и основность органических соединений в соответствии с протолитической теорией Бренстеда – Лоури. Факторы, влияющие на кислотные и основные свойства органических соединений.
10. Гидроксисоединения. Спирты и фенолы, их классификация, номенклатура, изомерия и медико-биологическое значение.
11. Химические свойства спиртов. Реакции окисления (действия системы НАД+ - НАДН), нуклеофильного замещения /SN/, хелатообразования.
12. Химические свойства фенолов. Реакции электрофильного замещения /SE/ и окисления.
13. Карбонильные соединения, их классификация. Электронное строение карбонильной группы. Реакционные центры в молекулах альдегидов и карбоновых кислот.
14. Реакции нуклеофильного присоединения /АN/ в молекулах альдегидов и кетонов. Реакции окисления и альдольного присоединения альдегидов. Понятие об альдольной и кротоновой конденсации альдегидов.
15. Карбоновые кислоты, их классификация, номенклатура, изомерия.
16. Химические свойства карбоновых кислот. Реакции диссоциации, галогенирования, декарбоксилирования и этерификации (нуклеофильное замещение у sp2 – гибридизованного атома углерода).
17. Гидроксикислоты, кетонокислоты, их строение, изомерия, номенклатура.
18. Реакции окисления гидроксикислот, декарбоксилирования a и b - кетонокислот (ПВК, ацетоуксусная кислота) и этерификации гидрокси-и-кетонокислот.
19. Пути превращения b-гидроксимаслянной кислоты в организме.
20. Медико-биологическое значение гидрокси-и-кетонокислот и их производных. Салициловая кислота и фармпрепараты на ее основе, их получение и применение в медицине.
ВАРИАНТ БИЛЕТА.
1. CH3
I
CH3 – CH – C – CH = CH – CH2 – NH2
I I
SH CH3
Определить, к какому классу относится это соединение по типу углеродной цепи, химическим связям, функциональным группам. Назвать его по заместительной номенклатуре ИЮПАК, указать звенья.
- Гидроксикислоты, их состав, строение, номенклатура, химические свойства, медико-биологическое значение.
- Энантиомерия. Оптическая активность. D и L – системы стереохимической номенклатуры. Проекционные формулы Фишера. Глицериновый альдегид как конфигурационный стандарт. Рацематы.
- Расшифровать схему превращений, называя реагенты и продукты реакций, указав их механизм:
 CH3 В
CH3 В
I НАД+ +2Cu(OH)2,t0 -CO2



 CH3 – C –CH2 – OH А Б
CH3 – C –CH2 – OH А Б
I +СН3ОН
CH3 НОН3С+ +С2Н5ОН Г
+С2Н5ОН(ИЗБ)
 Д Е Ж
Д Е Ж
- Написать уравнения реакций хелатообразования с участием многоатомных спиртов сорбита и инозита.
- Доказать соответствие критериям ароматичности гетероциклического соединения пиридина.
ЛИТЕРАТУРА:
См. Д.З. №1 –6.
ЗАДАНИЕ №8
БИОЛОГИЧЕСКИ АКТИВНЫЕ ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ
I. Подготовиться к ответам на следующие вопросы:
1. Классификация и общая характеристика гетероциклических соединений. Прототропная и лактим-лактамная таутомерия.
2. Кислотно-основные свойства азотсодержащих гетероциклов.
3. Пятичленные гетероциклы с одним и двумя гетероатомами, их производные. Структура гема. Гемоглобин и его роль в организме.
4. Шестичленные гетероциклические соединения с одним и двумя гетероатомами (пиридин и пиримидин) и их производные. Биологическая роль этих соединений.
5. Конденсированные бициклические гетероциклы. Пурин и соединения пуринового ряда, их биологическая роль.
6. Влияние гетероатомов в гетероциклических соединениях (пиридин, пиримидин) на реакционную способность в реакциях электрофильного (SE) и нуклеофильного (SN) замещения. Ориентирующее влияние гетероатомов.
II. Подготовиться к контролю по теме «Гетероциклические соединения».
III. Разобрать устно обучающую задачу №1 (см. литературный источник №2).
IV. Выполнить письменно упражнения:
1. Показать прототропную таутомерию на примере аденина и ксантина.
2. Дать объяснение кислотно-основных свойств гетероциклических соединений на примере имидазола.
3. Указать, у какого из соединений – пиридина или пиримидина более выражена способность к реакциям нуклеофильного замещения (SN). Дать объяснение на основе ориентирующего влияния гетероатомов.
4. Написать уравнения реакций сульфирования и дальнейшего гидроксилирования (с участием КОН) пиридина. Объяснить, по каким механизмам протекают эти реакции.
ЛИТЕРАТУРА:
1. Тюкавкина Н.А., Бауков Ю.И. Биоорганическая химия. – М.: Медицина, 1991. – С. 275-282, 286-287, 291-294, 296-298, 301-304.
2. Руководство к лабораторно-практическим занятиям по биоорганической химии /Н.Н. Артемьева, В.Л. Белобородов, С.К. Еремин, и др.; / Под ред. Н.А. Тюкавкиной. – М.: Медицина, 1985.- С. 164-166.
3. Методическое пособие: «Физиологически активные гетероциклические соединения, их строение и биологическая роль».
ЗАДАНИЕ № 9
УГЛЕВОДЫ. СТРОЕНИЕ И СВОЙСТВА МОНОСАХАРИДОВ
I. Подготовить ответы на следующие вопросы:
1. Углеводы. Классификация.
2. Моносахариды. Классификация по функциям и числу атомов углерода в цепи. Представители классов.
3. Энантиомерия, диастереомерия моносахаридов, эпимеры.
4. Образование циклических форм моносахаридов по Хеуорсу.
5. a,b-аномеры, таутомеры. Явление мутаротации.
6. Реакционная способность моносахаридов (свойства альдегидов, спиртов, полуацеталей и специфические свойства).
7. Производные моносахаридов (аминосахары, сахарные кислоты), их биологическая роль.
II. Подготовиться к лабораторной работе «Химические свойства моносахаридов».
III. Подготовиться к контрольной работе по теме «Моносахариды. Строение и химические свойства».
IV. Выполнить письменно упражнения:
1. Написать проекционные формулы таутомерной смеси для Д-глюкозы и Д- фруктозы. Назвать таутомеры.
2. Написать формулы a, Д – галактопиранозы; b,Д – дезоксирибофуранозы; 2-амино-2-дезокси-Д-глюкопиранозы.
3. Написать реакции:
а) окисления Д-рибозы;
б) восстановления Д-галактозы;
в) образование метил-a,Д-галактопиранозида.
V. Разобрать устно обучающие задачи в учебнике: Тюкавкина Н.А. «Руководство к лабораторным занятиям по биоорганической химии», М., 1985, с.201-213, задачи №1,2,3,4.
ЛИТЕРАТУРА:
1. Тюкавкина Н.А., Бауков Ю.И. Биоорганическая химия. – М.: Медицина, 1991. – С. 377-406.
2. Материалы лекций.
ЗАДАНИЕ №10
СЛОЖНЫЕ УГЛЕВОДЫ
I. Подготовить ответы на следующие вопросы:
1. Состав и строение дисахаридов (мальтоза, лактоза, сахароза). Их биологическая роль.
2. Химические свойства дисахаридов, особенности сахарозы.
3. Состав и строение гомополисахаридов: крахмал, гликоген, клетчатка. Вторичная структура крахмала и клетчатки.
4. Гидролиз крахмала.
5. Биологическая роль гомополисахаридов.
6. Состав и строение гетерополисахаридов (гиалуроновая кислота). Гликопротеины. Их биологическая роль.
II. Подготовиться к лабораторной работе «Химические свойства сложных углеводов».
III. Подготовиться к контрольной работе по теме «Строение и химические свойства сложных углеводов».
IV. Выполнить письменно упражнения:
1. Написать уравнения реакций гидролиза сахарозы и лактозы.
2. Написать уравнение реакции окисления мальтозы гидроксидом меди (II) при нагревании.
3. Написать уравнение реакции образования сахарата меди (II).
ЛИТЕРАТУРА:
1. Тюкавкина Н.А., Бауков Ю.И. Биоорганическая химия. – М.: Медицина, 1991. – С. 407 - 430.
2. Руководство к лабораторно-практическим занятиям по биоорганической химии /Н.Н. Артемьева, В.Л. Белобородов, С.К. Еремин, и др.; / Под ред. Н.А. Тюкавкиной. – М.: Медицина, 1985.- С. 201-213, задачи №1,2,3,4.
3. Методическая разработка кафедры по теме «Дисахариды».
4. Материалы лекций.
ЗАДАНИЕ №11
АМИНОКИСЛОТЫ. БЕЛКИ.
I. Подготовить ответы на следующие вопросы:
1. Классификация и строение аминокислот.
2. Физико-химические характеристики боковой цепи аминокислот.
3. Кислотно-основные свойства аминокислот.
4. Химические свойства аминокислот. Реакции декарбоксилирования, переаминирования, окислительного дезаминирования, образования пептидов.
5. Пептиды. Пространственное строение пептидной группы. Белки. Уровни структурной организации белковой молекулы.
6. Биологическая роль аминокислот и белков.
II. Подготовиться к лабораторной работе «Химические реакции, лежащие в основе качественного определения белков и аминокислот».
III. Разобрать обучающую задачу:
1. Определить область значений рН, в которой находится изоэлектрическая точка (и.э.т.) трипептида сер-асп-ала.
Молекулярная формула пептида:
O O
II II
H2N – CH – C – N – CH – C – N – CH – COOH

 I I I I I
I I I I I
CH2 H CH2 H CH3
I I
OH COOH
сериласпарагилаланин
N -конец С-конец
В водном растворе ионное состояние пептида отвечает формуле:
O O
II II
H3NÅ – CH – C – N – CH – C – N – CH – COOQ
I I I I I
CH2 H CH2 H CH3
I I
OH COOQ
Общий заряд пептида отрицательный. Это пептид кислотного характера. Его и.э.т. лежит в слабокислой среде.
Ответ: pJ<7
2. Какой заряд имеет пептид цис-гис-вал в растворе с рН 4,5?
Ионное состояние пептида цис-гис-вал отвечает формуле:
O O
II II
H3NÅ – CH – C – N – CH – C – N – CH – COOQ
I I I I I
 CH2 H CH2 H CH – CH3
CH2 H CH2 H CH – CH3


 I HNÅ I
I HNÅ I
SQ CH3


N
I
H
В кислой среде при рН 4,5 диссоциация групп кислотного характера подавлена. При этом формируется катион пептида:
O O
II II
H3NÅ – CH – C – N – CH – C – N – CH – COOH
I I I I I
 CH2 H CH2 H CH – CH3
CH2 H CH2 H CH – CH3


 I HNÅ I
I HNÅ I
SH СH3


N
I
H
Ответ: общий заряд положительный.
IV. Подготовиться к контрольной работе по теме: «Строение и химические свойства аминокислот».
V. Выполнить письменно упражнения:
1. Написать уравнение реакции переаминирования щавелевоуксусной и глутаминовой кислот.
2. Написать уравнение реакции декарбоксилирования лизина.
3. Составить схему реакции окислительного дезаминирования аспарагиновой кислоты.
4. Написать уравнение реакции образования трипептида глу-иле-фен и определить область значений рН, в которой находится и.э.т. данного пептида.
ЛИТЕРАТУРА:
1. Тюкавкина Н.А., Бауков Ю.И. Биоорганическая химия. – М.: Медицина, 1991. – С. 313-376.
2. Руководство к лабораторно-практическим занятиям по биоорганической химии /Н.Н. Артемьева, В.Л. Белобородов, С.К. Еремин, и др.; / Под ред. Н.А. Тюкавкиной. – М.: Медицина, 1985.- С.182-200. Обучающие задачи №2,3,5,6,9.
3. Материалы лекций
ЗАДАНИЕ №12
НУКЛЕИНОВЫЕ КИСЛОТЫ
I. Подготовиться к ответам на следующие вопросы:
1. Нуклеозиды (пуриновые и пиримидиновые), их образование, состав, строение, номенклатура. Гидролиз нуклеозидов.
2. Мононуклеотиды, их образование, состав, строение, номенклатура. Гидролиз нуклеотидов РНК и ДНК.
3. Уровни структурной организации ДНК (первичная, вторичная, третичная структуры). Фосфодиэфирные связи, комплементарность нуклеиновых оснований. Биологическая роль ДНК.
4. Уровни структурной организации РНК. Первичная структура, фосфодиэфирные связи. Виды РНК. Вторичная структура транспортной РНК («клеверный лист»), комплементарность нуклеиновых оснований. Биологическая роль РНК. Понятие о нуклеопротеидах.
5. Нуклеозидмоно- и полифосфаты: АМФ, АДФ, АТФ, их строение. Гидролиз АТФ. Биологическая роль АТФ и АДФ.
II. Подготовиться к контролю по теме «Нуклеиновые кислоты».
III. Разобрать устно обучающие задачи №№1,2,3 (см. литературный источник №2).
IV. Выполнить письменно упражнения:
1. Написать схему гидролиза нуклеозидов: гуанозина и уридина. Назвать продукты гидролиза.
2. Показать схему образования нуклеотидов РНК: 5’-Адениловой и 5’-Цитидиловой кислот.
3. Соединить посредством 3’®5’ фосфодиэфирной связи нуклеотиды ДНК: 5’-Тимидиловую и 5’ – Дезоксигуаниловую кислоты.
4. Показать стабилизацию вторичной структуры ДНК и РНК за счет водородных связей, возникающих между парами остатков комплементарных азотистых оснований: гуанина и цитозина; аденина и урацила.
ЛИТЕРАТУРА:
1. Тюкавкина Н.А., Бауков Ю.И. Биоорганическая химия. – М.: Медицина, 1991. – С. 431-436, 441-449, 452-456.
2. Руководство к лабораторно-практическим занятиям по биоорганической химии /Н.Н. Артемьева, В.Л. Белобородов, С.К. Еремин, и др.; / Под ред. Н.А. Тюкавкиной. – М.: Медицина, 1985.- С. 223-229.
3. Материалы лекции.
ЗАДАНИЕ №13
ЛИПИДЫ, СТРОЕНИЕ И СВОЙСТВА.
I. Подготовить ответы на следующие вопросы:
1. Липиды, классификация и биологическая роль. Природные высшие жирные кислоты как структурные компоненты омыляемых липидов. Состав и строение пальмитиновой, стеариновой, олеиновой, линолевой и линоленовой кислот.
2. Нейтральные липиды. Воска, жиры, масла. Естественные жиры как смесь триацилглицеринов. Гидролиз триацилглицеринов.
3. Сложные липиды. Фосфолипиды, L-фосфатидовые кислоты. Фосфатиды как производные L-фосфатидовых кислот. Состав, строение, гидролиз фосфатидов, их биологическая роль.
4. Сложные липиды. Сфинголипиды, сфингозин, церамиды, сфингомиелины, их состав, строение, биологическая роль.
II. Выполнить задания:
1. Написать схему образования триацилглицеринов:
а) линолеодистеарина;
б) 1,2 – дипальмитоолеина.
2. Написать схему образования фосфолипидов:
а) фосфатидилэтаноламина;
б) фосфатидилинозита.
3. Написать уравнения реакций кислотного гидролиза триолеина, фосфатидилсерина и щелочного гидролиза 1-линолео-2-стеаропальмитина и фосфатидилхолина.
ЛИТЕРАТУРА:
1. Тюкавкина Н.А., Бауков Ю.И. Биоорганическая химия. – М.: Медицина, 1991. - С. 457-467.
2. Руководство к лабораторно-практическим занятиям по биоорганической химии /Н.Н. Артемьева, В.Л. Белобородов, С.К. Еремин и др.; / Под ред. Н.А. Тюкавкиной. – М.: Медицина, 1985. – С. 118-122.
3. Материалы лекции.
Date: 2015-09-24; view: 3956; Нарушение авторских прав