
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Основні закони хімії
|
|
Закон збереження маси: в результаті хімічних перетворень сума мас речовин до реакції і сума мас речовин після реакції однакова.
Закон збереження енергії: будь-яка енергія не зникає і не виникає, а тільки одні її види переходять в інші.
Закон сталості складу: кожна речовина має постійний якісний і кількісний склад незалежно від способів її одержання. Речовини, що отримані різними способами, але які мають той самий якісний і кількісний склад, мають однакові хімічні властивості.
Закон кратних відношень: якщо два елементи утворюють один з одним кілька хімічних сполук, то маси одного елемента, що приходяться на ту саму масу іншого елемента, відносяться між собою як невеликі цілі числа.
Закон об'ємних відношень: об'єми взаємодіючих газоподібних речовин відносяться між собою і до об'ємів продуктів реакції, як невеликі цілі числа.
Закон Авогадро (1811 р.): у рівних об'ємах різних газів при однакових умовах міститься однакове число часток (молекул, атомів, йонів).
Наслідки: 1. Моль будь-якого газу при нормальних умовах займає об'єм 22,4 л.
2. Моль будь-якого газу за нормальних умов містить 6,02 · 1023 часток (стала Авогадро NА).
Закон еквівалентів: 1. хімічні елементи сполучаються один з одним, а речовини реагують і утворюються в еквівалентних кількостях.
2. Маси (об'єми) речовин, що реагують, пропорційні молярним масам (об'ємам) їхніх еквівалентів:
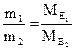
Завдання для самоконтролю до теми
"Основні закони хімії"
1. Обчисліть молярну масу еквівалентів Нітрогену в оксидах N2O, NO, NO2.
2. Обчисліть молярну масу еквівалентів металу в сполуках: Mn2O7, Mg2P2O7, Ba(OH)2, Ca3(PO4)2.
3. Обчисліть молярну масу еквівалентів металу, якщо при взаємодії 7,2 г металу з хлором було отримано 28,2 г солі. Молярна маса еквівалентів хлору 35,45 г/моль.
4. При відновленні 5,1 г метал (ІІІ) оксиду утворилось 2,7 г води. Визначте молярну масу еквівалентів металу і атомну масу металу. Молярна маса еквівалентів води дорівнює 9 г/моль.
5. На нейтралізацію 10 г лугу витрачено 9,9 г хлоридної кислоти. Обчисліть молярну масу еквівалентів лугу.
6. При пропущенні сірководню крізь розчин, який містить 2,98 г метал (І) хлориду, утворюється 2,2 г сульфіду. Обчисліть молярну масу еквівалентів металу.
7. Обчисліть молярні маси еквівалентів металу та його оксиду, якщо відомо, що 24 г металу сполучаються з 16 г кисню.
8. На нейтралізацію 1 г основи витрачено 0,56 дм3 гідроген хлориду (н.у.). Обчисліть молярну масу еквівалентів основи.
9. Унаслідок взаємодії 0,75 г двовалентного металу з кислотою виділилось 420 см3 водню (н.у.). Який метал використали для реакції?
10. 2 г двовалентного металу витісняють 1,12 л водню при нормальних умовах. Визначте молярну масу еквівалентів металу.
Date: 2015-09-24; view: 583; Нарушение авторских прав