Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Физические свойства и химический состав подземных вод
|
|
3.5. 1. Физические свойства подземных вод
При изучении подземных вод для различных целей определяют вкус, за- пах, цвет, прозрачность, температуру и другие физические свойства, которые характеризуют так называемые органолептические свойства воды, т. е. свойст- ва, определяемые при помощи органов чувств. Подземные воды обычно про- зрачны, бесцветны, не имеют запаха. Вкус подземной воды зависит от вида и содержания растворенных минеральных соединений и газов. Органолептиче- ские свойства могут резко ухудшаться при попадании в воду естественным или искусственным путем различных примесей (минеральных взвешенных частиц, органических веществ, некоторых химических элементов).
Температура подземной воды колеблется в широких пределах в зависи-
мости от глубины залегания водоносного слоя, особенностей геологического
строения, климатических условий и т. д. Различают воды холодные (температу- ра от 0 до 20°С), теплые, или субтермальные воды (20-37°С), термальные (37-100°С), перегретые (свыше 100°С). Очень холодные подземные воды цир- кулируют в зоне многолетней мерзлоты, в высокогорных районах; перегретые воды характерны для районов молодой вулканической деятельности (Камчатка, Исландия и др.).
На участках действующих водозаборов в основном распространены хо-
лодные воды с температурой от 5 до 20°С.
С увеличением глубины залегания температура воды по закону геотер-
мической ступени возрастает, достигая на глубине нескольких километров
100°С и более.
Согласно ГОСТ, к физическим свойствам подземных вод относятся также плотность, вязкость, электропроводность, радиоактивность и др.
Плотность воды − масса воды, находящаяся в единице ее объема. Мак- симальная плотность наблюдается при температуре 4°С. При повышении тем- пературы до 250°С плотность воды уменьшается до 0,799 г/см3, а при увеличе- нии количества растворенных в ней солей повышается до 1,400 г/см3. За счет пониженной плотности возможно конвективное, восходящее движение пере- гретых подземных вод.
Вязкость воды характеризует внутреннее сопротивление частиц ее дви- жению. С повышением температуры вязкость подземных вод уменьшается. Электропроводность подземных вод зависит от количества растворенных в них солей и выражается величинами удельных сопротивлений от 0,02 до
1,00 Ом • м. Радиоактивность подземных вод вызвана присутствием в ней ра-
диоактивных элементов (урана, стронция, цезия, радия, газообразной эманации радия − радона и др.). Даже ничтожно малые концентрации − сотые и тысячные
доли (мг/л) некоторых радиоактивных элементов − могут быть вредными для человека.
3.5.2. Химический состав подземных вод
Подземная вода представляет собой сложный водный раствор, содержа- щий растворенные соли, газы (С02, H2S, СН4 и др.), органические вещества и коллоиды. Количественные соотношения между отдельными компонентами обусловливают физические свойства и химический состав подземных вод.
Ионно-солевой состав. Подземная вода не встречается в химически чис- том виде. В ней обнаружено более 60 элементов периодической системы Мен- делеева. Основные компоненты (ионы), определяющие химический тип воды, −
|
Cl-, S0 2-
, HC0-3, Na
2+, Mg
2+, Са2+
и К +
. Эти ионы составляют более 90\% всех
растворенных в воде солей. Железо, нитриты, нитраты, водород, бром, йод,
фтор, бор, радиоактивные и другие элементы содержатся в воде в меньших ко-
личествах. Однако даже в небольших количествах они могут оказывать сущест-
венное влияние на оценку пригодности подземных вод для различных целей.
Суммарное содержание растворенных в воде минеральных веществ назы-
вают общей минерализацией. О ее величине судят по сухому или плот -
ному остатку (в мг/л или г/л), который получается после выпаривания опре- деленного объема воды при температуре 105−110°С. Между общей минерали- зацией подземных вод и их химическим составом существует определенная за- висимость (табл. 7).
Таблица 7
Классификация подземных вод по степени минерализации
| Виды воды | С у хой остаток, г / л | Прео бл адающи е ионы | Прео бл адающий химическ ий тип воды |
| Пресные | до 1 | НСО 3, СО 3, Са | Ги дрок ар бон а тно - каль циевый |
| Слабо сол о нов а т ы е | 1-3 | S042-, ре же С 1 | Су л ь ф а тны й, реж е хл орид н ый |
| Солоноватые | 3- 10 | То же | То же |
| Соленые | 10-50 | 2- S04, С 1 | Су л ь ф а тны й и хлори дн ый |
| Рассолы | Более 50 | CI, Са, Mg, Na | Хлори дн о - на тр ие вый |
В природных условиях общая минерализация подземных вод исключи- тельно разнообразна. Встречаются подземные воды с минерализацией от 0,1 г/л (высокогорные источники) до 500-600 г/л (глубокозалегающие воды Ангаро- Ленского артезианского бассейна). Общая минерализация − один из главных показателей качества подземных вод.
Для количественного выражения активной реакции подземных вод (рН) служит логарифм концентрации ионов водорода, взятый с обратным знаком, т. е. рН = −lg(H+). Вода с нейтральной реакцией имеет рН = 7, кислой рН < 7, щелочной рН > 7. Малые значения рН вызывают коррозию труб и ухудшают питьевые качества воды. Наилучшими питьевыми качествами вода обладает при рН = 6,5-8,5.
Свойство воды, обусловленное содержанием в ней ионов кальция и маг-
ния, называют жесткостью. Различают несколько видов жесткости.
Общая жесткость воды определяется суммарным содержанием в воде всех ионов кальция и магния.
Карбонатная жесткость (устранимая при кипячении воды) − обусловлена
содержанием в воде только гидрокарбонатных и карбонатных солей кальция и магния.
Кроме того, выделяют постоянную (неустранимую) жесткость, опреде-
ляемую вычитанием из общей жесткости карбонатной (устранимой).
Жесткость выражается в мг-экв/л Са2+ и Mg2+, причем 1 мг-экв/л жестко- сти соответствует 20,04 мг Са2+ или 12,16 мг Mg2+ в 1 л воды. Оценка вод по степени жесткости приводится по О. А. Алекину (табл. 8).
Классификация вод по степени жесткости
Таблица 8
| Воды | Общая жесткость, мг-экв/л |
| Очень мягкие | До 1,5 |
| Мягкие | 1,5-3,0 |
| Умеренно жесткие | 3,0-6,0 |
| Жесткие | 6,0-9,0 |
| Очень жесткие | Более 9,0 |
Газы в подземных водах. Газы содержатся в подземных водах в раство- ренном виде. Наиболее распространены в подземных водах кислород (02), угле- кислота (С02), сероводород (H2S), азот (N2), метан (СН4), благородные газы (ге- лий, аргон, радон и др.).
Газы заметно влияют на органолептические показатели подземных вод. Насыщенность воды свободной углекислотой придает ей способность разру- шать бетон.
Органические соединения и коллоиды. В подземной воде почти всегда со-
держатся органические вещества и микроорганизмы. Некоторые их виды пред-
ставляют серьезную опасность для питьевой воды.
В подземной воде могут также находиться коллоиды − твердые мине- ральные частицы, недиссоциированные Si02, Fe203 и т. д., находящиеся во взвешенном состоянии.
Виды химических анализов воды и формы их выражения. Различают три основных типа химических анализов: полевые, сокращенные и полные. Поле- вые анализы выполняются в полевых условиях с помощью походных лаборато- рий. Наиболее распространен сокращенный химический анализ, выполняемый
2-
в стационарных условиях с определением физических свойств, рН, СИ, S04,
- 2 2+
2+ 3+ 2+
+ - -
НС03, С03 -, Са
, Fe
, Fe
Mg, NH4
, N02, N03, H2S, 03, С02своб и C02 агрес-
сивной, общей и карбонатной жесткости, окисляемости и сухого остатка. Пол-
ный химический анализ проводится при детальном изучении водоносных гори-
зонтов.
Для краткой характеристики химического состава и физических свойств часто используют формулу М. Г. Курлова. В этой формуле ионный состав воды (в \%-экв) изображен наподобие дроби, где в числителе в убывающем порядке
указывается содержание анионов, а в знаменателе − катионов. Слева перед дро- бью перечисляются содержание микроэлементов (Br, I и др.) и свободных газов (С02 и др.), а также минерализация воды (М), в г/л. Справа от дроби записыва- ются температура воды Т в °С и величина рН.
Например, химический состав минеральных вод Мацесты по формуле
Курлова будет иметь следующий вид:
С1 95 НСО 3
 H2S 0,24 С02 0,12 М 11,3 Т 26,3° рН 6,7.
H2S 0,24 С02 0,12 М 11,3 Т 26,3° рН 6,7.
N a 7 8 C a l 4
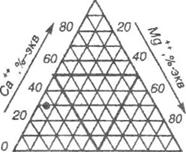
Графически химический состав подземных вод выражают в виде тре-
угольников, графиков-диаграмм и в других формах (рис. 21).
б а m, \%-экв
|
|
 100 0 10
100 0 10
 Са++
Са++
 Mg++
Mg++
Na++

|
HCO -

|
SO-
Cl-

 100 80 60 40 20 0
100 80 60 40 20 0
 Na+, \%-экв.
Na+, \%-экв.
Рис. 21. Выражение химического состава воды в графической форме:
а – треугольник анионного и катионного состава; б – график-диаграммы солевого состава; m – содержание ионов
 Оценка качества питьевых вод. Качество подземных вод, используемых для хозяйственно-питьевого водоснабжения, оценивается по органолептиче- ским и радиационным показателям, химическому составу и бактериальному за- грязнению. Гигиенические требования к качеству воды нецентрализованного водоснабжения, источником которого являются подземные воды, определяются Санитарно-эпидемиологическими правилами и нормами СанПиН 2.1.4.1175–02.
Оценка качества питьевых вод. Качество подземных вод, используемых для хозяйственно-питьевого водоснабжения, оценивается по органолептиче- ским и радиационным показателям, химическому составу и бактериальному за- грязнению. Гигиенические требования к качеству воды нецентрализованного водоснабжения, источником которого являются подземные воды, определяются Санитарно-эпидемиологическими правилами и нормами СанПиН 2.1.4.1175–02.
По органолептическим показателям питьевая вода должна быть прозрач- на, бесцветна, не иметь неприятного запаха и вкуса. Величина сухого остатка не должна превосходить 1 г/л, общая жесткость − 7,0 мг-экв/л, содержание же- леза − 0,3 мг/л. Содержание отдельных растворенных веществ не должно пре- вышать предельных значений, допустимых нормами.
В исключительных случаях могут быть использованы подземные воды с сухим остатком до 1,5 г/л, общей жесткостью до 10 мг-экв/л, содержанием же-
леза до 1 мг/л, но только по согласованию с органами санитарно- эпидемиологической службы. В питьевой воде совершенно недопустима пато- генная флора, т. е. болезнетворные микробы. Бактериальное загрязнение оце-
нивается по «коли-титру» и «коли-индексу». Подземная вода пригодна для пи- тья при большом «коли-титре» (не менее 300 мл) и малом «коли-индексе» (не более 3).
В целом, согласно Санитарным правилам, питьевая вода должна быть безопасна в эпидемическом и радиационном отношениях, безвредна по хими- ческому составу и иметь благоприятные органолептические показатели.
Оценка качества подземных вод для технических целей зависит от харак- тера того или иного производства. Для разных производств нужны воды раз- личного качества.
3.5.3. Агрессивность подземных вод к строительным конструкциям
Воды определенного химического состава могут оказывать разрушающее действие на бетонные и металлические конструкции, фильтры скважин, обсад- ные трубы, насосы и т. д. Подземная вода, разрушающая бетон и металл, счита- ется агрессивной.
Агрессивное действие вод на бетон проявляется в растворении его основ-
ного компонента − карбоната кальция, а также в образовании солей CaS04 •
2Н20, MgS04 • 2Н20 и сульфоалюмината кальция, вызывающего вспучивание и
крошение бетона.
Date: 2015-09-26; view: 2088; Нарушение авторских прав