
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Газовые законы
|
|
5.2. В соответствии с объединенным газовым законом 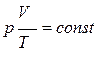 (при неизменном значении количества вещества газа).
(при неизменном значении количества вещества газа).
Графики 1 и 2 отображают прямопрорциональную зависимость, следовательно, отношение объема к температуре постоянно. Из этого следует, постоянство значения давления (р) –изобарические процессы.
 V
V
 р2
р2


 |
 р1
р1


 0 Т
0 Т
Рис. 5.18.
Если взять на графиках точки, которым соответствует одинаковое значение температуры и спроектировать их на ось объемов, то получится, что точке на нижнем графике соответствует меньший объем, а, следовательно, - большее давление (рис. 5.18). Следовательно, р1 > р2
5.5
 р
р


 1
1

 2
2
 0 V
0 V
Рис. 5.19

 р 1
р 1


 |



0 Т
Рис. 5.20
5.7. Рис. 5.4. 1-2, 3-4 – изобары (p12 < p34); 2-3 –изохора; 4-1 – изотерма.
Рис. 5.5. 1-2, – изобара; 2-3 –изотерма; 3-1 – изохора.
Рис. 5.6. 1-2, 3-4 – изобары; 2-3 –изохора; 4-1 – р ¯ Т ¯ V . Проведем изохоры 0-1 и 0-4. Изохоре 0-1 соответствует большее значение объема. Следовательно, при переходе газа из состояния 4 в состояние 1 его объем увеличивается.
Рис. 5.7. 4-5 – изотерма, 5-1 - адиабата.
Рис. 5.8. 1-2 – изохора; 2-3 – адиабата; 3-4 – изобара; 4-1- - изотерма.
Рис. 5.9. 3-1 – V ¯ Т р .
Рис. 5.12. 2-3; 4-1 - изобары (p23 < p41).
Рис. 5.14. 3-4 – изобара; 4-5 - V ¯ Т ¯ р ; 5-1 - V ¯ Т ¯ р ¯.
Рис. 5.15 1-2 – изобара; 2-3 –изохора; 3-4 - V Т р ¯; 4-1 V Т ¯ р ¯
5.8  Т= 1200 К.
Т= 1200 К.
 5.9. р
5.9. р


 9р0
9р0
|
 1
1
 |
|

 3р0
3р0
 2 4
2 4

 р0 3
р0 3
 |
0 V0 3V0 V
Рис. 5.21.

 р
р



 9р0 1
9р0 1
 |
3р0 2 4




 р0
р0
 0 100 300 V
0 100 300 V
Рис. 5.22.
5.10. CV( Ne ) = 12,5 кДж/(моль ×К); CР( Ne ) = 20,8 кДж/(моль ×К).
CV( С2Н6 ) = 24,9 кДж/(моль ×К); CР( С2Н6 ) = 33,2 кДж/(моль ×К).
ПРИЛОЖЕНИЯ
Стандартные значения теплоты образования сложных веществ из простых
Таблица 1
| Формула вещества | Теплота образования Qf, кДж/моль | Формула вещества | Теплота образования Qf, кДж/моль |
| СО | CH4 | ||
| CO2 | С2Н4 | ||
| Н2О(ж) | С2Н5ОН | ||
| Н2О(г) | С6Н12О6 |
Удельные теплоемкости веществ, удельные теплоты плавления льда и парообразования воды
Таблица 2
| Название вещества | Удельная теплоемкость, кДж/(кг×К) | Название вещества | Удельная теплоемкость, кДж/(кг×К) | Удельная теплота плавления, кДж/кг | Удельная теплота парообразования, кДж/кг |
| Лед | 2,1 | Серебро | 0,25 | ||
| Вода | 4,2 | Золото | 0,13 | ||
| Пар | 1,8 | Железо | 0,50 | ||
| Медь | 0,38 | Сталь | 0,50 | ||
| Свинец | 0,13 | Спирт | 2,5 |
Оглавление
Введение…………………………………………………………...…3
1.Единицы измерения физических величин……………………..…..4
2.Механика…………………………………………………………..…9
2.1.Действия с векторами. Кинематика…………………………..…9
2.2.Динамика……………………………………………………..….14
2.3.Работа, энергия. Импульс тела………………………………....19
3.Химическое равновесие………………………………………….…21
4.Тепловые явления…………………………………………………...28
5.Газовые законы……………………………………………………...33
Ответы и решения…………………………………………………..38
Приложения……………………………………………………………53
Оглавление……………………………………………………………..54
Учебное издание
Валентин Вениаминович Майзель
Олег Олегович Тужиков
Ирина Владимировна Лавникова
Юлия Викторовна Кострюкова
Date: 2015-09-18; view: 504; Нарушение авторских прав