
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Фазовые переходы 1 и 2 рода
|
|
До сих пор мы рассматривали, что вещество может находиться в различных фазах но само остается химически однородный во многих случаях это не так. Оно может состоять из нескольких химических различных компонент причем в разных фазах доля этих компонентов различна. Найдем такое максимальное количество, которое может одновременно состоять из n различных компонент. Предположим, что в равновесии находится R-радиус различных фаз соответственно нужно вести nr химический потенциалов 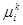 которые зависят от давления и температуры в системе. Здесь нижний индекс
которые зависят от давления и температуры в системе. Здесь нижний индекс 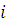 указывает компоненту
указывает компоненту 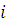 от 1 до
от 1 до 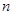 , а верхний индекс
, а верхний индекс 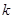 фазу в которую та компонента входит
фазу в которую та компонента входит 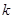 от 1 до r. Эти потенциалы зависят также от относительных консистенций
от 1 до r. Эти потенциалы зависят также от относительных консистенций 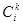 . Последнее определяется как
. Последнее определяется как
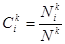
Полное число молекул всех компонент в й фазе имеются всего r(n-1) независимых концентраций в состояние равновесия химический потенциал 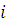 -компоненты должны принимать значения.
-компоненты должны принимать значения.
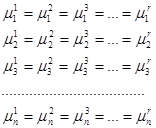
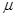 – зависимость от давления, температуры и концентрации.
– зависимость от давления, температуры и концентрации.
Число параметров не определенных равнозначно равно:
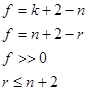
Величина 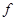 называется термодинамических степеней свободы. Число фаз которые могут находится в равновесном в частности если вещество химически однородно,
называется термодинамических степеней свободы. Число фаз которые могут находится в равновесном в частности если вещество химически однородно, 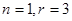 в случае 3-й точки, если же вещество состоит из 2 компонент
в случае 3-й точки, если же вещество состоит из 2 компонент 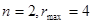 .
.
Рассмотрим частный случай когда имеются 2 компоненты, а вещество может находится в 2 различных фазах.
1.Пусть фаза 1 - это раствор, а фаза 2 - насыщенный пар в растворителе относительно концентрации растворимого вещества 1 вещества и растворителя 2 в жидкой фазе обозначен:
Условие равновесия 2-х фаз дается 2-мя уравнениями по одному для каждой из компонент:

Давление пара зависит не только от температуры, но и от концентрации растворимого веществаДавление пара в растворителе убывает с ростом по закону:
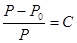 (Закон Рауля)
(Закон Рауля)
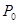 –давление пара над чистым растворителем над раствором.
–давление пара над чистым растворителем над раствором.
2.Пусть теперь фаза 1 жидкий раствор с концентрации растворимого вещества, а фаза 2 твердое вещество, в котором присутствует только растворитель используем те же уравнение для данной двухфазной систем. Решение предложим в виде 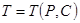 . Это соотношение показывает, что при заданном внешним давлением температура фазового перехода жидкость твердое тело зависит от концентрации
. Это соотношение показывает, что при заданном внешним давлением температура фазового перехода жидкость твердое тело зависит от концентрации 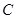 растворимого вещества при
растворимого вещества при 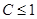 температура понижается:
температура понижается:
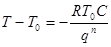
Фазовым переходом 1-го рода – называются такие переходы при котором скачком меняется первая производная химического потенциала. Поскольку:
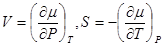
То можно описать процессы плавление, испарение и обратные им процессы.
Фазовые переходы 2-го рода - это переходы первое произведение химического потенциала  непрерывны, а скачком меняется 2-е производные. Теплота таких фазовых переходов равно 0 поскольку энтропия непрерывна
непрерывны, а скачком меняется 2-е производные. Теплота таких фазовых переходов равно 0 поскольку энтропия непрерывна
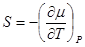
Cкачкообразные изменение претерпевают удельная теплоемкость
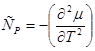
Коэффициент объемного расширения
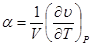
И изометрическая сжимаемость вещества:
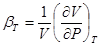
В отличие от фазовых переходах первого рода при фазовых переходe второго рода состояние системы меняется не прерывно и в точках фазового перехода меняется фаза объема не меняется 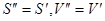 , но коэффициент теплоемкостного расширение
, но коэффициент теплоемкостного расширение 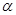 и сжимаемость
и сжимаемость 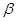 испытывает скачки. Связь между этими скачками и наклоном кривой равновесия в точке перехода определяется уравнением Эренфеста. Уравнение Клапейрона-Клаузиуса имеет вид:
испытывает скачки. Связь между этими скачками и наклоном кривой равновесия в точке перехода определяется уравнением Эренфеста. Уравнение Клапейрона-Клаузиуса имеет вид:
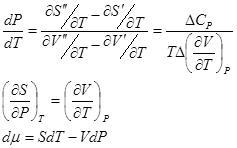
Из последних формул получаем уравнение Эренфеста для фазового перехода второго рода:
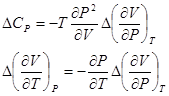
| <== предыдущая | | | следующая ==> |
| Традиции Салтыкова-Щедрина в литературе ХХ века | | | Рецептов для хорошей памяти и ясного ума |
Date: 2015-09-17; view: 1233; Нарушение авторских прав