
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

ОРГАНИЗМЫ-КОНЦЕНТРАТОРЫ 2 page
|
|
Общая направленность биогеохимического круговорота азота на планете - аккумуляция в молекулярной форме в атмосфере (рис. 11). Огромное количество азота содержит биосфера в связанном виде: в органическом веществе почвенного покрова (1,5x10" т), в биомассе растений (1,1x10^), в биомассе животных (6,1х107т).
В больших количествах азот содержится в биогенных ископаемых.
Вместе с тем, вследствие высокой растворимости солей азотной кислоты и солей аммония, азота в почве мало и почти всегда недостаточно для питания растений. Поэтому потребность культурных растений в азоте всегда велика.
В связи с этим велика и роль азотных удобрений: 30- 35 млн. тонн азота ежегодно вносится в почву в виде минеральных удобрений. Поступление за счет азотных удобрений составляет 30% от общих поступлений азота на сушу и в океан.
Это часто приводит к загрязнению среды и тяжелым заболеваниям человека и животных. Особенно велики потери нитратных форм азота, так как он не сорбируется почвой, легко вымывается водами, восстанавливается в газообразные формы и до 20-40% его теряется для питания растений. Все это, естественно, сказывается на биогеохимическом цикле азота.
Существенным и тревожным нарушением цикла азота является сильное увеличение отходов животноводства, отходов и стоков больших городов, поступление в атмосферу NH3 и оксидов азота при сжигании угля, нефти, мазута и т.д. Опасно проникновение оксидов азота в стратосферу (ядерные взрывы, выхлопы сверхзвуковых самолетов, ракет), так как это может быть причиной разрушения озонового слоя.
Таким образом, для удовлетворения нужд человечества потребность в азотных удобрениях должна быть компенсирована как можно быстрее. Но культура их применения должна быть более высокой.
АММОНИФИКАЦИЯ, разложение микотороорганизмами азотсодержащих органических соединений (белков, мочевины, нуклеиновых кислот и др.) с образованием свободного аммиака; один из важнейших этапов круговорота азота в природе, приводящий к обогащению почвы усвояемыми формами азота. В результате жизнедеятельности и гибели организмов в почву и водоемы попадает много азотсодержащих органических веществ, которые благодаря аммонификации минерализуются и могут быть вновь использованы растениями и различные микроорганизмами. При аммонификации соединения вначале гидролизуются при участии соответствующих ферментов до более простых соединений, используемых клеткой в процессах метаболизма. Микроорганизмы, участвующие в аммонификации белков, называют гнилостными, мочевины - уробактериями. Некоторые бактерии в процессе нитратного дыхания восстанавливают до аммиака нитраты. Нитрификация — микробиологический процесс окисления аммиака до азотистой кислоты или её самой далее до азотной кислоты, что связано либо с получением энергии (хемосинтез, автотрофная нитрификация), либо с защитой от активных форм кислорода, образующихся при разложении пероксида водорода (гетеротрофная нитрификация). Денитрификация (диссимиляционная нитратредукция) — сумма микробиологических процессов восстановления нитратов до нитритов и далее до газообразных оксидов и молекулярного азота. В результате их азот возвращается в атмосферу и становится недоступным большинству организмов. Осуществляется только прокариотами (причём как бактериям, так и археями) в анаэробных условиях и связана с получением ими энергии.
17. Круговорот фосфора в природе сильно отличается от биогеохимических циклов углерода, кислорода, азота и серы, так как газовая форма соединений фосфора (на-пример, РН3) практически не участвует в биогеохими- ческом цикле фосфора. Значение фосфора в жизни клетки и организмов очень велико: соединения фосфора входят в состав тканей мозга, скелета, панцирей. По-этому главная роль в биогеохимическом цикле фосфора принадлежит живому веществу и таким процессам, как питание, размножение, передвижение. Для растений наиболее доступным является фосфор неспецифических органических соединений и гумуса, и именно он играет главную роль в малом (локальном) биологическом цикле фосфора (рис. 12).
В почвах и породах широко распространено явление фиксации фосфора. Фиксаторами фосфора являются гидрооксиды железа, марганца, алюминия, глинистые минералы (особенно группы каолинита). Однако фик-сированный фосфор может на 40 - 50 % быть десорбирован и использован растениями. Это зависит от условий. Повышенная кислотность среды, образование Н2СОэ способствуют десорбции фосфора и усилению миграции фосфорных соединений.
В восстановительной среде образуются соединения фосфора с двухвалентным железом, и это тоже способ-ствует выносу фосфора из почвы. Миграция фосфора возможна и за счет таких явлений, как водная и ветровая эрозия. Поэтому биогеохимический цикл фосфора значительно менее замкнут и менее обратим, чем циклы углерода и азота, а загрязнение окружающей среды фосфором особенно чувствительно (рис. 13).
Фосфорные удобрения являются важным и необходимым звеном в получении урожаев сельскохозяйственных культур, однако, известные ныне запасы месторождений фосфатов, апатитов весьма ограничены и по предсказаниям ученых истощатся через 75-100 лет.
В то же время соединения фосфатов в последнее время становятся важнейшим фактором загрязнения речных и озерных вод (табл. 32).
В последние 50-75 лет общая картина распределения и миграции фосфора в биосфере резко нарушена человеком. Вот слагаемые этого явления.
1. Мобилизация фосфора из агроруд и шлаков, производство и применение фосфорных удобрений.
Производство многочисленных фосфорсодержащих препаратов и их использование в быту.
2. Производство фосфорсодержащих ресурсов продовольствия и кормов, вывоз и потребление их в зонах концентрации населения и больших городов.
3. Развитие рыбного и китобойного промыслов, добыча морских моллюсков, водорослей влечет за собой перераспределение фосфора с океана на сушу.
В итоге наблюдается процесс фосфотизации суши. Процесс этот проявляется неравномерно. Увеличивается содержание фосфора в окружающей среде больших городов, индустриальных центров, и, наоборот, страны, экспортирующие органические продукты и не применяющие фосфорных удобрений, теряют запасы фосфора в своих почвах.
18. Сера является одним из элементов, играющих важную роль в круговороте веществ биосферы. Она определяет важные биохимические процессы живой клетки, является компонентом питания растений и микрофлоры. Соединения серы участвуют в формировании химического состава почв, в значительных количествах находятся в подземных водах, а это, в свою очередь, играет решающую роль в процессах засоления почв.
Содержание серы в земной коре составляет 4,7x10_2%, в почве - 8,5х10_2%, в океане - 8,8х10‘2% (Виноградов, 1962; Ковда, 1985). Однако в засоленных почвах содержание серы может достигать значений, измеряемых целыми процентами. Сера имеет ряд изотопов, среди которых в природных соединениях наиболее распространены S32 (95,06%) и S34 (4,18%). В результате биогеохимических и биологических процессов происходит изменение в соотношении этих изотопов в сторону увеличения легкого изотопа в верхних гумусовых горизонтах почв. Это свидетельствует в пользу того, что интенсивный биологический круговорот серы в почвах охватывает только ее верхние слои.
Однако почвенно-грунтовые воды и подземные воды также принимают участие в биогеохимическом цикле серы. На это указывает сходство изотопного состава серы подземных, почвенно-грунтовых вод и воднорастворимых сульфатов из горизонта С сульфатно-содовых солончаков и свидетельствует об участии серы подземных вод в формировании сульфатно-содового засоления. Таким образом, в засоленных почвах биогеохимический круговорот серы не ограничивается верхними гумусовыми горизонтами, а охватывает значительную толщу: 5-10 и более метров (Буйлов, Буйлова, 1976).
Промышленные процессы и перевозки серных отходов уносят в атмосферу большое количество серы. В отдельных случаях значительная концентрация серы в воздухе служит причиной нарушений в окружающей среде. Двуокись серы (точнее, ее присутствие в воздухе) поражает как высшие растения, так и лишайники, причем эпифитные лишайники могут служить индикаторами на повышенное содержание серы в воздухе, так как их чувствительность к появлению S02 в воздухе значительно выше. Связано это с тем, что лишайники впитывают (поглощают) влагу из атмосферы всем слоевищем. Именно поэтому концентрация серы в них быстро достигает предельно допустимый уровень и организмы погибают.
Однако, несмотря на признание важности роли серных соединений в функционировании биосферы, информации о биогеохимическом циркулировании серы и ее балансе недостаточно. Более подробно этот вопрос рассмотрели Дж. П. Френд (1976) и Ф. Я. Шипунов (1980).
Биогеохимический цикл серы состоит из четырех стадий (рис.14).
I. Усвоение минеральных соединений серы живыми организмами (растениями и бактериями) и включение серы в состав белков и аминокислот.
II. Превращение органической серы живыми организмами (животными и бактериями) в конечный продукт - H2S.
Окисление минеральной серы живыми организмами (серобактериями, тионовыми бактериями) в процессе сульфатредукции. На этой стадии происходит окисление сероводорода, элементарной серы, ее тио- и тетра- соединений.
III. Восстановление минеральной серы живыми организмами (бактериями) в процессе десульфофикации до H2S.
Таким образом, важнейшим звеном всего биогеохимического цикла серы в биосфере является биогенное образование сероводорода. Биогеохимический цикл серы играет основную роль в общем круговороте этого элемента в биосфере. Приходные статьи баланса серы в общем круговороте следующие (Дж. П. Френд, 1976; цит. по Шипунову, 1980).
1. Дегазация земной коры - 12 х 10'2 г/год.
2. Выветривание осадочных пород (пирит, гипс и др.) - 42 х 1012г/год.
3. Антропогенные поступления серы в виде S02 - 65 х 1012 г/год.
Итого: 119 х 1012 г/год.
Уход серы за пределы биосферы в осадочные отложения в виде сульфидов и сульфатов - 100 х 1012 г/год.
Из этих данных видно, что антропогенное поступление серы в биосферу существенно изменяет круговорот этого элемента, а приход серы в биосферу превышает на современном этапе ее расход, как результат, в биосфере в целом наблюдается приход нециклической серы.
 19.
19.
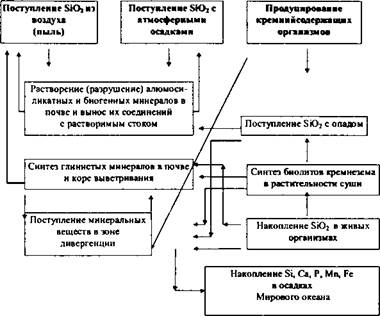
Кремний - второй по распространенности (после кислорода) в земной коре химический элемент. Его кларки: в земной коре - 29,5, в почве - 33, в океане - 5 х 10~5. Кварц и силикаты составляют 87 % всей литосферы, однако, несмотря на широкую распространенность в природе, биогеохимические циклы кремния, особенно континентальный, изучены недостаточно.
Содержание кремнезема в водах современных рек и озер составляет 10-30 мг/л, в морской воде - 0,5-3 мг/л, то есть он в природных водах находится в виде резко ненасыщенного раствора. Это связано с тем, что кремний непрерывно поглощается из воды живыми организмами.
В. И. Вернадский считал, что никакой организм в биосфере не может существовать без кремния, необходимого для образования клеток и тканей растений и животных, их твердых скелетных частей. Живое веще-ство извлекает кремний из природных вод и почв для питания и функционирования биохимических процессов, высвобождая его затем с экскрементами и при отмирании. В результате отмирания миллиардов организ-мов огромные массы кремнезема откладываются на дне водоемов. Так формируется биогеохимический цикл кремния. Процесс этот длится на протяжении многих веков геологической истории Земли. В. И. Вернадский подчеркивал, что историю кремнезема нельзя понять без анализа результатов жизнедеятельности организмов.
Идеи В. И. Вернадского получили подтверждение в трудах его ученика и соратника Я. В. Самойлова - создателя биолитной теории происхождения осадков кремнезема, фосфоритов, известняков (1921,1925). Н. М. Страхов (1966) доказал возможность биогенного и только биогенного извлечения Si02 из воды (раствора). Однако поступление растворенного Si02 с суши в ми-ровой океан недостаточно для нормального развития фитопланктона. По оценке С. В. Бруевича (1953), его поступает в 250 раз меньше необходимого количества. Именно поэтому в умеренных и тропических широтах южного и северного полушарий в (>кеане слабо развиты организмы с кремнистом скеЛ-чбм. При существующей насыщенности вод Si02 для нормального функ-ционирования фитопланктона диатомовых водорослей Si02 должен в течение года использоваться многократно (десятки и даже сотни раз). Из всей массы Si02, про-дуцированного в поверхностном фотосинтезирующем слое, донных отложений достигает не более части, а нередко и только i/50~i/100 часть. Остальной кремнезем снова переходит в водорастворимое состояние. Причем, кремнезем преимущественно образует истинные молекулярные растворы, так как коллоидный кремнезем неустойчив. В дальнейшем Si02 из воды захватывается новыми поколениями диатомовых водорослей, кремнистых губок, радиолярий.
Тем не менее, доходящая до дна ' //т часть остатков скелетов диатомового планктона приводит к большим по масштабам накоплениям кремнеземистых осадков. Эта ветвь круговорота Si02 относительно статична, необратима, так как Si02 таким путем выводится из биогеохимического круговорота (рис. 15).
Важнее другая более динамичная ветвь круговорота, которая и является собственно цикличной. Это тот
Si02, который многократно в году переходит из орга-низмов фитопланктона в окружающую среду и обратно. При этих микроциклических переходах совершается и реально проявляется наиболее важная функция водного биогеохимического цикла Si02. Это - функция энерго- и массо-переноса вещества из поверхностных в глубинные зоны Мирового океана, так как вместе с Si концентрируются и переносятся в виде труднораство-римых соединений многие элементы. Впервые эту гран-диозную функцию транспорта описал А. П. Лисицын (1974).
Вторая особенность биогеохимического цикла крем-ния в Мировом океане - его неразрывная связь с угле-родом, т.е. биогеохимические циклы кремния и углерода должны для правильного понимания путей миграции изучаться совместно.
Таким образом, в гидросфере планеты существует гидробиогеохимический цикл миграции кремнезема. Он - часть глобального цикла, но, тем не менее, является достаточно самостоятельным.
Континентальная ветвь круговорота Si02 сложна и богата разнообразными трансформациями кремнийсо-держащих соединений в природных ландшафтах, по-чвах, растительности, грунтовых водах (рис. 15). Водная миграция кремнезема тесно связана с ландшафтно-геохимическими условиями: составом растительности и литологией подстилающих отложений. В реальных условиях ландшафта на пути миграции элементов часто возникают участки, где на коротком расстоянии резко меняются условия, представляющие собой геохи-мические и биологические барьеры. Именно здесь про-исходит значительное уменьшение концентрации хими-ческих элементов, в том числе и кремнезема, в воде. Так, например, А. Г. Назаров (1976) показал, что на пере-увлажненных участках развития ленточных ельников содержание кремнезема в воде р. Таденки (приток р. Оки) резко падает до 6-7 мг/л, так как ель, особенно в молодом возрасте, является концентратором кремне-зема. Наибольшая концентрация этого элемента в водах р. Таденки была отмечена А. Г. Назаровым в ни
зовьях (17-18 мг/л), где река проходит через полосу зрелых сосновых боров и где наблюдается биогенное поступление кремнезема с массой хвойного опада и с почвенными растворами.
Влияют на растворимость кремнезема и условия сре-ды миграции. Подвижность кремнезема резко возрастает с увеличением pH среды, особенно в щелочном интервале. При pH 10-11 концентрация Si02 может достигать 200 мг/л. Сильно увеличивает растворимость аморфного кремнезема и повышение температуры. Сульфаты, бикарбонаты и карбонаты магния и кальция резко снижают растворимость кремнезема и вызывают его осаждение в виде силикатов щелочных земель или оксида. Однако в условиях сильно кислой реакции (pH 1-2) его растворимость также повышается.
Значительная часть Si02 суши расходуется на обра-зование глинистых алюмосиликатных минералов типа монтмориллонита, иллита, каолинита. Не ясно, какие процессы преобладают при осаждении Si02 - биогеохи-мические или физико-химические. Мощным механизмом, приводящим в движение этот круговорот, является растительный покров суши, в котором широко распространены процессы образования кремнеземистых органогенных минералов биолитов. Под биолитами (фитолитами) понимают минералы, образующиеся в процессе жизнедеятельности внутри организма (рис. 16). Их роль в круговороте Si02 чрезвычайно велика, но изучена недостаточно. Отложения кремнезема широко распространены в растительных клетках, в основном они инкрустируют клеточные оболочки, но возможно образование биолитов кремнезема в вакуолях и цитоплазме. Больше всего биолитов кремнезема содержат злаки, осоки, хвощи, папоротники, мхи, пальмы, хвоя сосен, елей, листья и кора вяза, осины, дуба. Например, в золе ковылей содержание Si02 может достигать 80% (Парфенова, Ярилова, 1962). Причем, биолиты кремнезема способны формироваться в крупные скопления: в стволах бамбука немецкий ботаник Коль (Kohl, 1899; цит. по Назарову, 1976) обнаружил аморфные образования кремнезема, достига-ющие в длину 4 см, массой в 16 г. Генезис почвенной крем- некислоты в некоторых условиях напрямую связан с накоплением этого элемента живыми организмами. Наиболее яркий пример - образование солодей, кремнекис- лота которых во многом накапливается благодаря деятельности диатомовых водорослей (Тюрин, 1937; Базилевич и др., 1964). Известны и другие примеры. Наиболее активная роль в процессах аккумуляции подвижных соединений принадлежит сине-зеленым водорослям. В процессе их жизнедеятельности происходит «захват» железа, марганца, кремнезема с образованием биолитов кальция и кремнезема (Парфенова, 1950; Назаров, 1974). Соотношение процессов накопления и выноса биолитов в почвах и в ландшафтах, по-видимому, сдвинуто в сторону накопления. По крайней мере, для условий умеренной зоны. Так, Л. Е. Новоросова (1951) установила, что в ельнике возраста 50 лет из хвои поступает 6 тонн крем-незема на квадратный километр поверхности подзоли-стой почвы. Кислая реакция среды не способствует ра-створению и выносу Si02 из почвы и ландшафта, и это приводит к накоплению кремнезема в поверхностных горизонтах подзолистых почв. Таким образом, растительный покров суши, особенно хвойные леса, выступает как мощный механизм, перекачивающий массы кремнезема из горных пород, почв и природных вод, и возвращающий их снова в ландшафт в форме биолитов. Последние, будучи не стойкими в условиях, резко отличающихся но своим термодинамическим характеристикам от тех, в которых они образовались (растительный орга-низм), последовательно проходят стадии кристаллиза-ции опала в мелкокристаллический халцедон и далее во вторичный кварц. Значительная часть кремнезема из биолитов включается в активную миграцию в почвенно-грунтовых водах в форме коллоидных и истинных растворов.
В круговороте кремнезема важное практическое зна-чение имеют его токсические соединения, играющие ре-шающую роль, например в развитии такого заболевания, как силикоз - результат воздействия на живые организмы аэрозолей Si02. Однако они изучены до сих пор недостаточно.
20. Педогеохимические циклы соединений железа и мар-ганца в решающей степени зависят от условий увлаж-нения, реакции среды, аэрированности почвы, условий разложения органического вещества. Миграция алюми-ния в меньшей степени зависит от окислительно-восста-новительных условий, так как он обладает постоянной валентностью. В то же время амфотерность этого эле-мента обеспечивает его зависимость от кислотно-основ-ных условий среды: в сильно кислой среде он ведет себя как катион, а в сильно щелочной - образует анионные комплексы. В нейтральных и слабо щелочных водах степей и пустынь он почти не мигрирует, наиболее вы-сока подвижность этого металла в сильно кислых водах вулканических районов и зон окисления сульфидов. Под защитой органических коллоидов алюминий мигрирует и в болотных водах. Тем не менее, интенсивность водной миграции алюминия в целом ниже, чем у железа и марганца, а его минералы более устойчивы.
Известно, что соединения железа, алюминия и мар-ганца в почвах с промывным типом водного режима миг-рируют в вертикальном направлении и образуют иллю-виальные горизонты, обогащенные полуторными окис-лами и марганцем. К. Д. Глинка (1924), К. К. Гедройц (1926), А. А. Роде (1937), Г. Вигнер (1941), С. П. Ярков (1942) доказали, что миграция полуторных окислов в условиях промывного типа водного режима происходит
в виде высокодисперсных золей, стабилизированных кислым гумусом. При этом немаловажную роль играет создание анаэробной обстановки, обусловливающей об-разование соединений двухвалентного железа и марган-ца. Решающее значение имеют агрессивные фульвокис- лоты, разрушающие почвенные минералы и образующие с железом, алюминием и марганцем легкоподвижные комплексные соединения (Тюрин, 1949; Пономарева, 1949; Александрова, 1954). В результате, например, в глеево-подзолистых почвах за год на площади 1 м2 мо-жет быть мобилизовано, перемещено и задержано от 150 до 2500 мг железа. В пересчете на 1 га это составляет от 1,5 до 25 тонн (Кауричев, Ноздрунова, 1958, цит. по: Ковда, 1973).
Соединения железа и марганца активно мигрируют и с боковым внутрипочвенным стоком, образуя скопления конкреций, пластов полуторных окислов в болотах, лу-говых и глеевых почвах, в мелководных озерах и лагу-нах. По склонам по ходу движения темно-окрашенных железисто-гумусовых вод нередко наблюдается обра-зование грунтоводных латеритов. Все это свидетель-ствует о способности этих соединений мигрировать на очень большие расстояния. Осаждение железа в акку-мулятивных ландшафтах происходит в виде бурого осадка карбонатов железа, окислов разной степени гид- ратированности, в виде фосфатов и гуматов. В степях и пустынях в условиях щелочной среды эти элементы мигрируют слабо.
В почвообразовании роли железа и марганца близки. Железо по кларку занимает 2-е место после алюминия среди металлов и 4-е среди всех элементов земной коры. Его кларк составляет 4,65. Содержание марганца в земной коре значительно ниже: 0,1%. Они занимают соседние места в периодической системе элементов Д. И. Менделеева, и имеют сходное строение электронных оболочек. Однако марганец в миграционном отношении более активен, так как значение pH, при котором из растворов выпадает в осадок Мп(ОН)2, выше, чем для Fe(OH)r
Железо и марганец активно вовлекаются в биологи-ческий круговорот, так как входят в состав многих фер-ментов. Железо участвует в образовании хлорофилла, его недостаток сказывается на интенсивности процессов фотосинтеза и проявляется заболеванием, которое назы-вается хлороз. Марганец принимает участие в окисли- тельно-восстановительных процессах: дыхании, фото-синтезе, в усвоении азота. У животных организмов и человека железо входит в состав гемоглобина крови. Кларк железа в живом веществе - 1 х 10“', кларк мар-ганца - 9 х 10~3. Миграция этих элементов возможна и в составе живого вещества. После отмирания организмов и их минерализации в почве часть этих элементов закрепляется в почве, другая же часть выносится в при-родные воды. Возвращаясь в почву, они начинают новый биогеохимический цикл (рис.17).
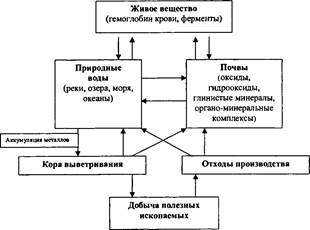 Биогеохимический цикл железа и марганца в значительной степени осложняется техногенными процессами, причем, несмотря на значительно более высокое содержание железа в земной коре, технофильность этих элементов примерно равна: TFc = (3,1 х 108): 4,65=6,6 х 107; Тм„= (6,0 х 106): 0,1=6,0 х 107, что объясняется высоким кларком железа в земной коре.
Биогеохимический цикл железа и марганца в значительной степени осложняется техногенными процессами, причем, несмотря на значительно более высокое содержание железа в земной коре, технофильность этих элементов примерно равна: TFc = (3,1 х 108): 4,65=6,6 х 107; Тм„= (6,0 х 106): 0,1=6,0 х 107, что объясняется высоким кларком железа в земной коре.
Участие алюминия в биологическом круговороте ог-раничено и на сегодня изучено слабо. Хотя в земной коре это самый распространенный металл (его кларк - 8,05), биофильность у него низкая, кларк живого веще-ства всего 5 х 10"3. Слабая подвижность алюминия оп-ределяет остаточное (за счет выноса более подвижных элементов) накопление его гидрооксидов в коре вывет-ривания влажных тропиков и образование бокситов.
В ноосфере алюминий играет исключительно важную роль, но технофильность его почти в 100 раз ниже, чем у железа.
21. Кларк кальция в литосфере составляет 2,96 %. Каль-циевые силикаты неустойчивы в зоне гипергенеза и при выветривании горных пород разрушаются в первую очередь. Поэтому кальций активно вовлечен в процессы геологического круговорота веществ.
Кальций обладает относительно высокой миграционной способностью, во многом определяемой особенностями климата. В гумидных условиях при активном развитии в почвах процесса выщелачивания он выносится в реки, озера, моря. Здесь кальций активно потребляется морскими организмами и накапливается после их отмирания в виде карбонатных отложений. В аридном и суперарид- ном климате кальций выпадает из растворов в виде карбонатов, формируя мощные толщи карбонатных пород и иллювиально-карбонатные горизонты в почвах.
Кальций играет важную роль в процессах почвообра-зования, он входит в состав почвенно-поглощающего комплекса, участвует в обменных реакциях почвенного раствора, обусловливая высокую буферную способность почв в кислом интервале среды. Гуматы кальция играют также важную роль в формировании структуры почвы, во многом обеспечивая ее водопрочность (Хан, 1969). Кроме того, кальций активно участвует в процессах осаждения полуторных окислов, марганца, нередко образуя конкреционные образования совместно с этими элементами и кремнеземом.
В почвах кислого ряда, характеризующихся значительным проявлением процесса выщелачивания, наблюдается явление биогенного накопления кальция в подстилке и аккумулятивных поверхностных горизонтах. Обусловлено это той важной ролью, которую выполняет кальций в растительных организмах. Он входит в группу элемен- тов-биофилов (Ферсман, 1934), т.е. таких элементов, которые обязательно входят в состав живого вещества и без которых существование организмов невозможно. Поэто-му кальций активно участвует в биологическом кругово-роте: на территории Европейской части СНГ раститель-ным покровом вовлекается в биологический круговорот 12,8 млн. т кальция в год (Ивлев, 1986).
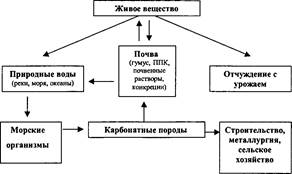 Размеры вовлечения кальция в биологический круговорот очень сильно различаются в разных природных зонах. Так, лесостепной растительностью (широколиственной и травянистой) ежегодно потребляется, по данным Т. И. Евдокимовой с соавторами (1976), 100 кг/га кальция, а тундровой растительностью - только 8,6 кг/га. В наибольшем количестве он требуется разнотравно-типчаковой растительности степей. Подсчитано, что в доисторический период его потребление с приростом составляло 137 кг/га в год. Весь этот кальций возвращался в почву с растительным опадом, т.е. малый биологический круговорот кальция носил почти замкнутый характер. В настоящее время ситуация коренным образом изменилась, растительность полей выносит ежегодно только 30-50 кг/ га кальция, но боль-шая его часть отчуждается с урожаем (рис. 18).
Размеры вовлечения кальция в биологический круговорот очень сильно различаются в разных природных зонах. Так, лесостепной растительностью (широколиственной и травянистой) ежегодно потребляется, по данным Т. И. Евдокимовой с соавторами (1976), 100 кг/га кальция, а тундровой растительностью - только 8,6 кг/га. В наибольшем количестве он требуется разнотравно-типчаковой растительности степей. Подсчитано, что в доисторический период его потребление с приростом составляло 137 кг/га в год. Весь этот кальций возвращался в почву с растительным опадом, т.е. малый биологический круговорот кальция носил почти замкнутый характер. В настоящее время ситуация коренным образом изменилась, растительность полей выносит ежегодно только 30-50 кг/ га кальция, но боль-шая его часть отчуждается с урожаем (рис. 18).
Но нарушение биогеохимического круговорота каль-ция в настоящее время происходит не только и не столько за счет отчуждения части его с сельскохозяйственной продукцией, но и за счет использования карбонатных пород в строительстве, сельском хозяйстве (известкование почв), металлургической промышленности.
Кларк магния в земной коре 1,87%, но распределение его очень неоднородно: если в ультраосновных породах его концентрация составляет 25,9%, то в основных - 4,5%, в кислых - 0,3%. По размеру ион Mg2+ такой же, как у никеля, близок к железу и кобальту. Поэтому наблюдается изоморфизм Mg2+ с Fe2+ и Ni2+, он входит в состав оливинов и пироксенов.
В то же время магний накапливается в океане и соляных озерах и по миграционной способности он приближается к таким элементам, как натрий и калий. Обусловлено это хорошей растворимостью хлоридов и сульфатов магния. В отличие от других щелочных и щелочноземельных элементов благодаря малому размеру ионного радиуса он легко входит в кристаллическую решетку глинистых минералов, образуя магнезиальные силикаты и алюмосиликаты.
Магний - биофильный элемент. Его кларк в живом веществе 0,02. Магний входит в состав хлорофилла, который при его недостатке разрушается. Растение реагирует на это явление оттоком хлорофилла из старых листьев к молодым. Передвижение пигмента идет по жилкам листа, поэтому они долгое время остаются зелеными, в то время как межжилковые участки листа желтеют. Известны и болезни животных организмов, связанные с нарушением магниевого обмена. Тем не менее биофильность магния ниже, чем у калия и кальция.
В гумидных ландшафтах магний выщелачивается из почв, хотя по сравнению с кальцием его подвижность ниже. Обусловлено это наличием нескольких геохимических барьеров. Во-первых, он активно используется живым веществом; во вторых, так же как и калий, входит в кристаллические решетки вторичных силикатов,
и, наконец, поглощается сорбционным путем глинистыми коллоидами и гумусом. В то же время значительная часть магния выносится с жидким стоком, и в грунтовых и речных водах магний стоит на втором месте после кальция.
Date: 2015-09-17; view: 1300; Нарушение авторских прав