
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Тепловые эффекты. Закон Гесса
|
|
Раздел химической термодинамики, который изучает тепловые эффекты химических реакций и фазовых переходов, называется термохимией.
Обычно химические реакции проводят при V = const или Р = const. Если V = const, то Qv = ∆Uv,
если Р = const, то Qp = ∆Up – p∆V,
таким образом, при V или Р = const теплота процесса приобретает свойства функции состояния, т.е. не зависит от пути процесса.
Qp и Qv называют изобарным и изохорным тепловыми эффектами реакций.
Независимость теплового эффекта процесса от пути его протекания была установлена опытным путем русским ученым Г.И. Гессом в 1836 г.
Тепловой эффект процесса не зависит от промежуточных стадий, а определяется начальным и конечным состояниями системы.
Математическое выражение закона Гесса:
Qv = ∆U; Ор = ∆Н
Представим себе процесс превращения исходных веществ в продукты реакции различными путями:
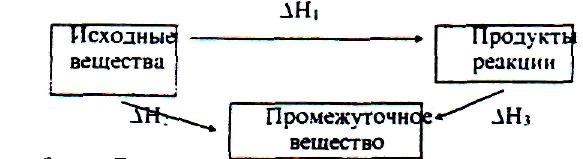
Закон Гесса утверждает, что указанные тепловые эффекты связаны между собой соотношением
∆H1 = ∆H2 + ∆H3
В термохимии используют термохимические уравнения реакций. Термохимическими называют такие уравнения, в которых приведены тепловые эффекты. Тепловой эффект реакции зависит от природы реагирующих веществ и их агрегатных состояний, поэтому а термохимических уравнениях символами (г. ж. т) обозначают состояния веществ. Например,
H2(г) + ½О2(г) = Н2О(ж) – 284,2 кДж/моль
Применяя закон Гесса. можно определять тепловые эффекты реакций, которые экспериментально определить нельзя.
Рассмотрим пример определения теплоты гидратообразования сульфата меди (II) CuSО45H2О
CuSО4 + 5H2О = CuSО45H2O.
Теплотой гидратообразования называют теплоту, выделяемую при присоединении к 1 моль твердой безводной соли кристаллизационной воды до образования устойчивого кристаллогидрата.
Экспериментальное определение теплоты образования CuSO45Н2О затруднительно, т.к. одновременно образуются кристаллогидраты различного состава.
(∆Hm)1
CuSO4 Cu2+SO42- (раствор)
(∆Hm)3 (∆Нm)2
CuSO45H2O
Гидратированные ионы Cu2+ и SO42- можно получить двумя путями:
1) растворением CuSO4 и
2) растворением CuSO4 через образование кристаллогидрата.
Исходя из закона Гесса:
(∆Нm)1 = (∆Нm)2 + (∆Нm)3
где (∆Нm)1, (∆Нm)2, (∆Нm)З – соответственно интегральные теплоты растворения CuSO4, CuSO45Н2О и теплота гидратообразования. Тогда теплота гидратообразования:
(∆Нm)3 = (∆Нm)1 – (∆Нm)2
Интегральной теплотой растворения (∆Нm) называют изменение энтальпии при растворении 1 моль вещества в некотором количестве чистого растворителя.
Закон Гесса позволяет также определять теплоты нейтрализации сильных кислот и сильных оснований.
Теплотой нейтрализации называют тепловой эффект реакции образования 1 моль жидкой воды из ионов водорода и гидроксила:
Н+ + ОН- = Н2О + Q1
Для того, чтобы можно было сопоставлять тепловые эффекты различных реакций и проводить термохимические расчеты, введено понятие теплового эффекта при стандартных условиях.
Под стандартным тепловым эффектом понимают его величину при давлении 1.01.105Па и температуре ТºК. В настоящее время термохимические исследования чаше всего проводят при 25°С. В справочных таблицах тепловые эффекты приводят при Т = 298ºК и записывают стандартный тепловой эффект – ∆Н°298.
Из закона Гесса вытекает несколько следствий, два из которых применяются для расчета тепловых эффектов:
1). Тепловой эффект реакции равен алгебраической сумме теплот образования продуктов реакции минус сумма теплот образования исходных веществ с учетом стехиометрических коэффициентов:
∆Н°298 = Σvi∆Н°298 (прод) – Σvi∆H°(исх)
Теплотой образования называют то количество теплоты, которое выделяется или поглощается при образовании 1 моль вещества из простых веществ, взятых в устойчивом состоянии при рассматриваемых условиях (р,Т).
2). Тепловой эффект реакции равен алгебраической сумме теплот сгорания исходных веществ минус сумма теплот сгорания продуктов реакции с учетом стехиометрических коэффициентов.
∆Н298 = Σvi∆Hc298(исх) – Σvi∆Hc298(прод)
Теплота сгорания – количество теплоты, которое выделяется при полном сгорании 1 моль вещества до высших оксидов при данных условиях (р, Т).
Date: 2015-09-17; view: 1707; Нарушение авторских прав