
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Химические свойства. 1. Взаимодействие с основаниями (реакция нейтрализации):
|
|
1. Взаимодействие с основаниями (реакция нейтрализации):
2HNO3 + Ca(OH)2 ® Ca(NO3)2 + 2H2O
2. Взаимодействие с основными оксидами:
2HNO3 + CuO 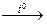 Cu(NO3)2 + H2O
Cu(NO3)2 + H2O
3. Взаимодействие с металлами:
6HCl + 2Al ® 2AlCl3 + 3H2
(металлы, стоящие в ряду напряжений до водорода, кислоты-неокислители).
4. Взаимодействие с солями (реакции обмена), при которых выделяется газ или образуется осадок:
H2SO4 + BaCl2 ® BaSO4¯ +2HCl
2HCl + K2CO3 ® 2KCl + H2O + CO2
5. При нагревании кислоты разлагаются на кислотный оксид и воду:
H2SO4 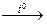 SO3 + H2O
SO3 + H2O
6. В водных растворах кислоты диссоциируют на катионы водорода и анионы кислотных остатков:
H2SO4 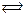 H+ + HSO4– (I ступень)
H+ + HSO4– (I ступень)
HSO4– 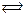 H+ + SO4 2– (II ступень)
H+ + SO4 2– (II ступень)
Ионы водорода придают кислотам кислый вкус и изменяют окраску индикаторов. Никаких других катионов, кроме ионов водорода, кислоты не образуют.
7. Действие на индикаторы:
лакмус – красный,
метилоранж – розовый
СОЛИ
Соли - сложные вещества, которые состоят из атомов металла и кислотных остатков. Это наиболее многочисленный класс неорганических соединений.
Классификация
Соли принято делить на:
| Средние |
| Кислые |
| Основные |
| Двойные |
| Смешанные |
| Комплексные |
В средних солях все атомы водорода соответствующей кислоты замещены на ионы металла, в кислых солях они замещены только частично, в основных солях группы ОН соответствующего основания частично замещены на кислотные остатки.
Двойные соли содержат два разных катиона и один анион: СаСО3 ∙МgСО3 (доломит), КСl ∙ NaCl (сильвинит), КАl(SО4)2 (алюмокалиевые квасцы).
Смешанные со ли содержат один катион и два разных аниона: СаОСl2 (или Са(ОСl)Сl).
В состав комплексных солей входит комплексный ион, состоящий из центрального атома, связанного с несколькими лигандами: K4[Fе(СN)6] (желтая кровяная соль).
Гидратные сол и (кристаллогидраты) – это соли, в которых содержатся молекулы кристаллизационной воды: СuSО4∙5Н2О (медный купорос), Na2SO4∙10Н2О (глауберова соль).
Date: 2015-09-18; view: 375; Нарушение авторских прав