
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Геометрические и энергетические характеристики атомов
|
|
Атомный радиус. Атом не имеет строго определенных границ. За его радиус принимается расстояние от ядра до главного максимума плотности внешних электронных оболочек. С увеличением заряда ядра в периодах атомный радиус немонотонно уменьшается, а в группах увеличивается.
Энергия ионизации Еi – это энергия, необходимая для отрыва наиболее слабо связанного электрона от атома, количественно выражается в кДж/моль или эВ. Чем меньше энергия ионизации, тем легче атом отдает электрон при образовании химической связи, т.е. элемент является более сильным восстановителем. Поэтому восстановительная способность нейтральных атомов с ростом заряда ядра в периоде уменьшается, в главных подгруппах растет.
Энергия сродства к электрону Еср – энергия, выделяющаяся при присоединении электрона к нейтральному атому, количественно выражается в кДж/моль или эВ. Она определяет окислительные свойства несвязанных атомов. Чем больше электронное сродство, тем более сильным окислителем является данный элемент. Окислительной способностью не обладают нейтральные атомы с устойчивыми конфигурациями s2, s2р6. У остальных элементов в таблице Д.И. Менделеева окислительная способность нейтральных атомов повышается слева направо и снизу вверх.
Электроотрицательностью элемента (ЭО) называют меру относительной способности атомов оттягивать на себя электроны при образовании химической связи. Она пропорциональна как энергии ионизации, так и энергии сродства к электрону. Имеется несколько шкал электроотрицательности. Согласно Р. Малликену, абсолютная электроотрицательность равна полусумме энергии ионизации и сродства к электрону:
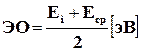 ,
,
Л. Полинг ввел относительную шкалу электроотрицательности (ОЭОR):
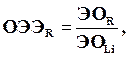
С ростом заряда в периодах электроотрицательность в общем растет, а в подгруппах падает.
Date: 2015-09-18; view: 588; Нарушение авторских прав